间歇性禁食减轻内毒素诱导小鼠葡萄膜炎的研究
关键词
摘要
全文
文章亮点
1. 关键发现
• 间歇性禁食能够抑制小胶质细胞的促炎型激活,加速内毒素诱导的小鼠葡萄膜炎的炎症消退,减轻组织结构的炎性破坏。
2. 已知与发现
3. 意义与改变
葡萄膜炎(uveitis)是一类好发于青壮年、易反复发作、并发症多且治疗棘手的严重威胁视力的眼部疾病,在世界范围内的致盲率高达10%~15%[1-3]。小胶质细胞的活化被证明参与葡萄膜炎的进展并介导其炎症损害的发生。活化的小胶质细胞释放出大量促炎性细胞因子,诱导外周血中大量免疫细胞的浸润,持续放大葡萄膜炎的破坏性炎症[4-5],使用药物干预清除小胶质细胞可以抑制炎性细胞的浸润,并避免实验性自身免疫性葡萄膜炎(experimental autoimmune uveitis,EAU)及内毒素诱导的葡萄膜炎(endotoxin-induced uveitis,EIU)的视力损害[5-6]。目前在临床治疗中,针对葡萄膜炎患者可选择的处理方案十分有限。主要包括使用糖皮质激素及免疫抑制剂等,可导致众多非特异性及严重的不良反应如高眼压、白内障等并不适于长期的治疗使用[7-8],部分患者还常见停药易复发的情况。因此寻找不良反应更少、更为有效的葡萄膜炎的治疗方案十分重要且必要。
间歇性禁食(intermittent fasting, IF)能够通过多种途径直接或间接的调节机体免疫系统,改善机体免疫环境,减轻机体炎症状态,对多种免疫疾病如多发性硬化(multiple sclerosis, MS)起到缓解作用[9]。另外,IF能够抑制促炎细胞因子如白介素-1β(interleukin-1β, IL-1β)、IL-6和TNF-α,减少循环单核细胞的数量,加速机体全身炎症状态的恢复[10]。但IF是否可以改善葡萄膜炎,目前尚不清楚。16 : 8喂养方案作为IF中常见的方案,仅将每日的进食时间限制为8 h,并没有对食物的种类和质量做更多的要求,目前已成为更易被大众所接受的主流IF方式[11]。鉴于IF已被证明具有良好的免疫调控及抗炎功能,本研究拟进行IF对EIU小鼠模型的体内疗效评估,并初步探究IF对视网膜小胶质细胞的调控作用。
1 材料与方法
1.1 动物与分组
健康的6~8周龄的雌性C57BL/6小鼠购自中山大学动物实验中心。 所有实验动物均为无特定病原体级(SPF级),予12 h光照/12 h黑暗循环。本研究已获得中山大学伦理委员会批准(许可证号SYXK[12]2024-308)。共将30只雌性C57BL/6J小鼠随机分为3组(每组n=10),即对照组、EIU组和IF+EIU组。对照组和EIU组的小鼠自由进食。IF+EIU组的小鼠采用16 : 8IF法,进食窗口为每天9:00—17:00的8 h,禁食期间可饮水。1.2 细胞系与细胞培养
小鼠小胶质细胞BV2在含有100 U/mL青霉素和100 μg/mL链霉素的DMEM/F12培养基(Pricella,PM150310,中国)中培养。对于低糖条件(low glucose, LG),细胞在无糖DMEM/F12培养基(Pricella,PM150272,中国)和含有3 151 mg/L D-葡萄糖的DMEM/F12培养基按1 : 9比例混合培养。所有细胞均在含5%二氧化碳的湿润环境中37 ℃培养。将细胞以5 × 105 cells/mL的体积浓度接种在6孔板中培养24h,并随机分为3组:对照组、LPS组(100 ng/mL)、LG + LPS组(100 ng/mL)。细胞处理方式为用100 ng/mL LPS处理6h,然后从每组提取细胞蛋白和mRNA进一步分析。1.3 方法
1.3.1 EIU模型构建经过3 d的禁食预处理后,通过玻璃体腔注射LPS诱导葡萄膜炎,建立EIU模型。小鼠右眼分别注射1μ L PBS(第1组)或1μ L 0.1μ g/μ L LPS(第2组和第3组)。在第1、3、5和7天测量小鼠的血糖和体质量。
1.3.2 光谱域光学相干断层扫描
每组小鼠均通过腹腔注射 1 % 戊巴比妥钠(0.008 mL/g)进行麻醉。在麻醉平稳后,使用复方托吡卡胺(沈阳兴齐眼药股份有限公司,中国)充分散瞳。使用光谱域光学相干断层扫描(spectral-domain optical coherence tomography, SD-OCT, Spectralis HRA+ OCT, Heidelberg Engineering, 德国)进行观察,标准OCT镜头附加+25 D镜片。小鼠水平放置在平面上,调整头部位置,使其眼睛的光轴与光学系统对齐。以小鼠视盘为中心进行径向线性扫描。检查过程中,使用透明质酸钠眼药水保持角膜湿润,确保图像更清晰。并使用ImageJ进行定量分析。
1.3.3 苏木精-伊红染色
在建立EIU小鼠模型3 d后,取每组小鼠(n =4)的眼球,在4%多聚甲醛溶液( paraformaldehyde solution, PFA)中固定24 h。然后用梯度浓度的乙醇(65%、75%、85%、95%和100%)脱水,并包埋在石蜡中。将石蜡块通过视盘切片,厚度为4μ m,脱蜡后按照生产商说明使用苏木精-伊红(hematoxylin-eosin staining, HE)染色试剂盒(DH0006-2;Leagene Biotech, 中国)进行染色。使用Tissue FAXS(TissueFAXS Spectra, 奥地利)拍摄切片照片。由2位经验丰富的研究人员使用ImageJ软件计数炎性细胞,并记录其计数的平均值。
1.3.4 视网膜铺片制备及免疫荧光染色
建立EIU小鼠模型7 d后,取每组小鼠(n = 4)的取出眼球,并在4% PFA中固定30 min后封闭2 h。为了观察神经节细胞和神经纤维,视网膜在4℃下用TUJ3抗体(1∶300, ab18207, Abcam, 美国)、Alexa Fluor 488标记的抗兔抗体(1∶500, 4412, Cell Signaling Technology, 美国)染色;用Alexa-Fluor 647标记的抗RBPMS-兔IgG(1∶800, CL647-15187, Proteintech, 美国)染色。为了观察小胶质细胞,用Alexa-Fluor 555标记的抗IBA1-兔IgG(1∶600, 36618, Cell Signaling Technology, 美国)染色。通过在视网膜上做4个径向切口,将其铺平在载玻片上,使用40倍共聚焦显微镜(LSM980 Airyscan2, Carl Zeiss, 德国)拍摄。每份视网膜铺片的4个随机区域被拍摄以量化小胶质细胞。图像使用ImageJ软件转换为8位格式,并使用Simple Neurite Tracer(SNT)插件将图像转换为骨架化形式。然后使用Analyze Skeleton(2D/3D)插件量化小胶质细胞突触的数量和长度。
1.3.5 视网膜石蜡切片免疫荧光染色
使用EIU小鼠建模7 d后的视网膜石蜡切片,经烤片、脱蜡及水化后,用Alexa-Fluor 555标记的抗IBA1-兔IgG(1∶600,36618,Cell Signaling Technology,美国)在4℃下孵育过夜。 磷酸盐缓冲溶液洗涤后,用4',6-二脒基-2-苯基吲哚( 4',6-Diamidino-2-phenylindole, Dihydrochloride, DAPI)染色细胞核。未染色的切片作为阴性对照。切片使用40倍共聚焦显微镜(LSM980 Airyscan2,Carl Zeiss,德国)拍摄。每只眼睛随机捕获4张图像,以量化小胶质细胞。 采用ImageJ进行细胞计数分析。
1.3.6 RNA提取及实时定量PCR分析
使用Trizol试剂(Thermo Fisher Scientific)从BV2细胞中提取总RNA。使用NanoDrop 1000分光光度计(Thermo Scientific,美国)测量RNA浓度。随后,使用SYBR PrimeScript RT-PCR试剂盒(Takara Biomedical Technology,北京)将RNA逆转录为cDNA。利用SYBR Green系统(RR064B,Takara Biotechnology,北京)在Roche 480仪器(Roche,美国)上进行实时PCR。炎症相关基因白介素1β(interleukin-1β, IL-1β)、肿瘤坏死因子α(tumor necrosis factor-α, TNF-α)、诱导型一氧化氮合酶( inducible nitric oxide synthase, iNOS)、 IL-6的表达水平以β肌动蛋白(β-actin)为内参进行标准化,引物序列见表1。
表 1 qPCR引物序列
Table 1 qPCR primer sequence
|
基因 |
引物名称 |
引物序列(5′~3′) |
|
IL-1β |
Forward |
GCAACTGTTCCTGAACTCAACT |
|
Reverse |
ATCTTTTGGGGTCCGTCAACT |
|
|
TNF-α |
Forward |
ACTGAACTTCGGGGTGATCG |
|
Reverse |
GGTGGTTTGTGAGTGTGAGG |
|
|
iNOS |
Forward |
GGAGTGACGGCAAACATGACT |
|
Reverse |
TCGATGCACAACTGGGTGAAC |
|
|
IL-6 |
Forward |
TAGTCCTTCCTACCCCAATTTCC |
|
Reverse |
TTGGTCCTTAGCCACTCCTTC |
|
|
β-Actin |
Forward |
AGCCATGTACGTAGCCATCC |
|
Reverse |
CTCTCAGCTGTGGTGGTGAA |
加入混合了蛋白酶抑制剂和磷酸酶抑制剂的RIPA裂解液(北京生物制品研究所有限责任公司),提取细胞蛋白质。蛋白质浓度使用BCA蛋白质测定试剂盒(北京索莱宝科技有限公司)进行测定。加入相同量的蛋白质(30 μ g)进行十二烷基硫酸钠聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate polyacrylamide gel electrophoresis, SDS-PAGE),并转移到聚偏二氟乙烯(polyvinylidene fluoride, PVDF)膜上。膜在室温下用5%牛血清白蛋白(bovine serum albumin, BSA)封闭1 h,然后在4°C过夜与兔抗-pSTAT3(1:2000, 9145, Cell Signaling Technology, 美国)、兔抗-iNOS(1:1000, GTX130246, GeneTex, 中国)、鼠抗-pSTAT1(1:1000, sc-8394, Santa Cruz, 美国)、鼠抗-TNF-α(1:200, sc-52746,Santa Cruz, 美国)、鼠抗-β-tublin3(1:500, sc-23950, Santa Cruz, 美国)一起孵育。第2天,膜被洗涤3次,然后进一步与辣根过氧化物酶(horseradish peroxidase, HRP)标记的兔抗-兔(1:10000, 7074, Cell Signaling Technology, 美国)或抗-鼠二抗(1:5000, 7076, Cell Signaling Technology, 美国)在室温下孵育1 h,再次洗涤3次后,膜使用ChemiDoc Touch成像系统(Bio-Rad, 美国)进行曝光显影。使用ImageJ软件(National Institutes of Health, 美国)对条带进行定量分析 [13]。
1.4 统计学方法
所有实验均独立重复至少3次。数据分析采用t 检验、方差分析及Tukey 's多重比较检验。所有计算和统计检验都使用GraphPad Prism 10.0 (California, USA)进行。所有结果以均值 ± 标准误(SEM)表示。P < 0.05认为差异具有统计学意义。2 结果
2.1 IF减轻内毒素诱导的小鼠葡萄膜炎表现
各组小鼠在建模前体质量比较差异无统计学意义,且均呈增加的趋势。IF预处理3 d后进行玻璃体腔内LPS注射,在建模后的第2天(5 d),与Ctr组相比,EIU组及IF+EIU组小鼠体质量水平稍下降趋势,但差异无统计学意义(P>0.05),见图1A。各组小鼠在建模前血糖水平比较差异无统计学意义(1、3 d)。在建模后的第2天(5 d),IF+EIU组较Ctr组小鼠血糖水平下降28%,较EIU组小鼠血糖水平下降26%(P<0.05),后IF+EIU组血糖水平有所回升,第7天时各组间小鼠血糖水平比较差异无统计学意义,见图1B。EIU组及IF+EIU组的小鼠眼7 d的OCT观察见图1C。与Ctr组相比,EIU组及IF+EIU组在起病早期(1~2 d),两组小鼠视网膜均增厚水肿,IF+EIU组增厚22%(P<0.05,图1D),EIU组增厚32%(P<0.001),两组小鼠各层视网膜结构基本正常,在发病中期(3~4 d)及末期(5~7 d),IF+EIU组视网膜厚度与Ctr组比较差异无统计学意义(P>0.05),EIU组仍轻度水肿增厚(P<0.01)。在早期,EIU组及IF+EIU组玻璃体腔内均可见大量炎性细胞浸润及炎性渗出物堆积,两组间比较差异无统计学意义(P>0.05),见图1E。进展至中期时,EIU组玻璃体腔内可见中等量炎性细胞与炎性渗出物,而 IF+EIU组玻璃体腔内浸润的炎性细胞与炎性渗出物明显减少,较EIU组减少了42%,组间比较差异有统计学意义(P<0.001),见图1F。至末期,EIU组玻璃体腔内仍可见少量炎性细胞浸润,IF+EIU组玻璃体腔内则几乎无炎性细胞浸润,IF+EIU组与Ctr组比较差异无统计学意义(P>0.05),见图1G。上述结果提示IF干预或能够缩短病程,加速恢复。
LPS注射后第3天,苏木精-伊红染色示EIU组视网膜水肿增厚,玻璃体腔内可见大量渗出的炎性细胞,见图1G。IF+EIU组小鼠玻璃体腔内也可见炎性细胞,但数目明显减少。与EIU组相比,IF+EIU组玻璃体腔内炎性细胞数目减少了54%,差异具有统计学意义(P<0.01,图1H)。
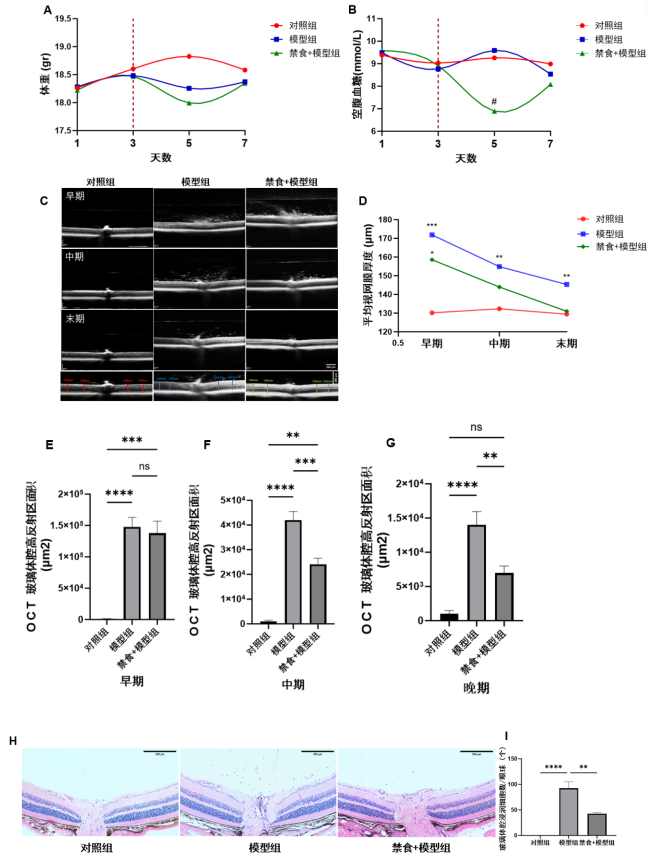
图 1 间歇性禁食减轻内毒素诱导的小鼠葡萄膜炎表现
Figure 1 Intermittent fasting treatment alleviates the manifestations of EIU
2.2 IF抑制了LPS诱导的体内视网膜小胶质细胞活化及其介导神经损伤
与Ctr组相比,EIU组的视网膜中IBA1+细胞表现出明显的激活态改变,细胞胞体变大、变圆,分支较少、较短,提示LPS激活了视网膜中的小胶质细胞。然而IF的干预抑制了该现象,IF+EIU组的小胶质细胞形态得以维持,几乎类似于Ctr组,见图2A。与Ctr组相比,EIU组中的小胶质细胞具有更少和更短的突触分支(P <0.05)。而IF逆转了LPS引起的小胶质细胞分支数目及形态的变化,IF+EIU组小胶质细胞突触分支与Ctr组比较差异无统计学意义,见图2B、C。静息状态下的视网膜小胶质细胞通常定位于内丛状层、神经纤维层及神经节细胞层。而在内毒素作用下小胶质细胞被激活,其增殖及迁移能力增强。IBA1免疫荧光染色中,各组小胶质细胞的定位与数目变化见图2D。Ctr组可见IBA1+细胞主要聚集在内丛状层。EIU组IBA1+细胞数量增加,并向神经节细胞层迁移,而IF的处理显著抑制了LPS诱导的小胶质细胞迁移和增殖(P<0.01),见图2E。
与Ctr组和IF+EIU组相比,EIU组小鼠周边视网膜处RBPMS阳性细胞(白色)密度下降(P<0.001),见图2I;神经纤维(绿色)密度变少(P<0.001),见 图2G,走行中断,粗细不均,且排列紊乱。而IF+EIU组神经节细胞数量与Ctr组比较差异无统计学意义(P>0.05),神经纤维密度稍减少,神经纤维走行尚规则,且连续性良好。上述结果提示IF可以逆转LPS诱导的视网膜神经损伤。
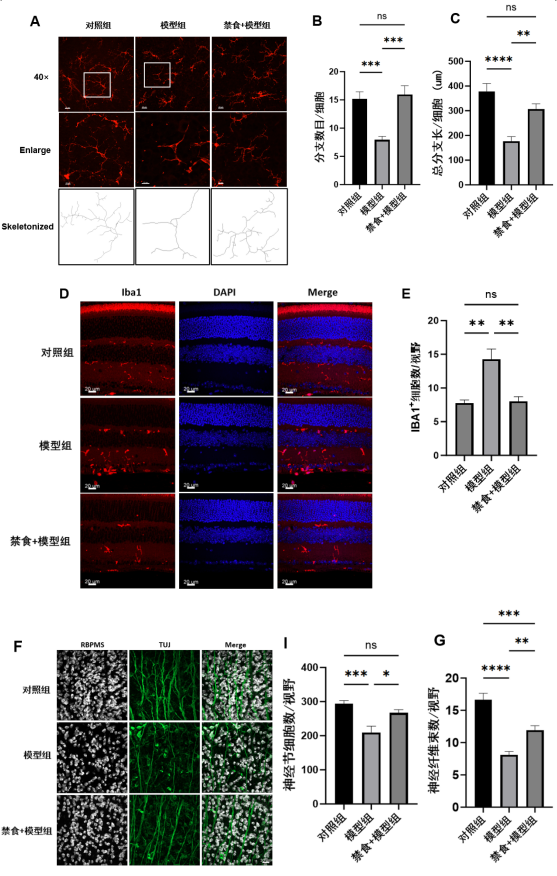
图 2 间歇性禁食抑制了LPS诱导的体内视网膜小胶质细胞活化及其介导神经损伤
Figure 2 Intermittent fasting suppressed the LPS-induced retinal microglial activation and its mediated neurotoxicity in vivo
2.3 IF抑制体外BV2细胞的活化和炎性因子产生
RT-qPCR结果显示,与Ctr组细胞相比, BV2细胞在LPS刺激下iNOS、IL-1β、IL-6及TNF-α的mRNA表达水平均明显升高。而与LPS组相比,在低葡萄糖培养干预下,这几种炎症因子的表达量则明显降低(P<0.05,图3A)。其中iNOS、IL-1β的下降更为显著(P<0.000 1)。WB结果显示,LPS能够诱导激活BV2细胞,激活相关炎症因子iNOS、TNF-α的表达水平明显升高 。而在禁食的干预可逆转BV2的激活(P<0.05)。以上结果提示,禁食干预能显著抑制LPS诱导的STAT1/3信号传导,抑制小胶质细胞的激活,减少促炎因子的产生与释放。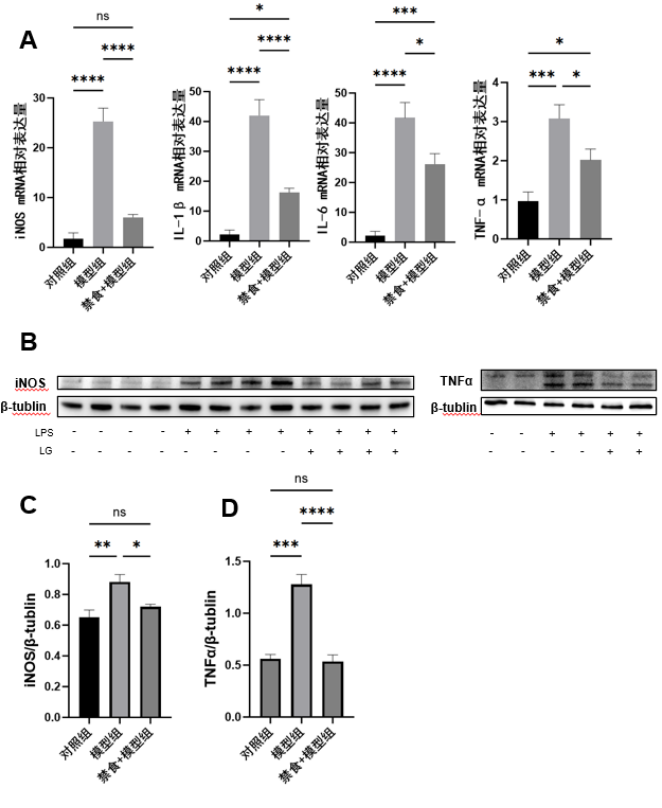
2.4 IF抑制了体外BV2细胞中LPS诱导的STAT1/3信号通路
LPS诱导BV2细胞p-STAT1及p-STAT3的表达(P>0.05),且在禁食的干预下明显下调了STAT1及STAT3的磷酸化(P<0.05)。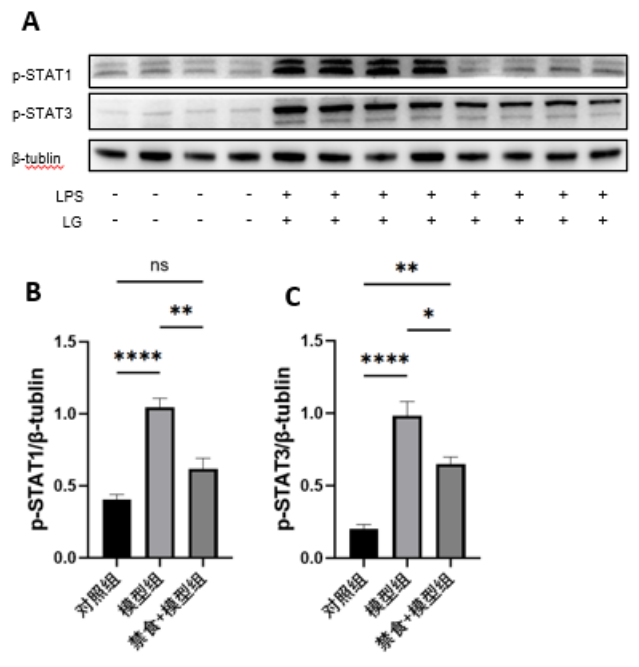
图 4 间歇性禁食抑制体外BV2细胞中LPS诱导的STAT1/3信号通路
Figure 4 Intermittent fasting suppresses LPS-induced STAT1/3 signaling in BV2 cells in vitro
3 讨论
葡萄膜炎是一种可导致眼内多个组织发生炎症性破坏的疾病,若无法得到及时、有效治疗,极易出现多种并发症。而累及眼后段结构的葡萄膜炎,其反复发作的炎症反应更会对视网膜及视神经造成不可逆的损害[14],不仅会导致患者视力剧烈下降,甚至会引起视神经萎缩,严重降低患者生活质量。而目前临床中针对葡萄膜炎的治疗,尚未发现长期有效且不良反应少的治疗管理方案。
IF能够通过多种方式改善机体免疫环境、减轻机体炎症状态,已经在其他多种疾病包括全身免疫性疾病的研究中得到充分证明[9, 15-16]。而其在眼部疾病的讨论,大多局限于糖尿病性视网膜病变等与代谢异常相关的疾病中,在眼免疫性疾病的研究尚未见报道,本研究采用了内毒素诱导的小鼠葡萄膜炎模型进行了该方面的探讨。
本研究显示,短期的IF不会引起小鼠体质量的急剧波动,这与前人的研究相一致[17],说明该禁食方案对全身营养状态的影响较为温和,机体耐受性良好。另一方面,在健康情况下IF对机体血糖无明显影响[18],而结果显示,在炎症发生早期,短期的IF足以降低小鼠空腹血糖。提示该饮食方案对葡萄糖依赖的病理生理过程可能具有潜在的调控作用。如先前的研究证实,禁食饮食方案能够通过降低葡萄糖水平,抑制肿瘤相关巨噬细胞在缺氧条件下的活性及M2型极化[19],从而发挥抗肿瘤细胞迁移与血管生成等作用。
前人的研究发现,禁食可以导致血液中循环的单核细胞数显著减少,改善慢性炎症性疾病,但并不会影响机体为响应急性炎症和组织修复过程中所需要的单核细胞的紧急动员[20]。通过OCT对小鼠玻璃体腔炎症的观察,EIU组与IF+EIU组在疾病早期的炎症表现比较差异无统计学意义,而自疾病中期开始,IF+EIU组的炎症表现明显轻于EIU组。病理学检查结果也与OCT结果相一致,在炎症反应的中期IF干预组小鼠玻璃体腔内的炎性渗出明显减少,组织破坏减轻。说明短期IF无法抑制葡萄膜炎症始发,但可有效促进葡萄膜炎症的终结或消退。
视网膜小胶质细胞的激活是葡萄膜炎持续进展并引起视网膜及视神经损害、破坏视力的关键因素。研究发现,促炎激活后的小胶质细胞(M1型)会破坏视网膜的血-视网膜屏障,诱导血液中的免疫细胞大量浸润,并累及视网膜,持续放大葡萄膜炎的破坏性炎症。而在小胶质细胞缺失的情况下,葡萄膜炎则根本不会发生[5]。此外,活化后的小胶质细胞其代谢状态也由氧化磷酸化转变为更加消耗葡萄糖的无氧糖酵解形式[21],而高水平的糖酵解也会进一步促进众多有害炎症介质的产生。本研究显示,IF在体外和体内均能够有效抑制小胶质细胞的激活,减少相关促炎细胞因子的产生与释放。这一过程在脑部疾病的研究中也被证实[22],与本研究结果部分一致。这证明了包括IF在内的能量限制饮食能够调控小胶质细胞的免疫表型。
本研究中还显示,IF可以显著减轻LPS诱导的视网膜神经损伤,保护视网膜功能免受炎症的破坏,这与前人的报道相一致。据描述,IF饮食能够通过抑制神经胶质细胞的活性,促进热休克蛋白-70(heatshockprotein70, HSP-70)及脑源性神经营养因子(brain-derived neurotrophic factor, BDNF)的产生,发挥视网膜神经保护作用[23]。另外也有研究者发现,IF的神经保护作用主要通过调节小鼠肠道菌群的组成,调节代谢物的信号传导,恢复星形胶质细胞及小胶质细胞的平衡,从而抑制神经系统的炎症损伤[24]。
STAT1和STAT3长期被视为在免疫激活和炎症途径发挥重要作用的关键转录因子[25]。STAT信号通路在小胶质细胞和巨噬细胞的极化过程中发挥着关键作用。当细胞受到刺激时,其表面的受体被激活并与胞内的酪氨酸激酶Janus 激酶(Janus kinase,JAK)相互作用,触发了胞浆中STAT的磷酸化激活。经磷酸化激活后的STAT迁移至细胞核,促进特定靶基因的转录,进而调控小胶质细胞/巨噬细胞向不同亚型激活。例如,STAT1参与介导的IL-12和iNOS等基因的转录,促使巨噬细胞向M1亚型极化。Liang等[26]的研究揭示,通过降低SOCS1的表达水平,可以激活JAK1/STAT1信号通路,从而促进巨噬细胞向M1型极化。而降低STAT3信号通路的激活有助于抑制神经元死亡,并抑制小胶质细胞M1型极化。研究显示,通过抑制细胞因子信号转导抑制因子1( suppressor of cytokine signaling 1, SOCS1)/JAK2/STAT3信号轴,能够降低蛛网膜下腔出血后的炎症反应,抑制神经功能的损失和神经元的凋亡[27]。此外,STAT1和STAT3在胞质内还有与NF-κB结合的能力,进而激活小胶质细胞,促进一系列下游的促炎基因表达[28]。经研究证实,中药成分芦荟素能够抑制STAT1/3的磷酸化激活及核内移位,以抑制巨噬细胞的激活,从而缓解LPS介导的炎症反应[29]。本研究也表明,葡萄糖饥饿处理能够显著下调LPS诱导的小胶质细胞中p-STAT1及p-STAT3的表达水平,并显著抑制既是STATs的下游靶点,也是小胶质细胞M1极化的标志物的iNOS的表达。由此推测IF减轻LPS诱导的葡萄膜炎,可能部分是通过抑制STAT1/3信号的传导以抑制小胶质细胞的M1型活化,进而发挥抗炎及保护性作用。
综上所述,IF能够在LPS诱导的葡萄膜炎中发挥抗炎作用,加速炎症反应的终结,减轻炎症反应对组织的破坏,并具有一定的神经保护作用。提示IF饮食管理可在非药物干预情况下达到减轻葡萄膜炎病情、缩短病程的效果。另一方面,IF能够抑制葡萄膜炎中小胶质细胞的促炎型激活。抑制小胶质细胞内STAT1/3信号的传导可能是其部分调控机制。本研究开创性地将“饮食调控”作为一种干预手段引入对葡萄膜炎治疗的探讨中,使IF有望成为能够缓解葡萄膜炎发生与发展的有效辅助治疗方式之一。在减轻葡萄膜炎患者治疗费用负担、现有药物不良反应以及丰富疾病治疗全流程管理方面具有重要意义。
利益冲突
所有作者均声明不存在利益冲突。开放获取声明
本文适用于知识共享许可协议 (Creative Commons),允许第三方用户按照署名(BY)-非商业性使用(NC)-禁止演绎(ND)(CC BY-NC-ND)的方式共享,即允许第三方对本刊发表的文章进行复制、发行、展览、表演、放映、广播或通过信息网络向公众传播,但在这些过程中必须保留作者署名、仅限于非商业性目的、不得进行演绎创作。基金
This work was supported by the Science and Technology Program of Guangzhou (202102080039), China