液相芯片技术及其在泪液细胞因子检测中的应用
关键词
摘要
液相芯片技术是一种利用混悬在液相中的分类编码微球作为反应及信号检测载体,集合流式细胞技术、激光技术、数字信号处理技术及传统化学技术为一体的新型生物分子检测技术。它充分利用发展成熟的流式细胞术检测原理,对目标分子(如核酸、蛋白质等)进行高通量分析。目前已在生物医学研究中得到了广泛的应用。现就其技术原理、特点及其在泪液细胞因子检测中的应用作简要介绍。
全文
一、液相芯片技术原理
液相芯片技术是一种以悬浮于液相中经过特殊编码、可识别的微球为载体,应用流式细胞术原理同时检测多个生物分子(抗原、抗体、蛋白质、核酸等)的阵列分析技术[1-6]。液相芯片的反应体系包括:微球、探针分子、被检测物和报告分子(图 1)。最常用的微球编码技术是光学信号(荧光、红外线、光散射、可见光)[7]。微球内部的物质受激发后产生不同的信号,从而将不同的特异性反应区分开来(定性、分类)。微球通过表面修饰的功能基团共价连结于能与被检测物特异性结合的探针分子。报告分子通常是一种能与被检测物特异性结合的标记有荧光的分子(如:抗体、抗原、核酸等)。报告分子可为不同的特异性反应提供检测信号(定量)[2]。先将编码的微球与探针分子结合(通常已由产品公司完成),再依次加入样品及报告分子。不同微球上的探针分子与样品中需要检测的各种目标分子进行特异性结合反应,目标分子再与报告分子发生特异性结合,即构成了一个液相芯片反应体系。可在同一混悬体系中对同一样品中的多种目标分子进行同时分析。
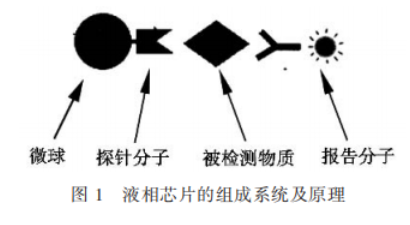
图1 液相芯片的组成系统及原理
目前商业化的液相芯片技术平台主要有:Luminex xMAP、BDTM FACSArray 生物分析仪、veraCodeTM(Illumina)multiplex 技术等[8]。Luminex xMAP 使用不同含量的两种荧光物质(红色和红外线)编码微球。这两种荧光物各有 10 种不同的强度,能够组合编码 100 种不同的微球。Luminex 检测仪(如:Lumine® 100/200TM)分析通过进样管的单个微球的数个参数确定被检测物的质和量。首先微球被 635 nm 的红色激光激发,微球内的荧光物质受激发后发射出不同强度的荧光以区分不同类别的微球(定性)。然后,结合在微球上的报告分子被 532 nm 的绿色激光激发,根据记录到的荧光强度确定被检测物质的含量。Luminex 公司于 2007 年推出了新一代微球 MaGPlex 微球,又称为磁珠(MaGnetic beads),它的最大特点是微球带有磁性,使得整个检测过程可以自动完成,大大提高了检测速度。Luminex 最新推出的 FLEXMAP 3DTM 系统基本原理与 Lumine® 200TM 系统相似,使用三种不同浓度的荧光物质编码微球,可同时检测 500 种目标分子,并可多次检测 384 个不同样本[8]。
BDTM FACSArray 生物分析仪(Cytometric Bead Array, BDTM CBA)依靠不同强度的单个荧光基团编码微球,能同时检测 30 种不同的目标分子。但 CBA 的优点可以是用任何配备有 488 nm 的激发激光和能够检测和区分 576 nm 和 670 nm 发射激光的流式细胞仪进行分析。研究者可以在流式细胞仪上进行多个目标分子的检测。
veraCodeTM(Illumina)multiplex 技术在 Illumina BeadXpress reader 上进行。它使用一种独特的数字全息技术编码石英玻璃微球,同时使用标准的荧光报告分子,如:藻红蛋白、Cy3 和 Cy5 等标记被检测物。高纯度的石英玻璃可减少背景荧光,提高检测灵敏度。该系统可同时检测 48 种目标蛋白的含量。当被激光激发时,微球内的全息物质使激光发生衍射产生独特的编码图像,可被内置的 CCD 照相机记录。通过分析获得的全息编码图像和报告分子的荧光区分不同的被检测物质的质和量。
最近的纳米半导体技术研究显示可以通过在多聚微球内精确地植入不同比例的不同大小量子点(硫化锌/硒化镉纳米晶体)达到多色光学编码[9-10]。量子点荧光具有强度高、可同时发射不同波长光的特点,非常适合用于多通道检测。理论上使用 10 种不同强度的 6 种不同颜色可同时检测 106 种目标分子[11]。
二、液相芯片技术在泪液细胞因子检测中的应用
1. 液相芯片技术应用于检测泪液细胞因子的探索
泪液中含有复杂的细胞因子成分,细胞因子可调节多种细胞功能,其浓度变化可引起一系列炎症反应,也可作为疾病恢复的信号和干眼等眼表疾病的标志物[12-14]。既往,通常使用 ELISA 检测泪液中细胞因子的浓度。由于泪液样本微量,ELISA 只能检测泪液样本中复杂的细胞因子中的 1 ~ 2 个细胞因子的浓度,很难进行多个细胞因子间的比较,不能够得到泪液中各种细胞因子之间相互作用和整体变化的结果,存在需要大量检测样本、操作繁琐、费时等问题[2, 15-16]。
液相芯片技术具有高通量、高灵敏度、高特异性的特点,非常适合于同时检测微量泪液样本中的多个细胞因子[2, 6, 17]。对多个细胞因子水平进行全面监测与评价比监测单个细胞因子更能反应疾病发生与发展的整体变化。Morgan 等[6]应用液相芯片技术检测了血浆、泪液、痰等不同标本中的 14 种细胞因子,并与 ELISA 法进行比较,结果表明两者之间具有较好的相关性。Narayanan 等[18]利用液相芯片技术发现泪液中的 IL-1β 水平较低(0.37 ~ 7.62 pG/ml),应用酶免疫分析法未能检测到。与 ELISA 相比,液相芯片技术的有效检测范围更宽,灵敏度相似或更高[6, 19-20]。我们利用液相芯片技术和 ELISA 检测了正常人泪液中 EGF 浓度,两种方法的结果有良好的相关性[21]。
最近,已有较多的研究应用液相芯片技术检测泪液中的各种细胞因子,但由于不同的技术平台及不同厂家提供的试剂盒所使用的标准品不一致,报道的各种细胞因子浓度的绝对值存在较大的差异(表 1)。Lafrance 等比较了 2 家应用液相芯片技术的仪器及 5 家厂商提供的试剂检测 91 位正常人(表 1)。
表 1 不同液相芯片试剂盒分析人泪液中各种细胞因子的含量
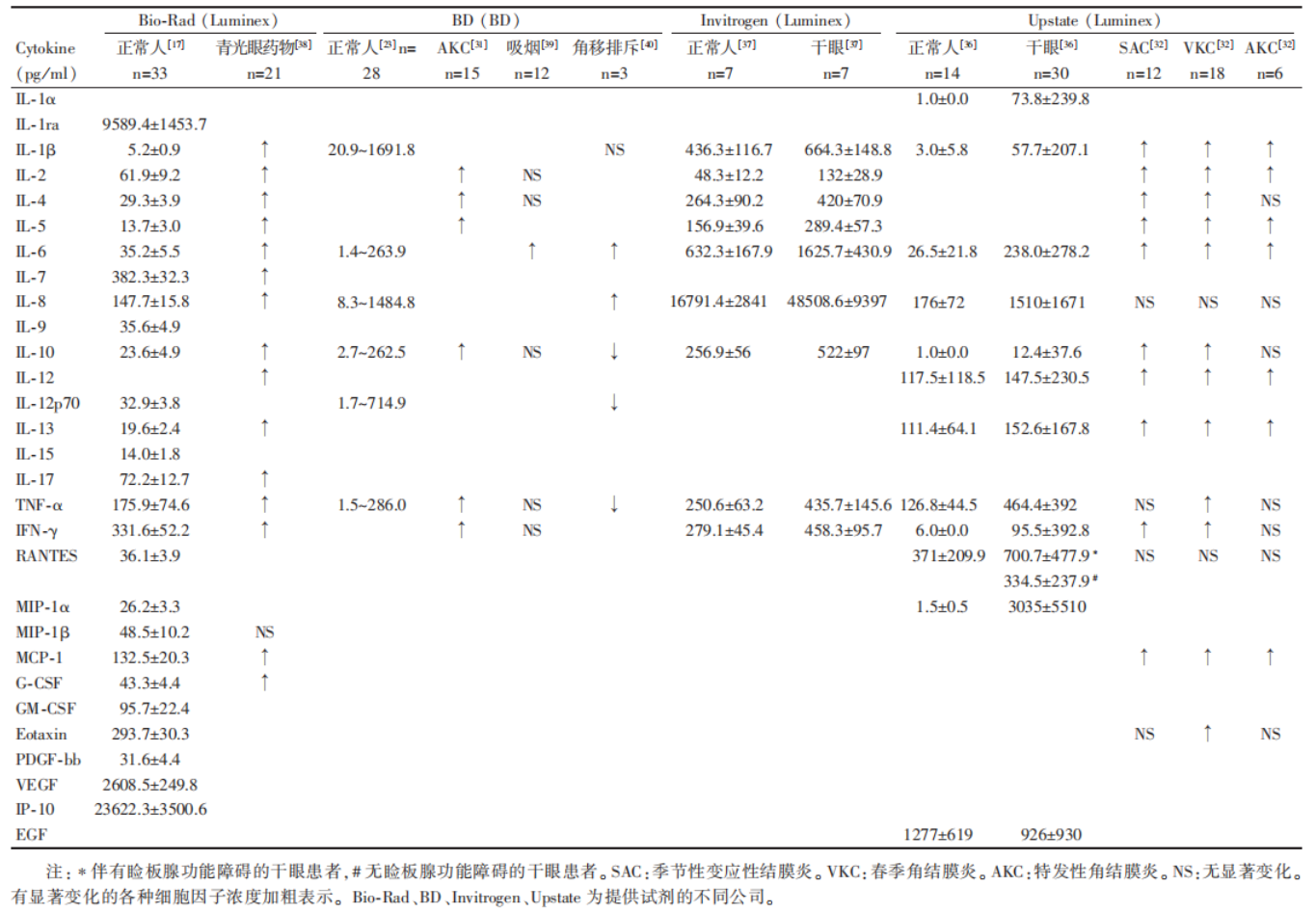
正常人(19 ~ 59 岁)泪液中的 6 ~ 27 种细胞因子的准确性、稀释线性关系和稳定性。结果表明 Luminex 的仪器及 Bio-Rad 的试剂最适合应用于泪液的液相芯片分析,其应用于检测 1 ~ 4 μl 的泪液仍具有较好的稀释线性关系(r > 0.80,P < 0.05)[17]。同时他们的结果还提示,泪液标本在 25℃放置半小时仍保持稳定,对进行液相芯片分析没有影响。
由于泪液成分复杂,各种细胞因子含量差异大,应用液相芯片技术同时检测多种成分时尚需进行探索,协调优化各项检测条件。如样本的稀释倍数、检测抗体的浓度和如何排除基质的干扰效应[8]。Martins 等[22]曾经报道,针对细胞因子检测过程中异嗜性抗体对检测目标的干扰问题,设计了特异性阻断剂,较好地解决了液相芯片技术应用中异嗜性抗体对多种细胞因子检测的干扰问题。
虽然理论上各实验室可以自行构建芯片,但目前应用液相芯片技术分析泪液的研究大多采用商品化的液相芯片试剂盒,而商品化的液相芯片主要是针对细胞因子的产品,其在泪液的检测仍局限于常见的各种细胞因子。下面就已报道的分析结果进行总结。
2. 泪液中细胞因子的正常生理变化
了解泪液中细胞因子的正常生理变化是进一步发现不同疾病状态下泪液中细胞因子的变化的先决条件。利用液相芯片技术可以较简便地监测泪液中多种细胞因子的生理变化。目前已有关于泪液中各种细胞因子在一天中的变化情况、比较基础泪液与反射泪液、睁眼与闭眼泪液中各种细胞因子的差异的报道。Uchino 等[23]利用液相芯片技术检测 28 位正常成年人泪液中 IL-1β、IL-6、IL-8、IL-10、IL-12P70 和 TNF-α 一天的变化情况相互影响。他们分别在 09:00、12:00、16:00、21:00 和 24:00 小时取样,虽然不同个体同种细胞因子水平相差较大,但其在一天中的变化都表现出特定的模式。IL-1β、IL-6、IL-10、IL-12P70 和 TNF-α 在早晨和深夜轻度升高。IL-8 在一天中维持较低的水平。促炎症因子与抗炎症因子 IL-10 的比值一天中无明显变化。其结果提示细胞因子的昼夜节律变化可能影响眼表疾病患者一天中症状轻重变化。Sonoda 等[24]利用液相芯片技术检测 23 位正常人基础泪液和反射泪液中的 IL-1β、IL-6、IL-8、IL-10、IL-12P70 和 TNF-α 水平,发现上述指标的水平无明显差异,IL-8 在反射泪液中较基础泪液明显降低。Uchino 等[25]利用液相芯片技术检测 17 位正常人 09:00 和闭眼(右眼)3 小时后泪液中 IL-1β、IL-6、IL-8、IL-10、IL-12P70 和 TNF-α 的含量,闭眼 3 h 后,虽然不同个体的同种细胞因子水平不一样,但睁眼状态(左眼)泪液中的 IL-1β、IL-6、IL-10、IL-12P70 和 TNF-α 表现出相同的升高趋势,IL-8 表现出相同的降低趋势。闭眼 3 h 之后,闭眼状态(右眼)泪液中 IL-10 的升高程度明显低于睁眼状态(左眼),其它细胞因子无明显变化。IL-10 为抗炎症细胞因子,其降低可能促进眼表的炎症反应。
3. 过敏性结膜炎患者泪液中细胞因子的变化
过敏性结膜炎主要为 IgE 介导的 I 型超敏反应所致,还可表现为 IV 型超敏反应[26-27]。特异性 IgE 异常增多介导肥大细胞脱颗粒,释放组胺、白三烯等活性介质,引发过敏反应。然而特异性 IgE 的上调机制尚未完全阐明。研究显示,B 细胞合成 IgE 具有 T 细胞依赖性,由过敏原特异性 CD4+T 细胞诱导和调节[28-29]。其中 CD4+ T 细胞分泌的 IL-4、IL-5、IL-6 和 TNF-α 促进 IgE 的合成,而 IFN-γ、IFN-α、TGF-β 抑制 IgE 合成。利用液相芯片技术同时检测多种细胞因子,可以计算各种细胞因子的比值,以便更好地理解各种细胞因子间的相互作用及致病机制。Cook 等[30]利用液相芯片技术同时检测 9 位过敏体质和 7 位非过敏体质志愿者泪液中的 6 种细胞因子(IFN-γ、TNF-α、IL-2、IL-4、IL-5、IL-10)发现过敏体质组与非过敏体质组相比:IL-10 的含量明显低,而 TNF-α/IFN-γ、IL-5/IFN-γ 和 IL-5/IL-10 的比值明显升高(IL-10 为抗炎症细胞因子),IL-5/IFN-γ 比值的升高表明 Th2 介导的体液免疫反应在过敏体质组中的过敏反应起主要作用。Nivenius 等[31]利用液相芯片技术检测 15 位特发性角结膜炎患者和 12 位正常人 IFN-γ、TNF-α、IL-2、IL-4、IL-5 和 IL-10。6 种细胞因子在特发性角结膜炎患者泪液中均升高,同时发现结膜体征的严重程度与 TNF-α、IFN-γ、IL-2、IL-4 和 IL-10 的水平显著相关。表明 Th1 和 Th2 介导的免疫反应共同参与特发性角结膜炎的发病。Leonardi 等[32]利用液相芯片技术同时检测 12 位季节性变应性结膜炎患者、18 位春季角结膜炎患者、6 位特发性角结膜炎患者和 14 位正常人的 IL-1β、IL-2、IL-4、IL-5、IL-6、IL-8、IL-10、IL-12、IL-13、IFN-γ、TNF-α、嗜酸性细胞活化趋化因子(Eotaxin)、MCP-1 和 RANTES 的浓度。他们观察到所有患者的 IL-1β、IL-2、IL-5、IL-6、IL-12、IL-13 和 MCP-1 水平均较正常对照组升高,并且这些细胞因子表现出显著的相关性。季节性变应性结膜炎患者的 IL-4、IL-5、IL-6、IL-10 和 TNF-α 水平显著高于正常对照组。
三、结论
液相芯片技术作为一种高通量、高灵敏度的检测方法,已在泪液细胞因子的检测中展现出广泛的应用前景。通过对泪液中多种细胞因子的同时检测,能够更全面地反映眼表疾病的病理生理变化。尽管目前该技术在泪液分析中的应用仍面临标准化和一致性的问题,但随着技术的不断进步和优化,相信液相芯片技术将在眼科学及相关领域发挥更重要的作用。