视盘倾斜综合征研究现状及进展
阅读量:6872
DOI:10.12419/24112601
发布日期:2025-02-28
作者:
姚浩钰 ,邹文军
展开更多 '%20fill='white'%20fill-opacity='0.01'/%3e%3cmask%20id='mask0_3477_29692'%20style='mask-type:luminance'%20maskUnits='userSpaceOnUse'%20x='0'%20y='0'%20width='16'%20height='16'%3e%3crect%20id='&%23232;&%23146;&%23153;&%23231;&%23137;&%23136;_2'%20x='16'%20width='16'%20height='16'%20transform='rotate(90%2016%200)'%20fill='white'/%3e%3c/mask%3e%3cg%20mask='url(%23mask0_3477_29692)'%3e%3cpath%20id='&%23232;&%23183;&%23175;&%23229;&%23190;&%23132;'%20d='M14%205L8%2011L2%205'%20stroke='%23333333'%20stroke-width='1.5'%20stroke-linecap='round'%20stroke-linejoin='round'/%3e%3c/g%3e%3c/g%3e%3c/svg%3e)
关键词
视盘倾斜综合征
视盘倾斜
假性视盘水肿
PHOMS
综述
摘要
视盘倾斜综合征(tilted disc syndrome, TDS)是一种以视盘形态和位置异常为主要特征的先天性眼底异常。其典型表现为视盘呈椭圆形、向下或向鼻侧倾斜,并伴随着周围脉络膜和视网膜色素上皮的发育异常。这些解剖结构的改变对患者的视功能产生深远的影响,并可能导致一系列眼部并发症的发生,如视盘旁高反射卵圆样团块状结构、脉络膜血管病变以及黄斑区病变等。在TDS的诊断过程中,通常依赖于眼底检查、光学相干断层扫描以及视野检查等多种方法的结合,以全面评估视盘的形态和功能。尽管TDS的研究已有多年,但其确切的发病机制尚不完全明确。现有研究表明,遗传因素、发育异常以及环境因素可能在TDS的发生中发挥重要作用。此外,TDS与其他眼部疾病之间的关系也是当前研究的热点问题。例如近视性视盘倾斜、视盘水肿、青光眼、视神经肿瘤等疾病在临床上常常需要与其进行鉴别诊断,以确保患者能够获得准确的诊断和适当的治疗。文章旨在全面回顾TDS的研究进展,包括其定义、流行病学特征、病理生理机制、相关视功能异常、诊断方法以及相关并发症,以期使临床医生更好地理解这一疾病的特征和机制,从而为患者的临床管理和治疗方案提供更为全面的指导。
全文
文章亮点
1. 关键发现
• 视盘旁高反射卵圆样团块状结构 (peripapillary hyper reflective ovoid mass like structure, PHOMS) 可能为视盘倾斜综合征 (tilted disc syndrome, TDS) 的重要标志,PHOMS 的转归可影响视盘倾斜综合征患者视力预后。• 高度近视引起的近视性视盘倾斜 (myopic tilted disc, MTD) 与 TDS 在临床表现上存在重叠,需进一步研究明确二者的分类标准。
2. 已知与发现
• 光学相干断层扫描技术可量化视盘倾斜角 ( 如 Bruch 膜开口平面与视神经管平面角度 ),结合眼底照相和增强深度成像光学相干断层扫描,可显著提高 PHOMS 的检出率。• TDS 可并发黄斑浆液性视网膜脱离 (macular serous retinal detachment, MSRD)、黄斑劈裂、脉络膜新生血管 (choroidal Neovascularization, CNV) 等,这些并发症的发病机制与后巩膜葡萄肿的机械牵引及血流紊乱相关。
• TDS需与MTD、视神经发育不全、视盘水肿及青光眼等疾病鉴别,其中PHOMS和血管逆向走形是TDS的重要鉴别特征。
3. 意义与改变
• 明确了 PHOMS 的诊断价值,推动 OCT 成为 TDS 的核心检查工具;对 TDS 患者定期随访可早期发现并发症,指导个性化治疗。• 需建立 TDS 的统一诊断标准,并通过纵向研究区分 TDS 与 MTD 的演变关联;PHOMS 的动态监测可能成为评估疾病预后的新指标。
• 揭示了 TDS 与其他眼底疾病的复杂关联 ( 如视盘血管炎,脉络膜新生血管 ),为多学科联合研究提供了新思路。
视盘(optic disc, OD)是视神经纤维与眼球交界处的重要解剖结构,其形态学特征在眼科临床诊断和病情监测中具有重要意义。视盘倾斜是指视盘的一侧较另一侧抬高隆起,从病因学角度可分为胚裂闭合不全导致的先天性视盘倾斜,即视盘倾斜综合征(tilted disc syndrome, TDS)和高度近视引起的近视性视盘倾斜(myopic tilted disc, MTD)。TDS由Ernst Fuchs于1882年首次描述后,已成为眼科学界广泛关注的焦点之一。本文将对于TDS的定义、流行病学、发病机制、相关视功能异常、诊断及鉴别诊断还有相关并发症进行系统回顾和综述,为临床诊治与进一步研究提供基础。
1 TDS的定义
正常视盘呈近竖椭圆形,垂直直径大于水平直径约9%,其形态主要受视神经插入的三维位置影响[1]。视盘在垂直或水平轴位上出现的一侧表面抬高被称为视盘倾斜。其相关的眼底变化也是该病的临床表现一部分,并且往往被纳入TDS本身的定义中。不同研究报告对TDS的定义不同。Apple等[2]将TDS描述为视盘向鼻下方倾斜,伴有视盘旁新月形缺损、视网膜色素上皮和脉络膜变薄、后巩膜葡萄肿形成以及视网膜血管逆向走形。TDS也被定义表现为视盘倾斜/扭转、散光屈光不正、视网膜血管逆位、β-视盘旁萎缩 (parapapillary atrophy, PPA)、鼻下脉络膜变薄、后巩膜葡萄肿、视野缺损[3]。北京眼病研究认为TDS是指具有倾斜或水平方向和椭圆形圆盘形状的相对较小的视盘,并且不伴有高度近视[4]。总的来说,TDS目前没有一致的定义,一般包括对视盘倾斜形态的描述,伴或不伴相关眼底及视觉功能异常。
图 1 典型TDS患者眼底照片
Figure 1 Fundus photos of typical TDS patients
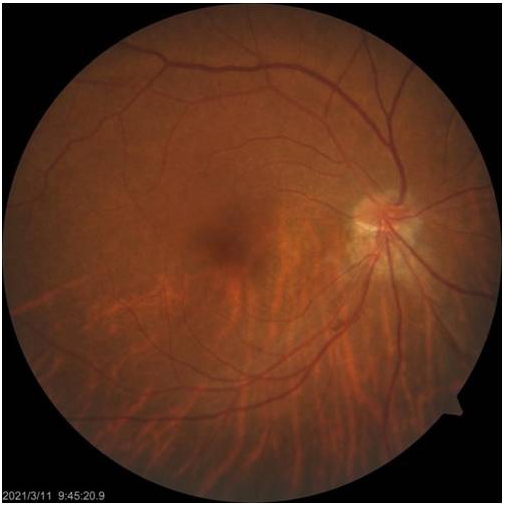
The optic disc is tilted downward, accompanied by a conus on the lower side of the optic disc, and the fundus below is atrophic.
2 TDS的流行病学
TDS是一种非遗传性疾病,80%的患者为双侧发病,男性与女性发病率没有差异[5]。其患病率较低,依据不同文献的报道,数值在0.4%~6.6%。这些研究之间患病率的显著差异不仅揭示了TDS的广泛表型,也反映了其定义的多元化。蓝山眼科研究报告显示,在散光<1.0 D的眼中,0.4%存在视盘倾斜[3]。How等[6]调查了新加坡丹戎巴葛地区2 000名年龄在40~79岁的华人,发现其中3.5%有视盘倾斜,且88.5%的视盘倾斜眼患有近视。北京眼病研究[4]纳入了平均年龄(55.9 ±10.4)岁、平均屈光不正(−0.39 ± 2.24) D的4 324名参与者,发现其中视盘倾斜的发病率为0.36%。对于儿童而言,在平均年龄为(6.3 ± 0.5)岁的中国儿童队列中,视盘倾斜的检出率为6.6%[7]。Gozde等[8]筛查了5 570名参与者的11 123只眼,发现0.83%的参与者患有先天性视盘倾斜。由于大多数文献中缺少对TDS的客观定义,且目前尚无公认的屈光变化标准来区分TDS和MTD,导致一些研究同时纳入了模棱两可的病例,从而可能造成一些报告中视盘倾斜患病率较高。3 TDS发病机制
TDS的发病机制尚不明确。由于在TDS患者的眼底观察到视盘鼻下部分的扩张和变薄,而这一部位恰是胚裂闭合的最后区域,因此经典假说认为TDS与胚裂闭合异常之间存在一定关联[9]。胚裂闭合是眼球早期发育的一个关键过程:在胚胎发育初期(妊娠第3周),神经外胚层向外突出形成视泡,视泡近端变细形成视柄与脑室保持连接;视泡远端进一步发育,形成双层结构的视杯,其不断凹陷将晶体上方和两侧包围,在下方形成胚裂。正常情况下胚裂应在妊娠第五周时闭合完全,形成完整的眼球,同时视神经由脑室通过视柄进入眼球。而由于胚裂闭合不完全,鼻下眼底变薄,视神经进入眼球的位置也随之发生偏移,视盘呈现出特征性的倾斜外观。但此假说并不能解释TDS中所有的眼底异常,特别是视盘旁新月形缺损。Giuffre[10]在此基础上将假说进一步完善,并解释了TDS中观察到的所有现象:由于视网膜神经节细胞的向心发育,一些神经纤维可能因为异常胚裂无法到达视柄并退化,视网膜神经纤维数量相对减少,视网膜变薄,无法抵抗眼压而扩张。在胚裂闭合后,脉络膜和巩膜会继发性发育,其形状受到视网膜形状的影响。因此,位于鼻下的脉络膜和巩膜会随着变薄的视网膜而扩张,形成后巩膜葡萄肿。同样的,由于视网膜上下神经节纤维的不平衡,视盘受到牵拉而向上产生位移,导致视盘倾斜;由视盘进入的视网膜血管也因此逆向走形。
4 与TDS相关视功能异常
4.1 屈光不正
屈光不正是TDS患者最佳矫正视力偏低的最常见原因,其中近视和散光患者视盘倾斜的发生率较高。研究表明,近视的严重程度与眼轴长度及视盘倾斜度相关[11-12]。散光是视盘倾斜患者中最常见的屈光不正类型,93%的视盘倾斜患者患有散光。随着健康人群散光程度的增加,视盘倾斜的风险也随之增加[13]。TDS患者的散光主要来源于角膜[14],大多为顺规散光,且角膜散光的轴位与倾斜视盘的最长直径方向有关。此外,TDS患者的晶体散光也明显更高,且主要为逆规散光,这可能是由于晶体形态变化引起的,同时TDS患者的晶体厚度和晶体轴长因子更高,可能导致晶状体倾斜[13]。4.2 弱视
TDS是一种先天性异常,其对视力的影响通常在婴儿期和儿童期视觉系统发育过程中就开始显现。Lempert和Porter[15]检查了205例年龄在3~75岁、曾被诊断为弱视的患者的视盘,发现45.4%患有视盘倾斜。Dehghani等[13]也发现在弱视在TDS中更为常见,是导致TDS患者最佳矫正视力下降的原因。同样的,Jonas等[14]也报道了弱视与视盘形状延长和角膜散光高度相关。因此对于患有TDS的幼儿,应进行屈光检查以检测和矫正散光,从而预防弱视。4.3 视野缺损
TDS患者的视野缺损通常继发于鼻下视网膜的局部扩张变薄和屈光不正,颞上象限是最常见的位置,也可能发生在周边任何地方甚至是近中央。当双眼均患有TDS时,患者可出现双颞侧偏盲[16]。该视野缺损由两部分构成,一部分是由近视和散光引起的屈光暗点,可通过戴镜矫正以减少或消除[17];而另一部分则是由于眼底扩张导致视神经轴突的局部密度降低所引发的神经源性视野缺损,即使经过适当的屈光矫正,这种缺损仍然存在[18];也有学者认为,这种不可矫正的视野缺损是由于视盘旁高反射卵圆样团块状结构(peripapillary hyper reflective ovoid mass like structure, PHOMS)消退伴随的神经萎缩。5 TDS的诊断
5.1 倾斜视盘的定性与定量
向鼻下侧倾斜的视盘是TDS最重要也是最直观的眼底表现,检眼镜和眼底照相中通常清晰可见:视盘倾斜表现为椭圆形或D形,其颞侧相对鼻侧抬高;视神经以锐角而非垂直进入眼球。视盘抬高的一侧可能会因为隆起而导致边界不清,但是毗邻完整的神经感觉层、色素上皮层(retinal pigment epithelium, RPE)和脉络膜;而视盘凹陷的部分与变薄的脉络膜以及RPE相邻。目前尚未提出“倾斜”视盘的严格定义与定量标准。Giuffrè[19]介绍了一种将视盘最大直径的长度除以垂直于该值的直径的方法,定义为最长视盘直径/最短视盘直径比(图2),即视盘的“椭圆度指数”,大于1.3被认为是视盘倾斜的标志。其他学者使用了与上述指数相反的倒置指数,即最小直径/最大直径比,小于0.8、0.75或0.7视为视盘倾斜的征兆[4, 6]。
图 2 视盘倾斜度测量
Figure 2 Optic disc tilt measurement
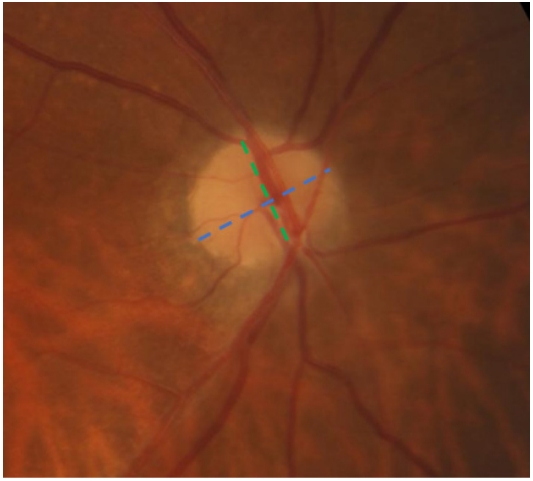
The longest optic disc diameter (blue dashed line); the shortest optic disc diameter (green dashed line).
在检眼镜或眼底照相的帮助下,临床医师可以对倾斜视盘做出主观定性,但缺乏客观的定性测量,测量者可以利用OCT技术对视盘倾斜角进行成像并量化[20]。Yoon等[21]将视盘倾斜角定义为Bruch膜开口(bruch's membrane opening, BMO)平面与通过视神经盘的视神经管平面之间的角度(图3)。通过分别在垂直和水平横截面上测量视盘倾斜角,来量化视盘的倾斜方位及角度。大多数旨在量化倾斜的研究都是为了更好地分析高度近视眼中与青光眼相关的形态变化。然而,同样的方法也可以用于TDS眼。
图 3 视盘倾斜角
Figure 3 Optic disc tilt angle
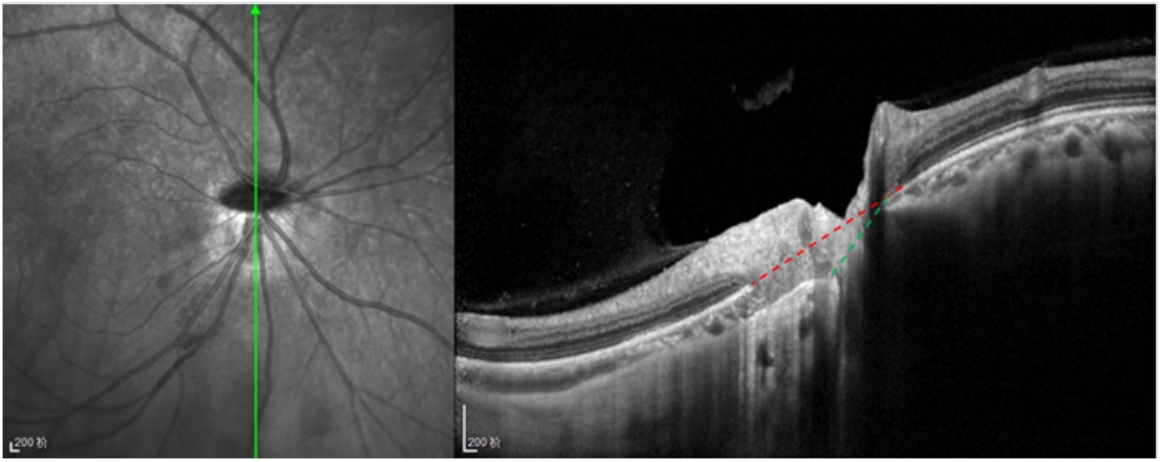
BMO plane (red dashed line); optic canal plane (green dashed line).
图 4 视盘倾斜患者视网膜血管逆向走形(红色圆圈)
Figure 4 Inversion of retinal blood vessels in patients with optic disc tilt (red circle)
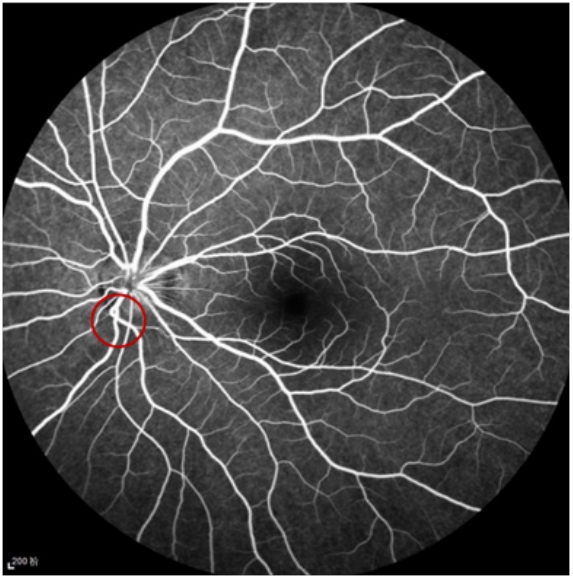
5.2 下方新月形斑
在首次描述TDS时已报告了视盘下方或鼻下的新月形斑。它对应于白色或灰色的近视盘区域,由α区(由于RPE不规则和位于周围而导致的不规则色素沉着)、β区(保留BM而完全RPE缺失)、γ区(无BM)和δ区(拉长和变薄的视盘周围巩膜凸缘)组成,δ区位于γ区内,位于视盘周围环处。在TDS中观察到的下鼻新月对应于β区萎缩。在蓝山眼科研究中,从3 583张眼底照片的数据库中诊断为TDS的77只患眼中64.9%观察到β区视盘萎缩[3]。5.3 视网膜血管异常插入及逆向走形
视网膜血管逆向走形是指血管从视盘出来后先向鼻侧走行,然后转向颞侧。这种现象可以在70% ~ 89%的TDS患者眼底观察到[3]。有报道称其他先天性视盘畸形也存在小血管异常。有学者报道在一例罕见的黄斑中心凹扁平患者眼底还同时还观察到了视盘发育不全、视盘前血管环与视网膜血管逆向走形[22]。此外,在视盘小凹中,OCT和OCTA显示视盘小凹内和视盘周围都有小的异常血管[23]。这些报告都表明,视盘的形态异常与视网膜血管的形成或获得性视网膜血管形态变化之间可能存在关系。5.4 眼底下半部苍白或后巩膜葡萄肿
TDS一直被认为是一种“停滞型”缺损,不仅影响视神经,还影响下部视网膜脉络膜。Giuffrè[19]认为胚裂的延迟闭合可能导致视盘形态变化和视网膜神经纤维的丢失,从而引起眼底下部视网膜、脉络膜和巩膜相对变薄。这种变薄导致眼底下部明显苍白,类似于近视性眼底变化第一阶段观察到的棋盘状眼底,定义为在近视眼中可以清晰地观察到中央凹周围和拱廊血管周围的脉络膜血管边界清晰[24]。相同的定义可用于描述在TDS中观察到的下方苍白区域。与TDS相关的后巩膜葡萄肿通常位于鼻下或下方。6 TDS与其他疾病的鉴别诊断
6.1 近视性视盘倾斜
TDS是一种先天性疾病,需要与后天形成的MTD相鉴别。在发病机制上,MTD并非由于胚裂闭合不全引起的,而是随着近视的加深,眼轴增长,眼球后极部逐渐受到机械牵拉,视盘周围边缘的视网膜、色素上皮和脉络膜随着时间的推移从正常位置向颞侧位移[9]。MTD同样会有视盘倾斜、视盘周围新月形、后巩膜葡萄肿、局部视网膜脉络膜变薄等一系列与TDS相似的眼底改变。但区别于TDS的视盘鼻侧倾斜,MTD的视盘倾斜方向往往位于颞侧[12]。相应地,新月形萎缩弧也通常在视盘的颞侧。TDS患者也常伴有不同程度的屈光不正,目前尚无明确的屈光变化限度来简单区分TDS与MTD,且TDS的患者随着近视的加重也可发展成MTD,因此我们需要更大队列的早期及纵向研究来明确这两者的区别与关联。6.2 视神经发育不全
视神经发育不全表现为小圆盘周围有黄色环,或称为“双环征”。视神经盘周围的血管通常在范围和形态上异常。由于胚胎在子宫内视网膜、视束、视交叉或后视路损伤而导致的视神经继发性节段性发育不全,可能造成轴突的不对称损失而使视神经盘呈现倾斜外观[9]。在发育不全的视神经盘中偶尔出现的继发性视网膜血管变化(如曲折)可能会使鉴别更加复杂。虽然相关临床病史是节段型视神经发育不全最有效的诊断方法,但通常需要核磁共振来定位视觉通路上原发性损伤的部位[25]。6.3 视盘水肿
视盘发生倾斜时,视盘一侧边缘隆起造成假性视盘水肿,需要与其他原因(如MTD、视盘玻璃疣、有髓神经纤维等)导致的假性视盘水肿、视盘水肿以及真性视盘水肿进行鉴别[26]。假性视盘水肿通常为视盘先天形态异常,也可因后天MTD引起(见前文)。视盘玻璃疣的OCT特征为清晰的低信号病灶,低信号内可伴有高反射帽或多个小的高反射聚集物[27];有髓神经纤维在检眼镜下表现为特征性的羽毛状白色不透明、有丝光泽样的髓鞘斑,可与TDS鉴别。视盘水肿特指由于颅内压升高引起的视盘神经纤维轴浆流障碍,往往伴随头痛、呕吐。除此之外,视盘水肿患者Bruch's层(BML)的常呈现W形、S形和D形;而正常人、假性视盘水肿以及视盘水肿最常见的形态是F形和V形,BML形态改变可以为视盘水肿的临床诊断提供支持[26]。真性视盘水肿是由视神经缺血、炎症、感染和肿瘤等各种病理因素导致的视盘周围神经纤维肿胀、出血。这些患者常以“视力下降”为主诉;此外,相对性传入瞳孔阻滞(relative afferent pupillary defect, RAPD)阳性以及视网膜皱褶等体征的出现也更支持视盘水肿的诊断[28];最后,核磁共振可为炎症与肿瘤引起的视盘水肿提供有力的诊断依据。6.4 青光眼
先天性 TDS 常见的下方或鼻下扩张和近视,以及下方视神经轴突密度降低,导致其视野缺损最常见的位置是颞上和上方。这些视野缺损表现为神经纤维束性缺损,与盲点有关。青光眼最初的视野缺损可能与视盘倾斜眼的视野缺损表现相似。然而,如果视野缺损随着近视矫正而减少或消失,则表明存在视盘倾斜。由于倾斜视盘与青光眼性视神经病变具有共同的特征,且缺乏特异性,目前尚无单一诊断测试能够明确区分青光眼性视神经病变和视盘倾斜,因此监测视神经和视野是否有进行性损伤的迹象仍是目前鉴别两者的要点。7 TDS常见并发症
7.1 视盘旁高反射卵圆样团块状结构
PHOMS这一名称源于通过增强深度成像光学相干断层扫描(enhanced depth imaging optical coherence tomography, EDI-OCT)成像确定的视神经盘水平B扫描(横截面)的形态学描述,其特征是位于视盘旁、Bruch膜开口(bruch's membrane opening, BMO)两侧、Bruch膜/RPE复合体上方、内部呈现均匀的高反射信号,其反射率与视网膜神经纤维层和神经节细胞层相似[29-30]。研究发现,视盘倾斜度增加与 PHOMS 有关[31-33]。2014 年的一项研究称39.5% 的TDS儿童患者有“圆顶状高反射结构”,红外图像显示视盘边缘鼻侧隆起,与神经倾斜插入一致[18]。Kim等[34]也报道了2例被诊断患有PHOMS患者在随访过程中逐渐出现了视盘倾斜。这可能是由于在TDS中筛板相对于BMO的鼻侧位移以及巩膜和筛板的逐渐拉伸,导致视神经轴突穿过筛板孔隙时引起局部应力,尤其是在鼻侧视盘的纤维中。这种异常形态容易导致慢性轴浆淤滞,进而在鼻侧形成可识别的 S 形视盘周围膨大,导致鼻侧假性视盘水肿和视盘隆起,在检眼镜和OCT上可识别为特征性的“C”形光晕(图5、6)。持续的神经纤维弯曲和轴浆流障碍可能造成损伤,对造成视野不可矫正的损害。
图 5 TDS合并PHOMS患者眼底照片
Figure 5 Fundus photos of patients with TDS combined with PHOMS
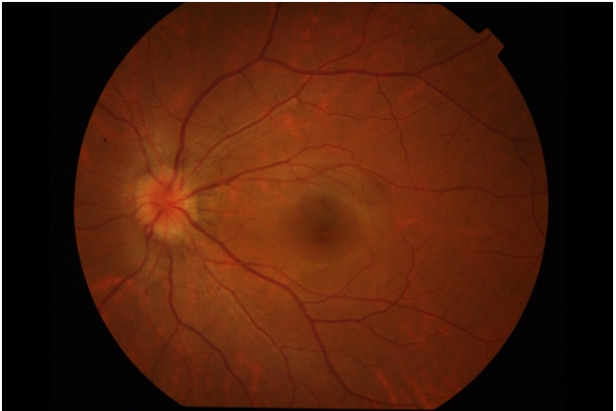
图 6 TDS合并PHOMS患者OCT成像,PHOMS(黄色箭头) Figure 6 OCT imaging of patients with TDS combined with PHOMS, PHOMS (yellow arrow)
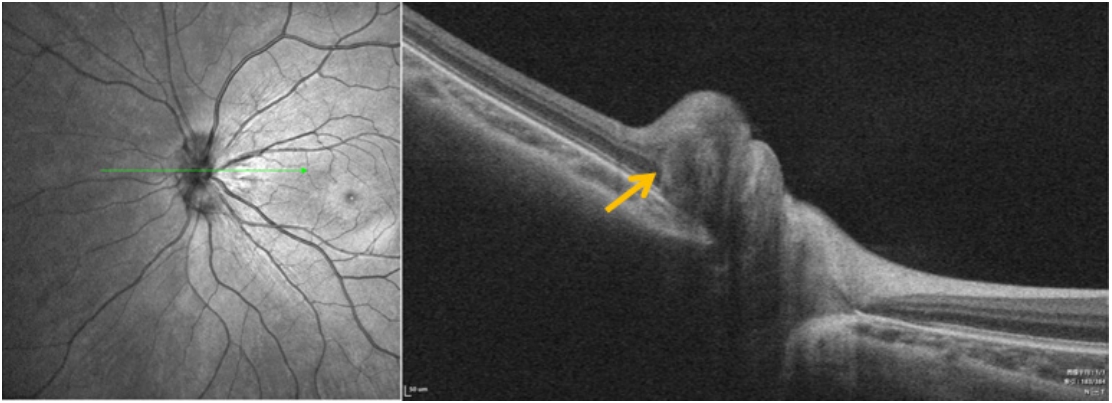
7.2 息肉状脉络膜血管病变与脉络膜新生血管
在TDS中,息肉状脉络膜血管病变(polypoidal choroidal vasculopathy, PCV)与脉络膜新生血管(choroidal neovascularization, CNV)总是位于鼻下后巩膜葡萄肿颞顶的发育不全与正常脉络膜之间的边界[35]。这可能是由2个原因导致,一方面下方眼底后葡萄肿区域脉络膜毛细血管较少可诱发缺氧;另一方面葡萄肿区域与正常区域的曲率差异可诱发血流紊乱,随后导致PCV与CNV。TDS并发的CNV参照近视性CNV治疗,而TDS中的PCV治疗方法与其他PCV病例亦无区别。7.3 黄斑浆液性视网膜脱离
黄斑浆液性视网膜脱离(macular serous retinal detachment, MSRD)是伴有眼下半部后巩膜葡萄肿的TDS最常见的黄斑并发症,患病率估计为17.3%~29.5%[35-36]。TDS并发MSRD 的发病机制尚未完全阐明,可能是由于眼底正常区域与葡萄肿区域的脉络膜厚度存在差异,下半部后巩膜葡萄肿部分的脉络膜较薄,在脉络膜厚度产生变化时,脉络膜血流可能会被部分阻塞,而这一过程可能会导致RPE改变和脉络膜通透性过高,从而导致SRD[37]。SRD的传统治疗同样适用于TDS患者[38-39],主要包括PDT[38-40]、选择性视网膜治疗(selective retina therapy, SRT)、玻璃体腔内注射抗VEGF药物治疗。目前尚无针对TDS并发SRD的既定治疗方案。7.4 黄斑劈裂
TDS中黄斑劈裂通常发生在葡萄肿区域[41-42],被认为是由于巩膜进行性扩张引起的向内牵引以及视网膜内层和视网膜血管对拉伸的相对阻力而导致的视网膜层间分离[43]。一项研究发现,与特发性黄斑裂孔患者相比,黄斑劈裂患眼内界膜表面结构存在差异,胶原纤维和细胞碎片更多[44],这强烈表明存在内部牵引力的作用。有学者认为随着TDS中下半部巩膜后葡萄肿的逐渐生长,会对Bruch膜-RPE-外层视网膜产生牵引力,而内层视网膜仍然黏附于坚固的纤维性内界膜,导致视网膜的层间分离[45]。7.5 脉络膜视网膜和视网膜色素上皮变化
脉络膜视网膜变性可见于TDS眼,通常位于眼底上部正常曲率与下部后巩膜葡萄肿的交界处。在TDS163眼中,有18眼报告了这种改变[46]。部分患者眼底可能会显示大片RPE变化带,类似于慢性中心性浆液性脉络膜视网膜病变的眼底改变。此外,有患眼可能会出现T形带状RPE改变,该带垂直于葡萄肿的上缘。这些大面积色素变化总是出现在交界区,可能是由于后巩膜葡萄肿相关的曲率变化导致的Bruch膜微破裂。因此,TDS是一种由胎裂闭合不全导致的先天性眼部缺陷,可造成假性视盘水肿,引起各种视功能异常,在临床上需要与其他视盘形态异常眼病进行鉴别。TDS与MTD都可造成视盘倾斜的外观,也可因后巩膜葡萄肿造成严重的眼底并发症。这两者的区别和联系尚不具体,后续需要更多的研究来明确TDS与MTD的分类标准与分期。PHOMS似乎是临床工作者认识TDS新的突破口,其发生与转归可能对TDS的预后产生深远影响,这两者的关联也亟待开展更多的相关研究进行探索。总之,临床医生应对TDS患者进行定期随访,以了解其视功能情况以及视盘及其周围结构形态的变化,以期对其有更为全面的认识,从而制定更有效的临床管理方案。
利益冲突
所有作者均声明不存在利益冲突。开放获取声明
本文适用于知识共享许可协议 (Creative Commons),允许第三方用户按照署名(BY)-非商业性使用(NC)-禁止演绎(ND)(CC BY-NC-ND)的方式共享,即允许第三方对本刊发表的文章进行复制、发行、展览、表演、放映、广播或通过信息网络向公众传播,但在这些过程中必须保留作者署名、仅限于非商业性目的、不得进行演绎创作。基金
1. 无锡市“双百”中青年医疗卫生拔尖人才项目(BJ2023036)。
This work was supported by the “Shuangbai” Young and Middle-aged Top Medical and Health Talents Project of Wuxi(BJ2023036).
This work was supported by the “Shuangbai” Young and Middle-aged Top Medical and Health Talents Project of Wuxi(BJ2023036).
参考文献
1. 范媛媛, 魏文斌. 视盘倾斜及其相关性研究现状[ J]. 国际眼科纵
览, 2016, 40(2): 73-80. DOI: 10.3760/cma.j.issn.1673- 5803.2016.02.001.
Fan YY, Wei WB. Research progress on morphology and associations of tilted optic disc[ J]. Int Rev Ophthalmol, 2016, 40(2): 73-80. DOI: 10.3760/cma.j.issn.1673-5803.2016.02.001.
Fan YY, Wei WB. Research progress on morphology and associations of tilted optic disc[ J]. Int Rev Ophthalmol, 2016, 40(2): 73-80. DOI: 10.3760/cma.j.issn.1673-5803.2016.02.001.
2. Apple DJ, Rabb MF, Walsh PM. Congenital anomalies of the optic
disc[ J]. Surv Ophthalmol, 1982, 27(1): 3-41. DOI:10.1016/0039-
6257(82)90111-4.
3. Vongphanit J, Mitchell P, Wang JJ. Population prevalence of tilted optic disks and the relationship of this sign to refractive error[ J]. Am J Ophthalmol,
2002, 133(5): 679-685. DOI:10.1016/s0002-9394(02)01339-9.
4. You QS, Xu L, Jonas JB. Tilted optic discs: the Beijing eye study[ J]. Eye,
2008, 22(5): 728-729. DOI:10.1038/eye.2008.87.
5. Patyal S. Visual field defects with tilted and tortedoptic discs[M]//
Resolving Dilemmas in Perimetry.Singapore: Springer Singapore, 2021:
179-184. DOI:10.1007/978-981-16-2601-2_13.
6. How ACS, Tan GSW, Chan YH, et al. Population prevalence of tilted
and torted optic discs among an adult Chinese population in Singapore:
the TanjongPagar Study[ J]. Arch Ophthalmol, 2009, 127(7): 894-899.
DOI:10.1001/archophthalmol.2009.134.
7. Guo Y, Liu LJ, Xu L, et al. Optic disc ovality in primary school children
in Beijing[ J]. Invest Ophthalmol Vis Sci, 2015, 56(8): 4547-4553. DOI:
10.1167/iovs.15-16590.
8. Orman G, Aydınoglu-Candan O, Sungur G. The prevalance of congenital
optic disc anomalies in Turkey: a hospital-based study[J]. Int Ophthalmol,
2022, 42(11): 3567-3577. DOI: 10.1007/s10792-022-02357-8.
9. Witmer MT, Margo CE, Drucker M. Tilted optic disks[ J]. Surv
Ophthalmol, 2010, 55(5): 403-428. DOI: 10.1016/j.survophthal.
2010.01.002.
10. Giuffré G. Hypothesis on the pathogenesis of the papillary dysversion
syndrome[J]. J Fr Ophtalmol, 1985, 8(8-9): 565-572.
11. 杜芬, 罗俊, 向剑波, 等. 视盘倾斜综合征的视盘及屈光状态
观察[ J]. 临床眼科杂志, 2019, 27(4): 328-330. DOI: 10.3969/
j.issn.1006-8422.2019.04.011.
Du F, Luo J, Xiang JB, et al. Optic disc and refractive status in patients with tilted disc syndrome[J]. J Clin Ophthalmol, 2019, 27(4): 328-330. DOI: 10.3969/j.issn.1006-8422.2019.04.011.
Du F, Luo J, Xiang JB, et al. Optic disc and refractive status in patients with tilted disc syndrome[J]. J Clin Ophthalmol, 2019, 27(4): 328-330. DOI: 10.3969/j.issn.1006-8422.2019.04.011.
12. Chan PP, Zhang Y, Pang CP. Myopic tilted disc: Mechanism, clinical
significance, and public health implication[ J]. Front Med, 2023, 10:
1094937. DOI: 10.3389/fmed.2023.1094937.
13. Dehghani C, Nowroozzadeh MH, Shankar S, et al. Ocular refractive
and biometric characteristics in patients with tilted disc syndrome[ J].
Optometry, 2010, 81(12): 688-694. DOI:10.1016/j.optm.2010.03.009.
14. Jonas JB, Kling F, Gründler AE. Optic disc shape, corneal astigmatism, and
amblyopia[J]. Ophthalmology, 1997, 104(11): 1934-1937. DOI:10.1016/
s0161-6420(97)30004-9.
15. Lempert P, Porter L. Dysversion of the optic disc and axial length
measurements in a presumed amblyopic population[J]. J Am Assoc Pediatr
Ophthalmol Strabismus, 1998, 2(4): 207-213. DOI:10.1016/S1091-
8531(98)90054-4.
16. Ju C, Widder J, Pham N. Tilted disc syndrome with bitemporal hemianopia
in a 67-year-old woman with high myopia and mixed/combinedmechanism glaucoma: areport of a rare case[ J]. UCLA Radiol Sci Proc,
2024, 4(3): 38-44. DOI: 10.5070/rs44353362.
17. Phu J, Wang H, Miao S, et al. Neutralizing peripheral refraction eliminates
refractive scotomata in tilted disc syndrome[ J]. Optom Vis Sci, 2018,
95(10): 959-970. DOI: 10.1097/OPX. 0000000000001286.
18. Pichi F, Romano S, Villani E, et al. Spectral-domain optical coherence
tomography findings in pediatric tilted disc syndrome[ J]. Graefe's Arch Clin Exp Ophthalmol, 2014, 252(10): 1661-1667. DOI:10.1007/s00417-
014-2701-8.
19. Giuffrè G. Chorioretinal degenerative changes in the tilted disc
syndrome[ J]. Int Ophthalmol, 1991, 15(1): 1-7. DOI:10.1007/
BF00150971.
20. Lee EJ, Han JC, Kee C. Deep optic nerve head morphology in tilted
disc syndrome and its clinical implication on visual damage[ J]. Invest
Ophthalmol Vis Sci, 2023, 64(13): 10. DOI: 10.1167/iovs.64.13.10.
21. Yoon JY, Sung KR, Yun SC, et al. Progressive optic disc tilt in young myopic
glaucomatous eyes[ J]. Korean J Ophthalmol, 2019, 33(6): 520-527.
DOI:10.3341/kjo.2019.0069.
22. Gediz BŞ, Ali Şekeroğlu M. Multimodal imaging in a case of fovea Plana
associated with situs inversus of the optic disc[ J]. Turk J Ophthalmol,
2020, 50(3): 190-192. DOI: 10.4274/tjo.galenos.2020.98415.
23. Adams MK, Cohen SY, Souied EH, et al. Multimodal imaging of choroidal
and optic disk vessels near optic disk pits[J]. Retin Cases Brief Rep, 2020,
14(4): 289-296. DOI:10.1097/ICB.0000000000000765.
24. Nghiem-Buffet S, Sibilia L, CohenSY. Tilted disc in eyes with fovea
Plana[J]. Graefes Arch Clin Exp Ophthalmol, 2023, 261(11): 3159-3164.
DOI: 10.1007/s00417-023-06161-7.
25. Denis D, Hugo J, Beylerian M, et al. Congenital abnormalities of the
optic disc[ J]. J Fr Ophtalmol, 2019, 42(7): 778-789. DOI:10.1016/
j.jfo.2018.09.011.
26. Sibony PA, Kupersmith MJ, Kardon RH. Optical coherence tomography
neuro-toolbox for the diagnosis and management of papilledema, optic disc
edema, and pseudopapilledema[J]. J Neuroophthalmol, 2021, 41(1): 77-
92. DOI: 10.1097/WNO.0000000000001078.
27. Allegrini D, Pagano L, Ferrara M, et al. Optic disc drusen: a systematic
review: up-to-date and futureperspective[J]. Int Ophthalmol, 2020, 40(8):
2119-2127. DOI:10.1007/s10792-020-01365-w.
28. Martin-Gutierrez MP, Petzold A, Saihan Z. Correction: NAION or not
NAION? A literature review of pathogenesis and differential diagnosis of
anterior ischaemic optic neuropathies[ J]. Eye (Lond), 2024, 38(3): 631.
DOI:10.1038/s41433-023-02873-6.
29. Xie X, Liu T, Wang W, et al. Clinical and multi-mode imaging features of
eyes with peripapillaryhyperreflective ovoid mass-like structures[J]. Front
Med, 2022, 9: 796667.DOI:10.3389/fmed.2022.796667.
30. Chapman JJ, Heidary G, Gise R. An overview of peripapillaryhyperreflective
ovoid mass-like structures[J]. Curr Opin Ophthalmol, 2022, 33(6): 494-
500. DOI:10.1097/ICU.0000000000000897.
31. Ly u I J, Park KA , Oh S Y. A ssociation bet ween myopia and
peripapillaryhyperreflective ovoid mass-like structures in children[ J]. Sci
Rep, 2020, 10(1): 2238. DOI: 10.1038/s41598-020-58829-3.
32. Borrelli E, Barboni P, Battista M, et al. Peripapillaryhyperreflective ovoid
mass-like structures (PHOMS): OCTA may reveal new findings[ J]. Eye,
2021, 35(2): 528-531. DOI:10.1038/s41433-020-0890-4.
33. 王静, 刘佩, 吴松笛. 误诊为视神经炎的视盘倾斜综合征合并视
盘周围强反射卵圆形肿块样结构1例[ J]. 中华眼底病杂志, 2022,
38(5): 407-408. DOI: 10.3760/cma.j.cn511434-20210802-00412.
Wang J, Liu P, Wu SD. Chin J Ocul Fundus Dis, 2022, 38(5): 407-408. DOI: 10.3760/cma.j.cn511434-20210802-00412.
Wang J, Liu P, Wu SD. Chin J Ocul Fundus Dis, 2022, 38(5): 407-408. DOI: 10.3760/cma.j.cn511434-20210802-00412.
34. Kim MS, Hwang JM, Woo SJ. Long-term development and progression
of peripapillaryhyper-reflective ovoid mass-like structures: two case
reports[ J]. J Neuroophthalmol, 2022, 42(1): e352-e355. DOI:10.1097/
WNO.0000000000001366.
35. Cohen SY, Dubois L, Nghiem-Buffet S, et al. Spectral domain optical
coherence tomography analysis of macular changes in tilted disk
syndrome[ J]. Retina, 2013, 33(7): 1338-1345. DOI:10.1097/
IAE.0b013e3182831364.
36. Garcia-Ben A,González Gómez A, García Basterra I, et al. Factors associated
with serous retinal detachment in highly myopic eyes with inferior posterior
staphyloma[ J]. Arch Soc Esp Oftalmol, 2020, 95(10): 478-484. DOI:
10.1016/j.oftal.2020.05.013.
37. Kumar V, Surve A, Kumawat D, et al. Macular associations of tilted
disc syndrome[ J]. Indian J Ophthalmol, 2021, 69(6): 1451-1456.
DOI:10.4103/ijo.IJO_1902_20.
38. Minowa Y, Ohkoshi K, Ozawa Y. Subthreshold laser treatment for serous
retinal detachment associated with tilted disc syndrome[ J]. Case Rep
Ophthalmol, 2021, 12(3): 978-986. DOI:10.1159/000520570.
39. Kubota F, Suetsugu T, Kato A, et al. Tilted disc syndrome associated with
serous retinal detachment: long-term prognosis. A retrospective multicenter
survey[ J]. Am J Ophthalmol, 2019, 207: 313-318. DOI:10.1016/
j.ajo.2019.05.027.
40. Kathare R, Gandhi P, Prabhu V, et al. Posterior staphyloma-induced serous
maculopathy: evolution and successful treatment with subthreshold
micro pulse laser[ J]. Eur J Ophthalmol, 2024, 34(6): NP48-NP53.
DOI:10.1177/11206721241272249.
41. Mizuno H, Suzuki H, Mimura M, et al. Three cases of macular hole that
occurred in inferior scleral staphyloma associated with tilted disc syndrome:
a case series[J]. J Med Case Rep, 2022, 16(1): 36. DOI:10.1186/s13256-
022-03252-7.
42. Shinohara K, Tanaka N, Jonas JB, et al. Ultrawide-field OCT to
investigate relationships between myopic macular retinoschisis and
posterior staphyloma[ J]. Ophthalmology, 2018, 125(10): 1575-1586.
DOI:10.1016/j.ophtha.2018.03.053.
43. Ikuno Y. Overview of the complications of high myopia[J]. Retina, 2017,
37(12): 2347-2351. DOI:10.1097/IAE.0000000000001489.
44. Bando H, Ikuno Y, Choi JS, et al. Ultrastructure of internal limiting
membrane in myopic foveoschisis[ J]. Am J Ophthalmol, 2005, 139(1):
197-199. DOI:10.1016/j.ajo.2004.07.027.
45. Cohen SY, Vignal-Clermont C, Trinh L, et al. Tilted disc syndrome (TDS):
new hypotheses for posterior segment complications and their implications
in other retinal diseases[ J]. Prog Retin Eye Res, 2022, 88: 101020.
DOI:10.1016/j.preteyeres.2021.101020.
46. Cohen SY, Dubois L, Ayrault S, et al. T-shaped pigmentary changes
in tilted disk syndrome[ J]. Eur J Ophthalmol, 2009, 19(5): 876-879.
DOI:10.1177/112067210901900532.