Dandy-Walker 综合征患者的眼部表现与术后随访:一项病例报告与文献综述
阅读量:2007
DOI:10.12419/24092802
发布日期:2025-08-28
作者:
崔金利 # ,刘泽浩 # ,刘桂池 ,刘欣雨 ,林英
展开更多 '%20fill='white'%20fill-opacity='0.01'/%3e%3cmask%20id='mask0_3477_29692'%20style='mask-type:luminance'%20maskUnits='userSpaceOnUse'%20x='0'%20y='0'%20width='16'%20height='16'%3e%3crect%20id='&%23232;&%23146;&%23153;&%23231;&%23137;&%23136;_2'%20x='16'%20width='16'%20height='16'%20transform='rotate(90%2016%200)'%20fill='white'/%3e%3c/mask%3e%3cg%20mask='url(%23mask0_3477_29692)'%3e%3cpath%20id='&%23232;&%23183;&%23175;&%23229;&%23190;&%23132;'%20d='M14%205L8%2011L2%205'%20stroke='%23333333'%20stroke-width='1.5'%20stroke-linecap='round'%20stroke-linejoin='round'/%3e%3c/g%3e%3c/g%3e%3c/svg%3e)
关键词
Dandy-Walker综合征
视盘水肿
视网膜神经纤维层厚度
颅内压管理
摘要
文章报道了一例5岁女性Dandy-Walker综合征(Dandy-Walker syndrome,DWS)患儿的临床表现、眼科检查及影像学特征。该患儿在确诊DWS后行后颅窝蛛网膜囊肿部分切除术,然而术后视力仍进行性下降,眼科随访过程中发现视网膜神经纤维层(Retinal Nerve Fibers Layer,RNFL)进行性变薄,提示颅内压尚未有效控制,视神经损害在进一步发展。由于DWS病变位置特殊性,头颅磁共振成像(Magnetic Resonance Imaging,MRI)及常规腰椎穿刺未能确定幕上颅内高压,后经侧脑室直接测压,证实仍然存在颅压异常增高。行右侧脑室-腹腔分流术后,患儿双眼视力有所提高,双眼RNFL)厚度无继续变薄。目前DWS的治疗方式包括后颅窝囊肿切除术、脑脊液分流术及内镜下第三脑室造瘘术。 术后DWS患者的颅内压的测量有特殊性,幕上与幕下区域之间的脑实质内压力可能形成显著的压力梯度,腰椎穿刺测压可能无法准确反映颅内压,脑室内测压方法则创伤更大。此时需要眼科检查提供支持颅内高压的证据,如RNFL厚度进行性下降、视盘水肿及视网膜血管形态异常,这些检查无创、简便、可多次重复,是临床医生评估颅内压的有效手段,建议纳入DWS患者术后颅内压的常规管理中。
全文
文章亮点
1. 关键发现
· 报道1例Dandy-Walker综合征(Dandy-Walker syndrome, DWS)出现眼部并发症的病例,结合相关文献,明确了DWS的眼部表现以及治疗预后,揭示视网膜神经纤维层厚度的动态监测可作为颅内压变化的重要线索,为临床管理与决策提供参考。
2. 已知与发现
· 在某些颅内病变情况下,腰椎穿刺测压无法准确反映真实的颅内压。
· 眼科检查如视网膜神经纤维层厚度进行性下降、视盘水肿及视网膜血管形态异常,可作为临床医生评估颅内压的有效手段。
· 疑似脑脊液分流不佳的患者,应建议及时转诊至神经外科,以免延误治疗时机。
3. 意义与改变
· 本病例表明,DWS患者颅内压监测存在复杂性。眼底表现可作为监测颅内压变化的重要窗口。鉴于眼底检查的无创性和可重复性,其在临床实践中具有不可替代的作用,为DWS患者的围术期颅内压管理提供了重要参考,有助于优化临床决策。
Dandy-Walker综合征(Dandy-Walker syndrome,DWS)是第四脑室的正中孔、侧孔先天性闭锁导致的先天性中枢神经系统畸形[1],常导致脑积水,协调神经肌肉的脑区异常和运动发育异常。继发脑积水引起的视神经压迫性病变是DWS的重要眼科并发症[2]。其他DWS相关眼部异常包括眼球震颤、斜视、角巩膜硬化、白内障、中央凹发育不全、黄斑水肿和视网膜血管灌注不足等[3-6]。本文介绍了一例DWS患儿术前及术后的眼部临床特征,以及术后视盘旁视网膜神经纤维层(Retinal Nerve Fibers Layer,RNFL)厚度的变化,提出应重视DWS患者的眼部表现,因其不仅可帮助诊断DWS,还在患者颅内压的随访与管理中有重要作用。
1 病例报告
患儿女,5岁 ,试管婴儿,孕28周出生,体重1.2 kg,主诉为“家长发现右眼视力下降2月余”,伴视物时头部歪斜,患儿同时有步态不稳,可站立,但斜向行走较为缓慢。
眼科检查:最佳矫正视力(Best Corrected Visual Acuity,BCVA)右眼:0.4,左眼:0.9,右眼屈光度为+1.75 DS/-1.75 DC×175°,左眼屈光度为+1.00 DS/-0.75DC×170°,双眼眼前段未见明显异常,双眼视盘高度水肿。头颅磁共振成像(magnetic resonance imaging,MRI):后颅窝、第四脑室扩大,幕上脑室明显扩张积水并轻度间质性脑水肿,小脑蚓部缺如、胼胝体及双侧小脑半球发育不良(图1A、B)。脑功能成像-脑脊液成像:中脑导水管脑脊液流速增高。诊断Dandy-Walker综合征,继发脑积水,脑水肿,右眼弱视。
治疗:患儿2023年9月1日在全身麻醉下行后颅窝蛛网膜囊肿部分切除术+硬膜修补+颅骨整复+神经内镜检查术。病理:囊肿壁送检增生显微组织呈囊壁样,伴少量炎症细胞浸润。术后第3天患儿体温高,脑脊液常规和细菌培养未见颅内感染迹象,考虑为呼吸道病毒感染所致。术后第9天因切口脑脊液漏,行腰大池置管引流术,术中腰椎穿刺术测压150 mmH2O(1 mmH2O=0.009 8 kPa,儿童正常范围40~95 mmH2O[7]),压颈实验提示脑脊液循环通畅,9 d后拔除引流管。
术后1个月,患儿行走尚可,BCVA右眼为手动/眼前,左眼为0.05,双眼眼前段未见明显异常,双眼视网膜血管迂曲,黄斑区星芒状渗出,视盘旁可见“paton”线。OCT提示双眼黄斑区外层视网膜连续性中断,层间可见高反射,RNFL增厚(图2A~F)。连续观察1个月双眼视力未见好转,眼底情况基本同前(图2G, H)。
术后2个月MRI(图1C, D):1)Dandy-Walker综合征治疗后复查,目前交通性脑积水,请结合临床;2)双侧桥小脑脚区、第四脑室异常信号灶,考虑少量积血可能性大,建议随访;3)后颅窝囊肿开窗术后,脑积水并轻度间质性脑水肿(较前稍好转),术区局部软组织稍肿胀(较前好转)。后患儿至神经外科再次行腰椎穿刺测颅内压150 mmH2O,结合患者的检查结果神经外科认为双眼视力下降并不考虑与颅内压升高相关。
术后5月患儿视力继续下降至双眼视力仅余光感,光定位不准,右眼视力下降较左眼下降明显,双侧瞳孔等大等圆,直径约3mm,直接对光反射迟钝,OCT显示双眼RNFL厚度持续变薄(图2I、J,图3),提示视神经的损害在进一步发展中。建议患儿再次就诊于神经外科。
在第一次颅窝蛛网膜囊肿部分切除术后半年余,患儿又进行了第二次手术:全身麻醉下行右侧脑室腹腔分流(ventriculoperitoneal shunt,VPS)+右侧脑室穿刺测压术,术中侧脑室穿刺测压大于330 mmH2O,明确压力过高后,置入可调压抗感染分流装置(强生,初压120 mmH2O)。
第2次手术后1月余,双眼视力提高至右眼:手动/10 cm,左眼:手动/30 cm,光定位准。双眼RNFL厚度未再进一步下降(图3)。双眼视盘色苍白,界清,视网膜血管迂曲,黄斑区星芒状渗出及paton线消失。双眼OCT提示黄斑区外层视网膜连续性中断较前好转,层间高反射减少(图4)。MRI结果示右侧侧脑室前⻆可见引流管;后颅窝增宽,脑室系统扩张较前减轻。
第2次手术后1月余,双眼视力提高至右眼:手动/10 cm,左眼:手动/30 cm,光定位准。双眼RNFL厚度未再进一步下降(图3)。双眼视盘色苍白,界清,视网膜血管迂曲,黄斑区星芒状渗出及paton线消失。双眼OCT提示黄斑区外层视网膜连续性中断较前好转,层间高反射减少(图4)。MRI结果示右侧侧脑室前⻆可见引流管;后颅窝增宽,脑室系统扩张较前减轻。
图1 Dandy-Walker综合征患儿术前及第一次术后MRI影像
Figure 1 Preoperative and postoperative MRI images of the patient with Dandy-Walker syndrome
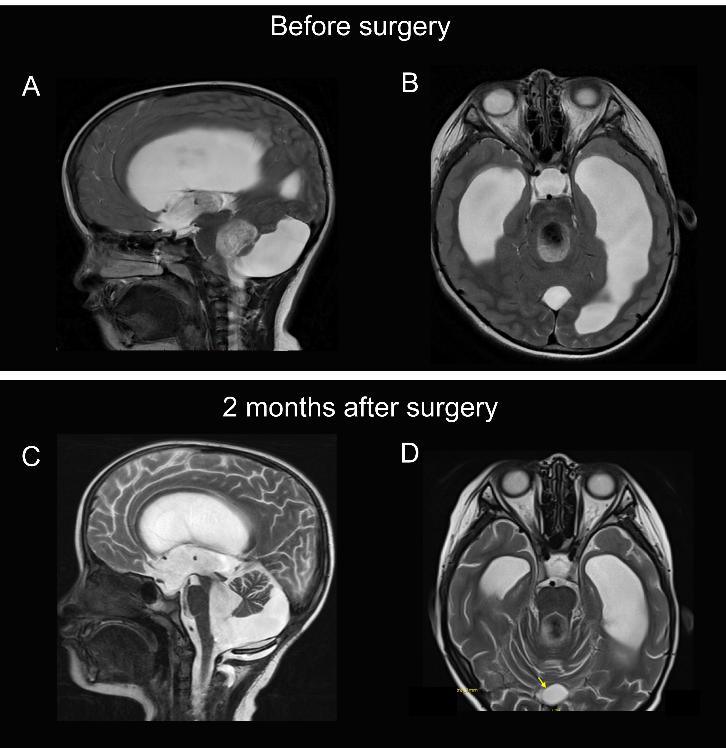
术前MRI,(A) T2序列矢状位:后颅窝、第四脑室扩大,幕上脑室明显扩张积水并轻度间质性脑水肿,小脑蚓部缺如;(B) T2序列水平位:胼胝体及双侧小脑半球发育不良,脑室扩张明显。后颅窝蛛网膜囊肿部分切除术后2个月MRI;(C) T2序列矢状位:后颅窝囊肿开窗术后,脑积水并轻度间质性脑水肿(较前稍好转),术区局部软组织稍肿胀(较前好转);(D) T2序列水平位:可见脑室扩张(较前好转)。
Before the first surgery, (A) Sagittal T2-weighted section: enlarged posterior cranial fossa and fourth ventricle, marked dilatation of the supratentorial ventricles with hydrocephalus and mild interstitial cerebral edema, with absence of cerebellar vermis; (B) Horizontal T2-weighted section: hypoplasia of the corpus callosum and bilateral cerebellar hemispheres, with significant ventricular dilatation. Two months after the partial resection of arachnoid cyst in posterior cranial fossa, (C) Sagittal T2-weighted section: after posterior cranial fossa cystotomy, with hydrocephalus and mild interstitial cerebral edema (slightly improved than before), and slight localized soft-tissue swelling at the operative area (improved than before); (D) Horizontal T2-weighted section: cerebral ventricle dilatation (improved than before).
图2 Dandy-Walker综合征患儿第一次手术1、2、5个月后眼部随访情况
Figure 2 Ocular manifestations follow-up of the patient with Dandy-Walker syndrome 1 month, 2 months, and 5 months after the first surgery
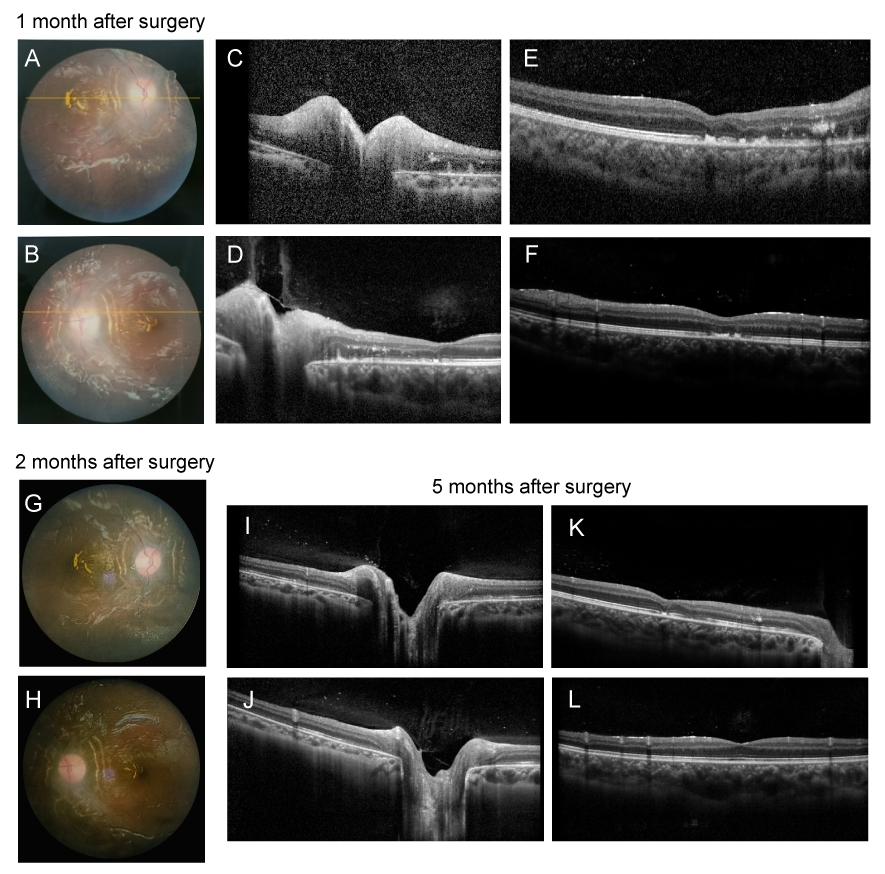
(A,B) Fundus photographs showed tortuous retinal vessels, stellate exudates in the macular region, and paton's lines in the retina near the optic disc in both eyes; (C, D) OCT showed papilledema in both eyes; (E,F) Disruption of the retinal continuity in the outer layer of the macular area, and high reflective points between retinal layers; (G, H) Fundus photographs of both eyes 2 months after the first surgery; (I-J) OCT showed less papilledema in both eyes than before; (K,L) Disruption of the retinal continuity in the outer layer of the macular area, and the interlayer hyperreflectivity was reduced compared with before.
图3 Dandy-Walker综合征患儿视网膜神经纤维层厚度随时间变化
Figure 3 RNFL thickness over time in the patient with Dandy-Walker syndrome
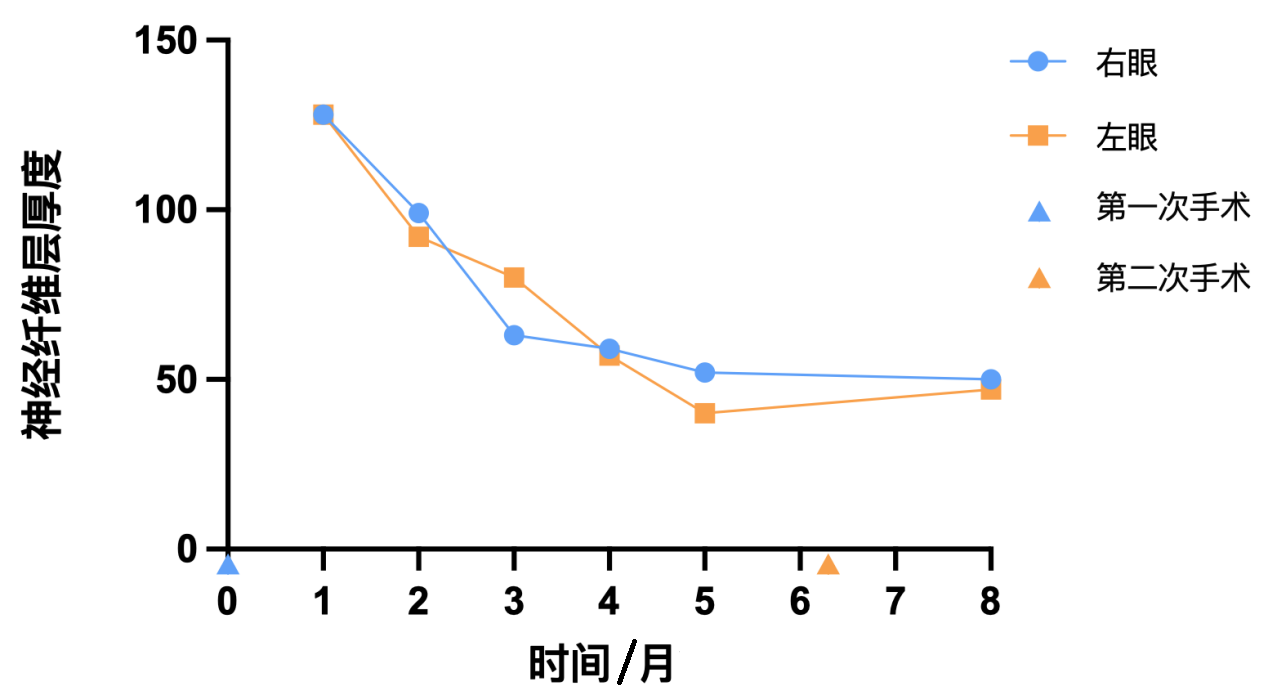
图4 Dandy-Walker综合征患儿右侧脑室腹腔分流术后1月余眼部随访情况
Figure 4 Ocular follow-up more than 1 month after right ventriculoperitoneal shunt in the patient with Dandy-Walker syndrome.
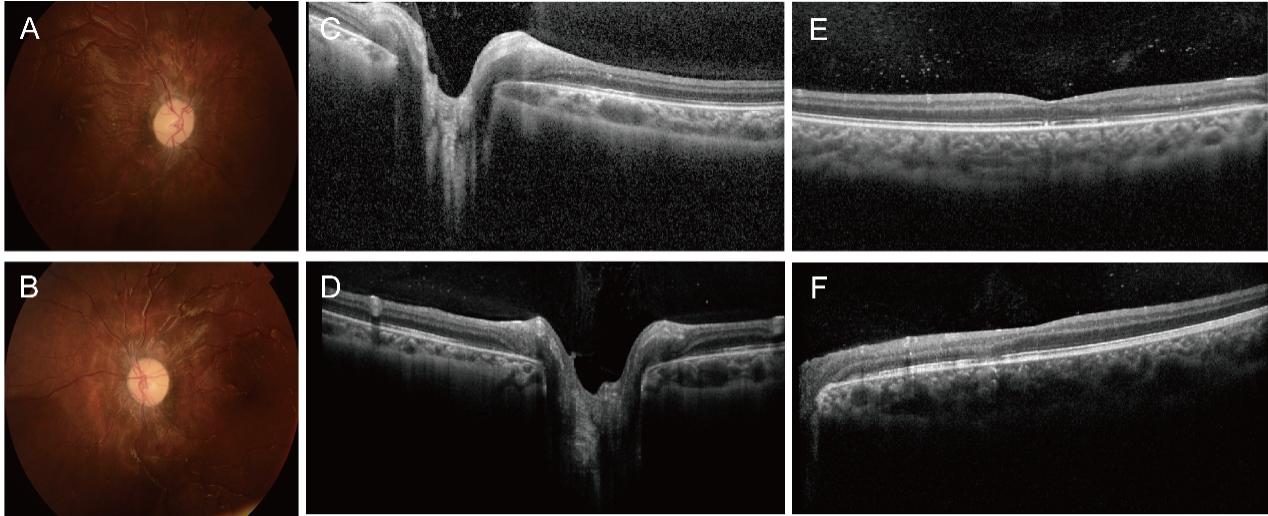
(A, B) Funduscopic photographs: the optic discs of both eyes with normal color and clear boundary. Retinal vessels were tortuous. Stellate exudates in the macula and paton's lines were absent; (C, D) OCT showed that the condition of papilledema in both eyes remains stable; (E, F) Disruption of the continuity of the macular outer layer in both eyes was improved than before, and the interlayer hyperreflectivity is reduced.
2 讨论
DWS是一种罕见的先天性小脑发育不全,常与胼胝体发育不全、脑积水和其他颅内畸形共存。 据调查,在活体新生儿中,DWS发病率为1/35 000~1/25 000[2],77%的DWS病例会出现脑积水[8]。由于先天性颅内畸形及脑积水,DWS患者可出现多种眼部并发症,包括视神经萎缩、黄斑水肿,以及眼球震颤、斜视、角巩膜硬化、白内障视网膜脱离、高度近视、视网膜无灌注区等,亦有文献报道可合并眼部发育不良如黄斑中心凹发育不良[2, 4, 5, 9]。本文报告了一例DWS畸形继发脑积水的患儿,虽然进行了手术,但是颅内压并未控制。后患儿经眼科随诊发现双眼视神经纤维的持续变薄,经侧脑室直接测压确认颅内高压的存在,并进一步行VPS,避免了进一步的损伤。
Dandy-Walker综合征的手术指征主要包括严重脑积水(颅内压升高>200 mmH2O[10])、颅内压升高症状(如头痛、呕吐、视力模糊等)、进行性神经功能恶化(如发育迟缓和共济失调)、保守治疗无效,以及影像学显示明显的脑结构异常(如后颅窝囊肿或第四脑室扩张)[8, 11]。目前针对DWS颅内高压的手术方式包有以下几种:1)后颅窝囊肿切除术,手术采用囊肿开窗,囊壁切除和将囊腔中的阻塞膜切除,同时处理粘连闭塞的出口[2]。本例患儿第一次手术即行颅窝囊肿切除术。2)脑脊液分流术:①VPS,较易放置,错位或移位的发生率相对较低,可用于DWS伴发脑积水的一线治疗和首选治疗。患儿第二次手术采取该手术方式后,虽然视力未见明显提升,但RNFL厚度趋于稳定。②囊肿腹腔分流术(cyst peritoneal shunt,CPS),将囊肿中囊液引流至腹腔,促进侧脑室中液体通过中脑导水管向下流动,缓解积水,同时引流囊腔和侧脑室积水[12]。③双分流术(VPS/CPS),在VPS的基础上同时进行CPS,双分流手术,目前应用尚不广泛[2]。3)神经内镜下第三脑室造瘘术(ETV),神经内镜损伤小,出血少,术后粘连风险低,在DWS中的治疗逐渐增多,但ETV需要特定的解剖条件,如三脑室有足够的解剖空间,蛛网膜下腔的大小等[13]。本例DWS患儿存在视物模糊、步态不稳的症状,且头颅影像学检查发现幕上脑室明显扩张积水,符合手术指征,神经外科就诊后行囊肿切除术治疗。
然而,术后患者的颅内压也有可能未得到有效控制。文献报道,后颅窝囊肿切除术手术失败率高达75%,病死率约10%[2],近年新的病例研究已显示病死率明显下降,但在导水管狭窄的情况下,囊肿膜切除不能同时治愈并存的脑积水,还需要后续的脑脊液分流术或ETV[14]。对1986—2002年间在印度治疗的72例Dandy-Walker综合征儿童的比较研究中,基于ETV的治疗成功率为76%,而基于分流的治疗总成功率为65%[14]。值得注意的是,Aaron等[13]发现CPS的成功率仅为50%,而VPS的成功率为81%,这表明选择CPS可能降低了总分流成功率。分流术失败的原因包括机械性梗阻,感染,分流阀故障以及假性囊肿等,分流失败的风险在植入分流管后的第一年最高[15-18]。因此,对患者进行术后随访,评估颅内压的控制情况,对于患者的预后十分重要。
值得注意的是,即使腰椎穿刺测压接近正常,也并不能排除颅内高压的情况,尤其是眼部情况持续进展时。 约14%~51%的儿童在分流失败后眼底检查仍可见视盘水肿[19]。然而也有颅内高压,却不合并视盘水肿的病例,这是因为视神经严重萎缩的情况下,没有足够数量的神经纤维水肿以表现为视乳头水肿。如文献报道一例7岁DWS的男孩在VPS后仍然头痛和视力逐渐下降。视力检查为双眼0.05,双眼视乳头未见水肿,仅表现为视盘苍白,边界清晰。CT显示分流管位置正确,腰椎穿刺测压在正常范围内。VPS探查发现分流管功能失常,修正手术后两个月,右眼视力改善至0.1,左眼手动视力[19]。这与本例患儿的诊疗过程有类似,在初次接受后颅窝囊肿切除术后,在一定程度上改善了脑脊液循环,所以行走步态好转;然而存在持续视神经损伤,RNFL厚度持续变薄,视力持续下降,说明颅内压在术后仍未得到足够控制。其原因可能是慢性蛛网膜下腔阻塞,导致神经发育不全和蛛网膜颗粒未成熟[20];此外,慢性阻塞还可能改变脑脊液循环系统的弹性和缓冲能力[21],这些原因阻碍脑脊液的正常循环和吸收。有研究发现在开颅手术完全解除颅内高压后6~8周,视盘水肿的眼底表现可消失[22]。
对于本例DWS患儿,虽然腰椎穿刺测压接近正常,即脊髓周围的脑脊液中压力正常,但是仍在进展的眼部表现提示在第四脑室以上区域存在颅内压增高。其原因可能是在许多病理状态下,颅内压的分布呈现出显著的不均匀性,腰椎穿刺及脑室内测压结果可能不一致[23],幕上与幕下区域之间的脑实质内压力可能形成显著的压力梯度[24]。检测部位离损伤部位越近,所获得的颅内压越高[7]。即使采用脑室内测压法,也仅在脑脊液能够在其所有自然池之间自由循环时,我们才能观察到颅内压的均匀分布。同时颅内压受多种因素影响,单次测量可能无法准确反映真实情况[25]。另外,在脑积水术后早期出现颅内压的升高,也并不一定是分流手术的失败,可能与蛛网膜下腔阻塞及缓冲能力下降有关。
由于部分患者腰椎穿刺测量颅内压可能存在偏差,眼科检查如OCT在这些患者的颅内压随访监测中可起到重要作用。有文献报道,在特发性高颅压患者(idiopathic intracranial hypertension, IIH)中,平均与各象限的视盘旁RNFL厚度均与患者腰穿测得的颅内压有相关性[26]。在对脑水肿术后患儿的随访中发现,视盘旁RNFL厚度与黄斑区厚度均较正常对照组有显著下降,提示OCT对于颅内压升高的诊断价值[27]。此外,在颅内压升高所致视盘水肿患者中,OCTA的浅层视网膜血管丛血流密度(SVC%)、深层视网膜血管丛血流密度(DVC%)较正常对照或无视盘水肿的颅内压升高患者均显著下降[28]。以上文献的研究结果均提示眼科检查特别是OCT检查可用于间接反映患者颅内压,相比于有创的腰椎穿刺测颅内压以及脑室内测压具有优势,为无创、简便、可重复的颅内压随访提供了手段。
结论
DWS继发脑积水进而导致颅内压升高,可能会对视神经产生压迫性损害,因此应该进行及时处理,如手术干预。颅内压的测量方法有多种,腰椎穿刺测压反映颅内压的前提是脑脊液在脑室系统和脊髓蛛网膜下腔之间必须保持自由连通。在某些颅内病变情况下,腰椎穿刺测压不能代表真实的颅内压。对于DWS患者脑室内测压更为准确,但临床上因其为有创操作,较少使用。眼科检查如RNFL厚度、视盘水肿、视网膜血管扩张和迂曲可作为反映颅内压的间接指标。其中视盘水肿程度不是最敏感指标,特别是在视神经萎缩的患者。相比之下,RNFL厚度是一个更为敏感的指标。颅内手术后RNFL的变化,需要根据病程病情具体分析,保持稳定可能是因为颅内压控制,而RNFL持续变薄则可能是颅内压未控制的持续压迫损害。术后需要定期监测RNFL厚度和视神经功能变化,若OCT检查RNFL厚度进行性下降和视功能持续受损,则可能提示仍存在颅内高压的情况。
眼科检查在DWS患者的术后颅内压管理具有重要作用。我们不能简单假设手术后颅内压一定会降低。定期的术后复查,必要的颅内压监测,对于及时保护和恢复患者视力极为关键。腰椎穿刺测颅内压、脑室内测压为有创检查,头颅MRI耗时较长且费用昂贵,与它们相比,眼科检查如OCT及较为简便、经济且无创,定期测量RNFL厚度或眼底检查对于及时发现颅内压增高具有显著的临床意义。这对于抢救患者的长期健康和视力恢复至关重要,疑似脑脊液分流不佳的儿童应建议其及时就诊于神经外科,早期的诊断和分流修复有助于视力恢复,避免失去抢救视力的时机。
声明
在论文撰写中无使用生成式人工智能。论文撰写中的所有内容均由作者独立完成,并对出版物的真实性和准确性承担全部责任。利益冲突
所有作者均声明不存在利益冲突。开放获取声明
本文适用于知识共享许可协议(Creative Commons),允许第三方用户按照署名(BY)-非商业性使用(NC)-禁止演绎(ND)(CC BY-NC-ND)的方式共享,即允许第三方对本刊发表的文章进行复制、发行、展览、表演、放映、广播或通过信息网络向公众传播,但在这些过程中必须保留作者署名、仅限于非商业性目的、不得进行演绎创作。
基金
暂无基金信息
参考文献
1. Correa G G, Amaral L F, Vedolin L M. Neuroimaging of Dandy-Walker malformation: New concepts [J]. Top Magn Reson Imaging, 2011, 22(6): 303-312. DOI: 10.1097/RMR.0b013e3182a2ca77.
2. Spennato P, Mirone G, Nastro A, et al. Hydrocephalus in Dandy–Walker malformation [J]. Childs Nerv Syst, 2011, 27(10): 1665-1681. DOI: 10.1007/s00381-011-1544-4.
3. March W F, Chalkley T H F. Sclerocornea Associated with Dandy-Walker Cyst [J]. Am J Ophthalmol, 1974, 78(1): 54-57. DOI: 10.1016/0002-9394(74)90009-9.
4. Rusu I, Gupta M P, Patel S N, et al. Retinal vascular nonperfusion in siblings with Dandy-Walker variant [J]. J Am Assoc Pediatr Ophthalmol Strabismus, 2016, 20(2): 174-177. DOI: 10.1016/j.jaapos.2015.11.010.
5. Ebrahimiadib N, Karkheiran S, Roohipoor R, et al. Foveal hypoplasia associated with Dandy-Walker syndrome [J]. Can J Ophthalmol, 2017, 52(4): e125-e127. DOI: 10.1016/j.jcjo.2017.01.020.
6. Nishant P, Aftab N, Raj A, et al. Adult-onset Dandy–Walker syndrome with atypical ocular manifestations [J]. Can J Ophthalmol, 2023, 58(4): e175-e177. DOI: 10.1016/j.jcjo.2023.01.008.
7. Smith M. Monitoring Intracranial Pressure in Traumatic Brain Injury [J]. Anesth Analg, 2008, 106(1): 240. DOI: 10.1213/01.ane.0000297296.52006.8e.
8. Marinov M, Gabrovsky S, Undjian S. The Dandy-Walker syndrome: Diagnostic and surgical considerations [J]. Br J Neurosurg, 1991, 5(5): 475-483. DOI: 10.3109/02688699108998476.
9. Lee H J,Phi J H,Kim S K,et al. Papilledema in children with hydrocephalus: incidence and associated factors[J]. J Neurosurg Pediatr,2017,19(6):627-631. DOI: 10.3171/2017.2.PEDS16561.
10. Steiner L A, Andrews P J D. Monitoring the injured brain: ICP and CBF [J]. Br J Anaesth, 2006, 97(1): 26-38. DOI: 10.1093/bja/ael110.
11. Fischer E G. Dandy-Walker syndrome: an evaluation of surgical treatment [J]. J Neurosurg, 1973, 39(5): 615-621. DOI: 10.3171/jns.1973.39.5.0615.
12. Domingo Z, Peter J. Midline Developmental Abnormalities of the Posterior Fossa: Correlation of Classification with Outcome [J]. Pediatr Neurosurg, 1996, 24(3): 111-118. DOI: 10.1159/000121026.
13. Yengo-Kahn A M, Wellons J C, Hankinson T C, et al. Treatment strategies for hydrocephalus related to Dandy-Walker syndrome: evaluating procedure selection and success within the Hydrocephalus Clinical Research Network [J]. J Neurosurg Pediatr, 2021, 28(1): 93-101. DOI: 10.3171/2020.11.PEDS20806.
14. Mohanty A, Biswas A, Satish S, et al. Treatment options for Dandy–Walker malformation [J]. J Neurosurg Pediatr, 2006, 105(5): 348-356. DOI: 10.3171/ped.2006.105.5.348.
15. Lenfeldt N, Koskinen L O D, Bergenheim A T, et al. CSF pressure assessed by lumbar puncture agrees with intracranial pressure [J]. Neurology, 2007, 68(2): 155-158. DOI: 10.1212/01.wnl.0000250270.54587.71.
16. Miranda P, Simal J A, Menor F, et al. Initial proximal obstruction of ventriculoperitoneal shunt in patients with preterm-related posthaemorrhagic hydrocephalus [J]. Pediatr Neurosurg, 2011, 47(2): 88-92. DOI: 10.1159/000329622.
17. Turhan T, Ersahin Y, Dinc M, et al. Cerebro-spinal fluid shunt revisions, importance of the symptoms and shunt structure [J]. Turk Neurosurg, 2011, 21(1): 66-73
18. Garber S T, Riva-Cambrin J, Bishop F S, et al. Comparing fourth ventricle shunt survival after placement via stereotactic transtentorial and suboccipital approaches [J]. J Neurosurg Pediatr, 2013, 11(6): 623-629. DOI: 10.3171/2013.3.PEDS12442.
19. Nazir S, O’Brien M, Qureshi N H, et al. Sensitivity of papilledema as a sign of shunt failure in children [J]. J AAPOS. DOI: 10.1016/j.jaapos.2008.08.003.
20. Massicotte E M, Del Bigio M R. Human arachnoid villi response to subarachnoid hemorrhage: possible relationship to chronic hydrocephalus [J]. J Neurosurg, 1999, 91(1): 80-84. DOI: 10.3171/jns.1999.91.1.0080.
21. Našel C, Gentzsch S, Heimberger K. Diffusion-weighted magnetic resonance imaging of cerebrospinal fluid in patients with and without communicating hydrocephalus [J]. Acta Radiol, 2007, 48(7): 768-773. DOI: 10.1016/j.jaapos.2008.08.003.
22. Walsh FB, Hoyt, W.F. Clinical Neuroophthalmology, Third Ed. Baltimore: Williams & Wilkins Co, 1969.
23. Wolfla C E,Luerssen T G,Bowman R M. Regional brain tissue pressure gradients created by expanding extradural temporal mass lesion[J]. J Neurosurg,1997,86(3):505-510. DOI: 10.3171/jns.1997.86.3.0505.
24. Rosenwasser R H, Kleiner L I, Krzeminski J P, et al. Intracranial pressure monitoring in the posterior fossa: a preliminary report [J]. J Neurosurg, 1989, 71(4): 503-505. DOI: 10.3171/jns.1989.71.4.0503.
25. Czosnyka M. Monitoring and interpretation of intracranial pressure [J]. J Neurol Neurosurg Psychiatry, 2004, 75(6): 813-821. DOI: 10.1136/jnnp.2003.033126.
26. Kaya Tutar N, Kale N. The Relationship between Lumbar Puncture Opening Pressure and Retinal Nerve Fiber Layer Thickness in the Diagnosis of Idiopathic Intracranial Hypertension: Is a Lumbar Puncture Always Necessary? [J]. The Neurologist, 2024, 29(2): 91-95. DOI: 10.1097/NRL.0000000000000528.
27. Taha Najim R, Mybeck L, Andersson S, et al. Thinner peripapillary retinal nerve fibre layer and macular retinal thickness in adolescents with surgically treated hydrocephalus in infancy [J]. Acta Ophthalmol (Copenh), 2022, 100(6): 673-681. DOI: 10.1111/aos.15162.
28. Kwapong W R, Cao L, Pan R, et al. Retinal microvascular and structural changes in intracranial hypertension patients correlate with intracranial pressure [J]. CNS Neurosci Ther, 2023, 29(12): 4093-4101. DOI: 10.1111/cns.14298.