眼科研究型医院专职研究护士管理实践
关键词
摘要
全文
文章亮点
1. 关键发现
· 本研究通过分析中山大学中山眼科中心2013-2024年专职临床研究护士(clinical research nurses, CRN)的管理实践,构建标准化临床研究护士(CRN)管理体系后,眼科临床研究项目质量评分从(67.5±17.2)分提升至(99.3±0.95)分(P<0.001),证实了该体系的有效性。2. 已知与发现
· CRN对提升研究规范性和数据质量具有关键作用已成为行业共识。但此前国内缺乏针对眼科领域CRN管理的系统性实践经验总结。· 本研究发现在临床研究中对CRN采用标准化的“准入-培训-模式”管理体系和实践模式,能够显著提升临床研究的质量。
3. 意义与改变
· 本研究为我国眼科临床研究护理的专业化发展提供了可复制的“标准化管理模板”,推动了CRN从“经验型执行者”向“专业型研究者”的角色转型。· 在实践层面,使临床研究项目质量大幅度提升;在行业层面,为其他专科研究型医院的CRN管理提供了参考范式,推动临床研究护理向专业化、规范化方向发展。
1 眼科临床研究护士的管理体系构建
1.1眼科临床研究护士的准入标准
1.2 眼科临床研究护士的分层培训体系
1.3 眼科临床研究护士的双轨管理模式
2 OCRN的核心职能与实施流程
2.1 核心职能
2.2 分阶段实施要点
团队培训与启动会:筹备并召开项目启动会,明确人员分工、授权及执行流程,组织药物临床试验质量管理规范(good clinical practice,GCP)、研究方案及标准操作规程(standard operating procedure,SOP)专项培训。
3 实施效果评价
表1 临床研究质控项目
Table 1 Quality Control Items for Clinical Research
|
不符合(0) |
基本符合(1) |
完全符合(2) |
不适用(NA) |
|
|
一、项目启动前的规范性评价 |
|
|
|
|
|
1. 临床研究通过机构科学性审查 |
|
|
|
|
|
2. 按要求保存伦理审查批件、年度/跟踪审查及意见函 |
|
|
|
|
|
3. 临床研究的有关信息按要求在首例参与者签署知情同意书前在国家医学研究登记备案信息系统完成上传并获得备案号 |
|
|
|
|
|
4. 干预性临床研究按相关要求在首例参与者签署知情同意书前在相应平台完成注册 |
|
|
|
|
|
5. 临床研究涉及人遗办审批或备案情况 需要在开展相关研究前完成 |
|
|
|
|
|
6. 临床研究经机构批准立项 |
|
|
|
|
|
7. 机构开展临床研究或参与多中心临床研究的 与立项部门或资助方签署任务书或合作协议 明确双方权利、义务及责任分担等 |
|
|
|
|
|
二、过程文件的规范性评价 |
|
|
|
|
|
8. 按要求保存伦理批准的方案 |
|
|
|
|
|
9. 按要求保存伦理批准的知情同意书 |
|
|
|
|
|
10. 主要研究者及团队开展临床研究取得法律法规要求的资质 具备相应能力 |
|
|
|
|
|
11. 按要求保存培训和启动记录 |
|
|
|
|
|
12. 按要求保存研究者分工授权表 |
|
|
|
|
|
13. 按要求保存临床研究投保单 |
|
|
|
|
|
14. 按要求保存方案变更、暂停、终止、结题的报告 |
|
|
|
|
|
15. 按要求保存方案违背报告 |
|
|
|
|
|
三、随访过程实施规范性评价 |
|
|
|
|
|
16. 所有参与者按要求签署知情同意书 |
|
|
|
|
|
17. 入组参与者符合入组标准 不符合排除标准 |
|
|
|
|
|
18. 按要求实施盲法和随机 |
|
|
|
|
|
19. 按要求保存参与者筛选/入组/随访的原始记录 |
|
|
|
|
|
20. 按方案要求实施临床研究 保护参与者安全和利益 |
|
|
|
|
|
21. CRF按要求填写 |
|
|
|
|
|
22. 按要求给予参与者补偿 |
|
|
|
|
|
23. 临床研究数据可查询、可溯源 |
|
|
|
|
|
24. 按要求处理、记录和报告不良事件及严重不良事件 |
|
|
|
|
|
25. 主要研究者定期开展自查 |
|
|
|
|
|
26. 保护参与者隐私 |
|
|
|
|
4 讨论与建议
5 结论
附图1 临床研究项目质量评分频数分布(OCRN:有OCRN参与;No-OCRN:无OCRN参与)
Figure 1 Frequency distribution of quality scores for clinical research projects (CRN: with Clinical Research Nurse involvement; No-CRN: without Clinical Research Nurse involvement)
附图A 项目启动前规范性评价
Figure A Compliance assessment prior to project initiation
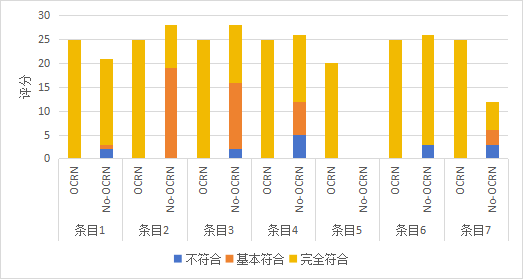
附图B 过程文件规范性评价
Figure B Compliance assessment of process documentation
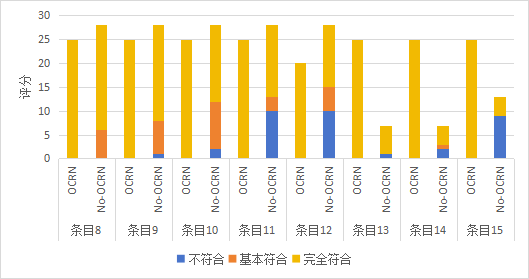
附图C随访过程实施规范性评价
Figure C Compliance assessment of follow-up process implementation
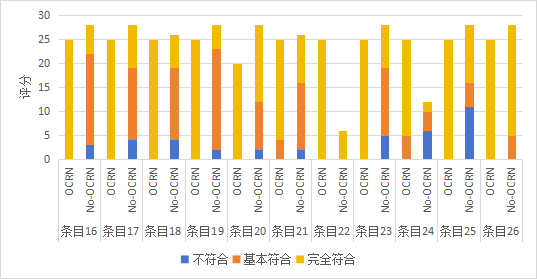
Frequencies lower than the total number of participants indicate the presence of non-application options.