激活TREK-TRAAK K2P对氧化损伤人RPE细胞吞噬功能的保护作用
关键词
摘要
全文
文章亮点
1.关键发现
2.已知与发现
• TREK-TRAAK K2P广泛表达于大脑及视网膜组织,具有维持细胞稳态的作用。• RPE细胞吞噬功能对维持感光细胞存活具有重要作用,慢性氧化损伤导致的RPE细胞吞噬功能障碍是年龄相关性黄斑变性(age related macular degeneration, AMD)重要的发病机制之一。
3.意义与改变
• 激活TREK-TRAAK K2P通道可以保护氧化损伤的人RPE细胞吞噬功能,有望成为AMD的潜在治疗靶点。年龄相关性黄斑变性(age related macular degeneration, AMD)是导致65岁以上老年人视力丧失的首要原因,预计到2024年,全球将有2.88亿AMD患者[1]。根据是否有新生血管形成分为干性AMD和湿性AMD,脉络膜新生血管(choroidal neovascularization, CNV)的形成及视网膜地图样萎缩是AMD的晚期事件,尽管可以通过抗血管内皮生长因子(vascular endothelial growth factor, VEGF)或基因治疗控制疾病进展,但病变对感光细胞的损害往往很难恢复[2-4]。视网膜色素上皮(retinal pigment epithelial, RPE)细胞的吞噬功能障碍是AMD的早期事件和重要因素[3]。早期纠正RPE细胞的吞噬功能损害有助于预防和延缓AMD的发生和发展。
双孔钾离子通道(two pore-domain potassium channels,K2P)广泛表达于中枢神经系统及视网膜组织,主要作用是介导钾离子外流,对维持细胞静息电位和稳态起重要作用,弱内向整流相关及花生四烯酸激活的弱内向整流相关双孔钾离子通道(tandem of pore domains in a weak inward rectifying related-tandem of pore domains in a weak inward rectifying related arachidonic acid activated two pore-domain potassium channels,TREK-TRAAK K2P)是其中的重要亚型,对花生四烯酸及机械牵拉敏感,可以被利鲁唑特异性激活[5-6]。笔者前期研究发现,激活TRAAK通道可以减轻人视网膜色素上皮细胞系(adult retinal pigment epithelial cell line-19,ARPE-19)细胞氧化损伤导致的细胞凋亡[7],但激活该通道对氧化损伤的RPE吞噬功能是否有影响还不明确。为进一步探索该通道去激活对氧化损伤RPE细胞吞噬功能的影响,本研究构建了人RPE细胞氧化损伤模型,通过TREK-TRAAK K2P通道的特异性激活剂利鲁唑激活通道开放,观察其对RPE细胞吞噬功能的影响,现将结果报道如下。
1 材料和方法
1.1 主要试剂和仪器
TREK-1、TREK-2、TRAAK单克隆抗体(以色列Alomone),利鲁唑(美国Sigma), 叔丁基过氧化氢(tert-butyl hydroperoxide, t-BHP)(美国MP),酶标仪(美国Bio-Tex),光学显微镜(德国Leica),免疫荧光显微镜(日本Olympus)。1.2 人RPE细胞的提取、鉴定及培养
本研究所用的人RPE细胞来自中山大学中山眼科中心眼科学国家重点实验室的馈赠。本实验所用的冻存人原代RPE细胞来源于3只眼球,均来自广东省眼库提供的意外死亡的年轻眼球捐献者,分别为13岁、28岁、43岁。本研究严格遵循《赫尔辛基宣言》,眼球组织的获取经捐献者家属知情同意后签署知情同意书,并通过中山大学中山眼科中心伦理委员会批准(伦理批件号:2021KYPJ196),RPE细胞从角膜移植术后残留的眼球组织提取。参考文献操作步骤提取人原代RPE细胞[8-9],并使用RPE细胞特异性RPE65抗体进行细胞免疫荧光鉴定,取3~5代的人RPE细胞用于后续实验。1.3 免疫荧光检测TREK-TRAAK K2P定位表达
以1×105/mL密度将RPE细胞接种于细胞玻片,4%多聚甲醛溶液固定,0.1%Trion溶液与1%牛血清白蛋白缓冲溶液(bovine serum albumin, BSA)混合液封闭打孔,实验组分别加50 μL︰1 200的TREK-1、TREK-2、TRAAK抗体,对照组加入等量磷酸盐缓冲液(phosphate buffered saline, PBS),分别加入1︰500的488荧光二抗,50 μL4',6-二脒基-2-苯基吲哚(4',6-diamidino-2-phenylindole, DAPI)溶液染细胞核,封片后用荧光显微镜拍照。1.4 氧化应激模型构建及细胞活力检测
实验分组:对照组、t-BHP组(200、300、500、1 000 μmol/L 6 h、300 μmol/L分别作用3、12、24 h),MTT法检测细胞存活率。简要操作步骤:将RPE细胞种于96孔板,每孔10 000个细胞,待细胞80%融合时,分别加入不同终浓度含t-BHP的完全培养基0.1 mL,对照组加入含等量溶质(蒸馏水)的完全培养基0.1 mL,37℃孵育预定时间;随后每孔加入20 μL MTT和180 μl无血清DMEM/F12培养液,避光孵育后吸出原液,再加入150 μL二甲基亚砜(dimethyl sulfoxide, DMSO),使结晶物充分溶解。在酶联免疫检测仪上490 nm波长读取OD值。细胞存活率=(实验组OD值-空白调零OD值)/(对照组OD值-空白调零OD值)×100%。1.5 感光细胞外节提取
参考文献提取新鲜猪眼感光细胞外节(photoreceptor outer segment, POS)[10]。简要步骤:新鲜猪眼以PBS溶液充分清洗,剪开眼球,小心分离取出视网膜组织,随后将视网膜剪成1 mm×1 mm的碎片,置于20 mmol/L Tris-HCL溶液中振荡1 min,1 500 r/min离心5 min,重复以上步骤吸取上清液后与Tris-HCL溶液1︰1混合,4℃下15 000 r/min离心45 min,收获的沉淀即猪眼POS。将提取的POS重悬于10 mmol/L钠-PBS,-80 ℃冻存备用。1.6 FITC-POS及荧光微球颗粒的制备
异硫氰酸荧光素(fluorescein Isothiocyanate, FITC)标记的感光细胞外节膜盘FITC-POS制备:冻存的POS室温下解冻,15 000 r/min离心30 min去上清,加入1 mg/mL FITC混合,室温孵育1 h,离心后去上清,再加入含血清的DMEM/F12溶液重悬,FITC密度调整为1×106/mL备用。荧光微球制备:取出1 mL荧光微球颗粒,PBS洗涤3次,去上清后以含血清的DMEM/F12溶液重悬,荧光微球密度调整为1×106/mL备用。1.7 RPE细胞吞噬实验
细胞分4组:对照组、模型组(200 μmol/L t-BHP 6 h)、模型加药组(100 μmol/L利鲁唑预培养6 h后加入200 μmol/L t-BHP培养6 h)、利鲁唑组(100 μmol/L利鲁唑12 h)。各组分别加入等量FITC-POS或荧光微球进行吞噬实验。简要步骤:密度为1×105 /mL 的RPE细胞悬液接种在玻璃片上,待60%融合时按上述分组干预。PBS洗涤后,分别加入浓度为2×106 /mL的FITC-POS或荧光微球颗粒,37 ℃孵育6 h后吸出培养基,PBS漂洗。特异性吞噬组以0.2%台盼蓝溶液浸10 min,4%多聚甲醛固定,各组加入0.8 μg/mL DAPI 10 min,封片后荧光显微镜拍摄(40倍镜下每块玻片随机选取3个视野拍照,图片计数或Image-Pro Plus 6.0软件分析荧光面积)。评价指标:细胞吞噬率=吞噬细胞数/视野下细胞总数×100%,非特异性吞噬指数=细胞吞噬颗粒总数/细胞总数,特异性吞噬指数为平均每个细胞吞噬FITC-POS面积。1.8 统计学分析
采用SPSS 25.0软件分析数据。符合正态分布的计数资料以(x±s)表达,计量资料多间比较使用单因素方差分析,组间两两比较采用LSD-t检验,率的比较采用χ2检验。P<0.05为差异有统计学意义。2 结果
2.1 TREK-TRAAK K2P表达于人RPE细胞质
TREK-1、TREK-2及TRAAK三种蛋白亚型在人RPE细胞上均有较高表达,免疫定位相似,主要为细胞质表达,在核周胞质荧光有增强(图1)。
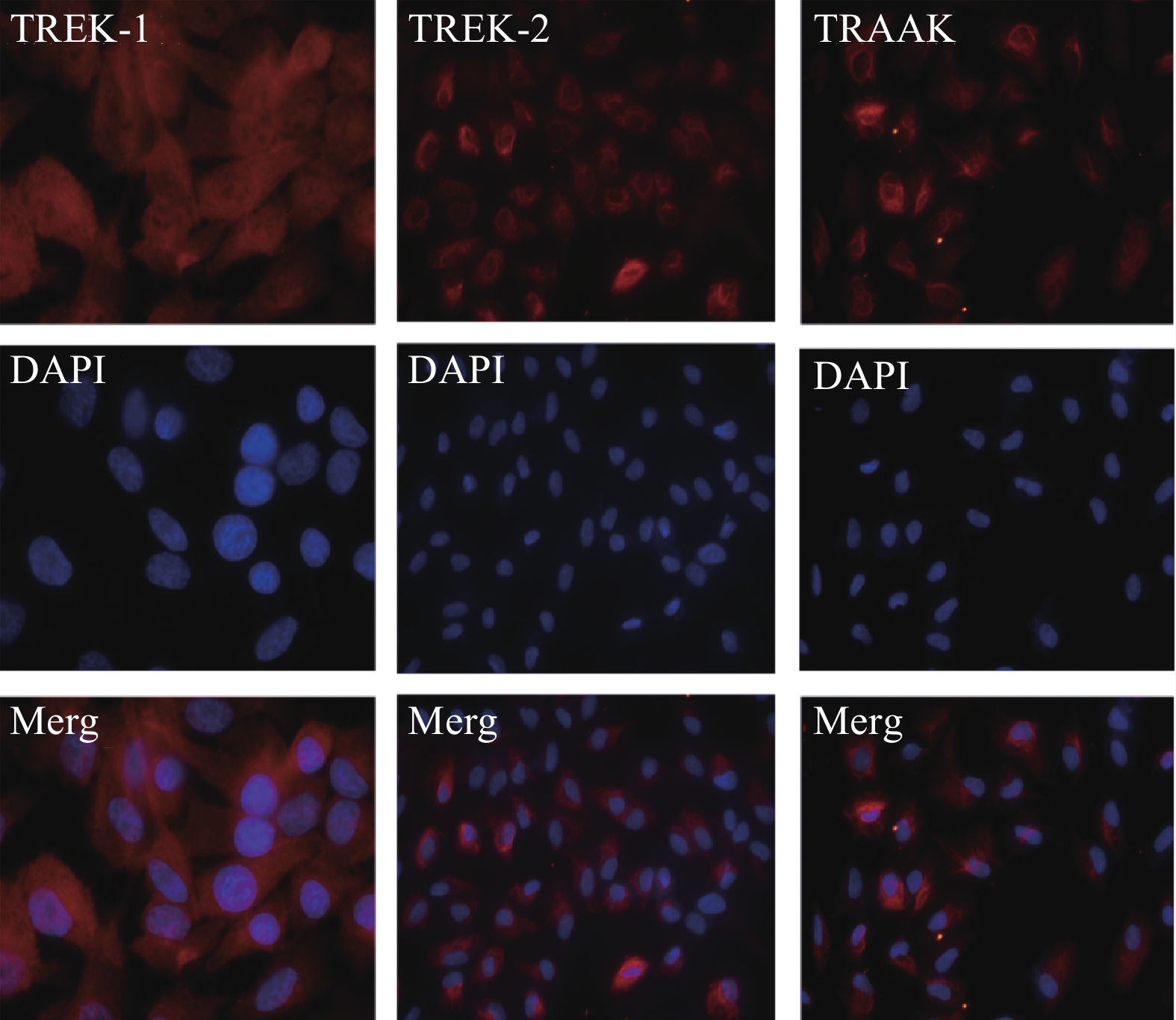
TREK-1(×100)、TREK-2及TRAAK蛋白(×40)在人RPE细胞质中均匀表达,围绕细胞核的荧光增强。
Immunofluorescence labeling demonstrates that TREK-1 (×100), TREK-2, and TRAAK proteins (×40) were distributed throughout the cytoplasm, with intensified fluorescence around the nucleus.
2.2 t-BHP氧化损伤模型的建立
正常对照组细胞存活率为100%,200 μmol/L t-BHP干预6 h细胞存活率与对照组比较差异无统计学意义(P>0.05),500 μmol/L t-BHP 干预6 h细胞平均存活率仅为28.1%,SPSS软件Probit回归分析计算得到t-BHP干预6 h细胞半数致死浓度为400 μmol/L。随着t-BHP浓度的增加或作用时间的延长,细胞的存活率进一步下降,300 μmol/L t-BHP作用24 h,细胞基本死亡(表1)。为模拟慢性氧化损伤对RPE细胞功能影响,最终选择200 μmol/L t-BHP干预6 h作为后续实验的体外细胞造模方法。|
组别 |
细胞存活率/% |
|
正常对照组 |
100 |
|
200 μmol t-BHP 6 h组 |
95.7±6.8 |
|
300 μmol t-BHP 6 h组 |
67.5±4.0 |
|
500 μmol t-BHP 6 h组 |
28.1±3.9 |
|
1 000 μmol t-BHP 6 h组 |
22.7±2.7 |
|
300 μmol t-BHP 3 h组 |
97.5±1.7 |
|
300 μmol t-BHP 12 h组 |
10.7±3.0 |
|
300 μmol t-BHP 24 h组 |
1.68±0.1 |
2.3 人RPE细胞对POS和荧光微球的吞噬
100倍荧光显微镜下观察用于吞噬实验的经FITC标记的POS颗粒在488 nm荧光下显示绿光,表现为大小均匀一致的块状物质(图2A),荧光标记的微球颗粒表现为均匀的圆形绿色颗粒(图2C)。经过6 h的共同孵育,人RPE细胞吞噬了FITC-POS和荧光微球,分布在细胞质内,细胞核边缘(图2B、D)。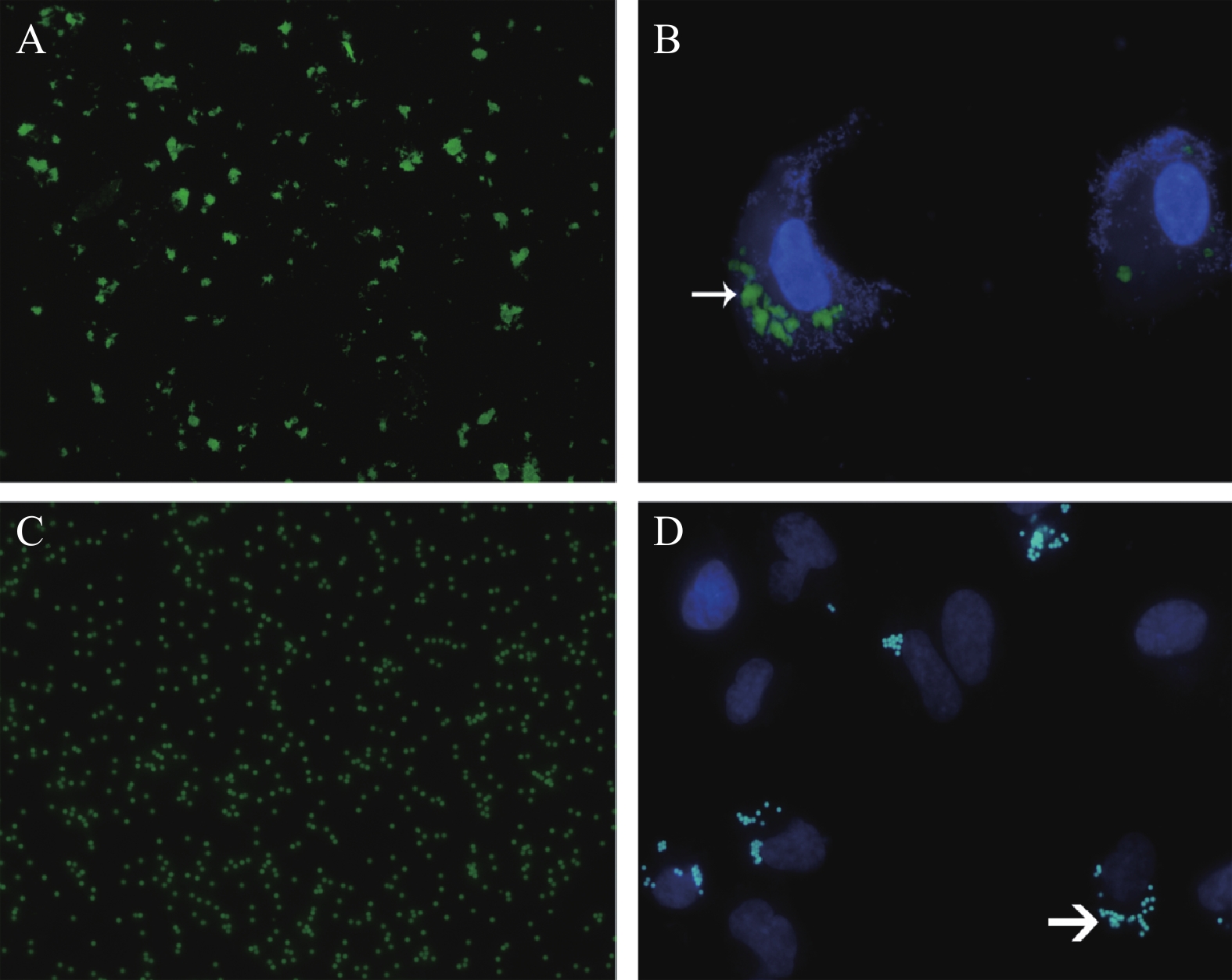
(A) 经FITC标记稀释的猪视网膜外节膜盘(FITC-POS);(B)RPE细胞与FITC-POS共同孵育6 h,RPE细胞吞噬的POS(白色细箭头);(C)经稀释的荧光微球颗粒;(D)RPE细胞与FITC-POS共同孵育6 h,RPE细胞吞噬的荧光微球颗粒(白色粗箭头)。
2.4 利鲁唑激活TREK-TRAAK K2P可改善氧化损伤的人RPE细胞的特异性吞噬功能
如图3所示,荧光显微镜下拍照,Image-Pro Plus 6.0软件分析绿色荧光面积指数(即吞噬的FITC-POS特异性吞噬指数),对照组、利鲁唑组、t-BHP组、利鲁唑加t-BHP组的吞噬指数分别为671±47、675±65、155±26、450±58。单因素方差分析进行组间比较,t-BHP组吞噬指数低于其他各组,与各组之间比较差异均有统计学意义(P<0.001),而利鲁唑组吞噬指数稍高于对照组,但差异无统计学意义(P>0.05)。各组的特异性吞噬率:对照组(96.0±1.0)%、利鲁唑组(89.7±2.1)%、t-BHP组(80.7±8.3)%、利鲁唑加t-BHP组(81.0±2.6)%,t-BHP组吞噬率低于其他各组,但两两比较差异无统计学意义(P>0.05),正常组吞噬率大于利鲁唑组,但差异亦无统计学意义(P>0.05)。
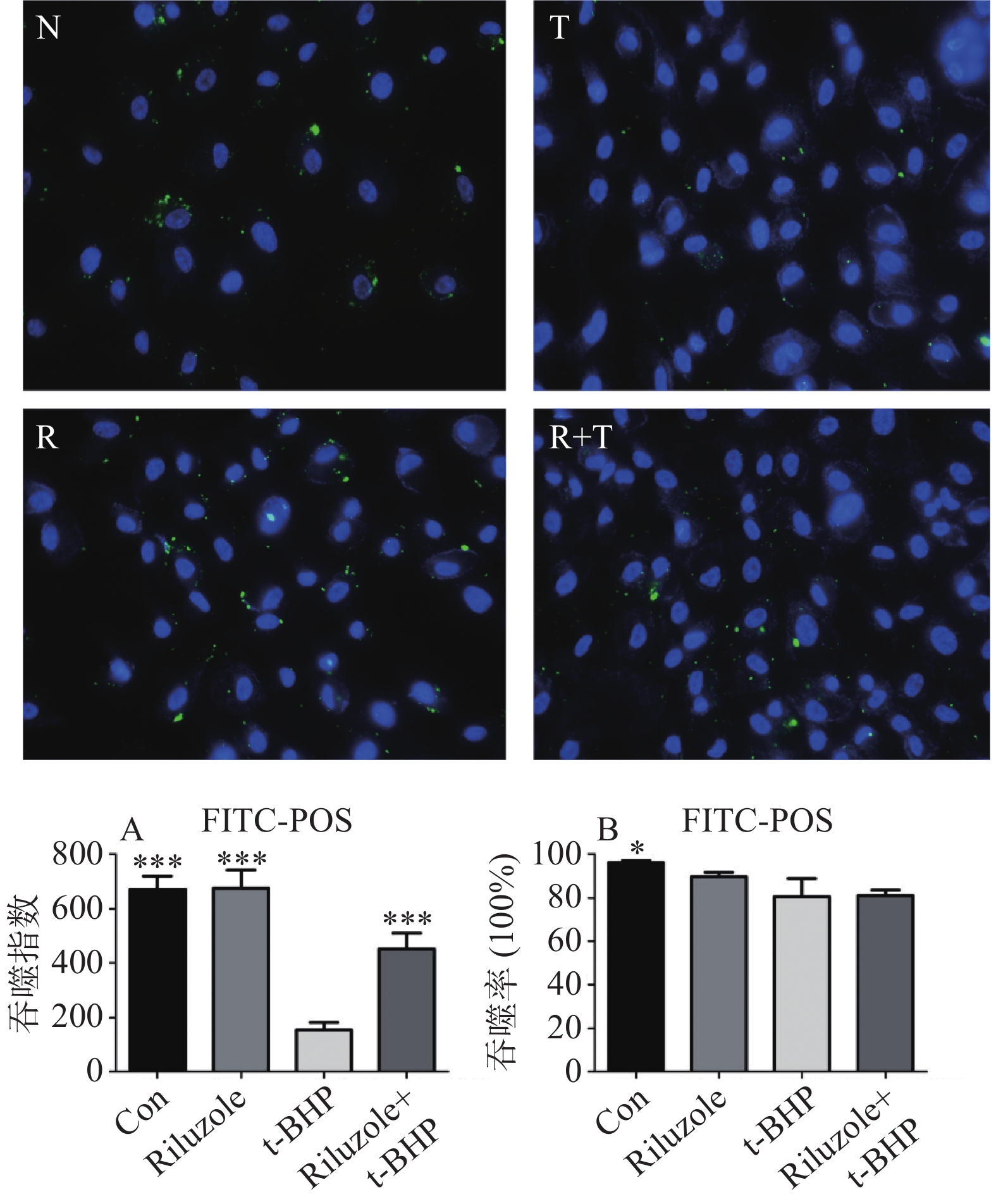
N:对照组,R:利鲁唑组,T:t-BHP组,R+T:利鲁唑加t-BHP组;各组经6 h的吞噬,可见大部分RPE细胞内有FITC-POS荧光。(A) 吞噬指数:t-BHP组显著低于其他各组(P<0.001),利鲁唑加t-BHP组显著高于t-BHP组(P<0.001);(B) 吞噬指数:仅对照组高于t-BHP模型组(P<0.05),其他组间差异无统计学意义。*: P<0.05,***: P<0.001。
2.5 利鲁唑激活TREK-TRAAK K2P可保护氧化损伤的人RPE细胞的非特异性吞噬功能
如图4所示,荧光显微镜下拍照,各组的吞噬指数(即平均每个细胞吞噬的荧光微球颗粒数):正常组(11.4±0.9)、t-BHP组(5.6±0.2)、利鲁唑加t-BHP组(9.8±1.3)、利鲁唑组(12.6±1.6)。单因素方差分析进行各组间比较,t-BHP组吞噬指数低于其他各组,与各组之间差异均有统计学意义(P<0.001),而利鲁唑组吞噬指数稍高于对照组,但差异无统计学意义(P>0.05)。各组的吞噬率:正常组(92.0±5.7)%、利鲁唑组(95.5±6.1)%、t-BHP组(83.5±5.3)%、利鲁唑加t-BHP组(88.8±3.3)%,单因素方差分析进行各组间比较,t-BHP组吞噬率均数低于利鲁唑加t-BHP组,但差异无统计学意义(P>0.05),两两比较,仅利鲁唑组吞噬率高于t-BHP组,差异有统计学意义(P<0.05)。
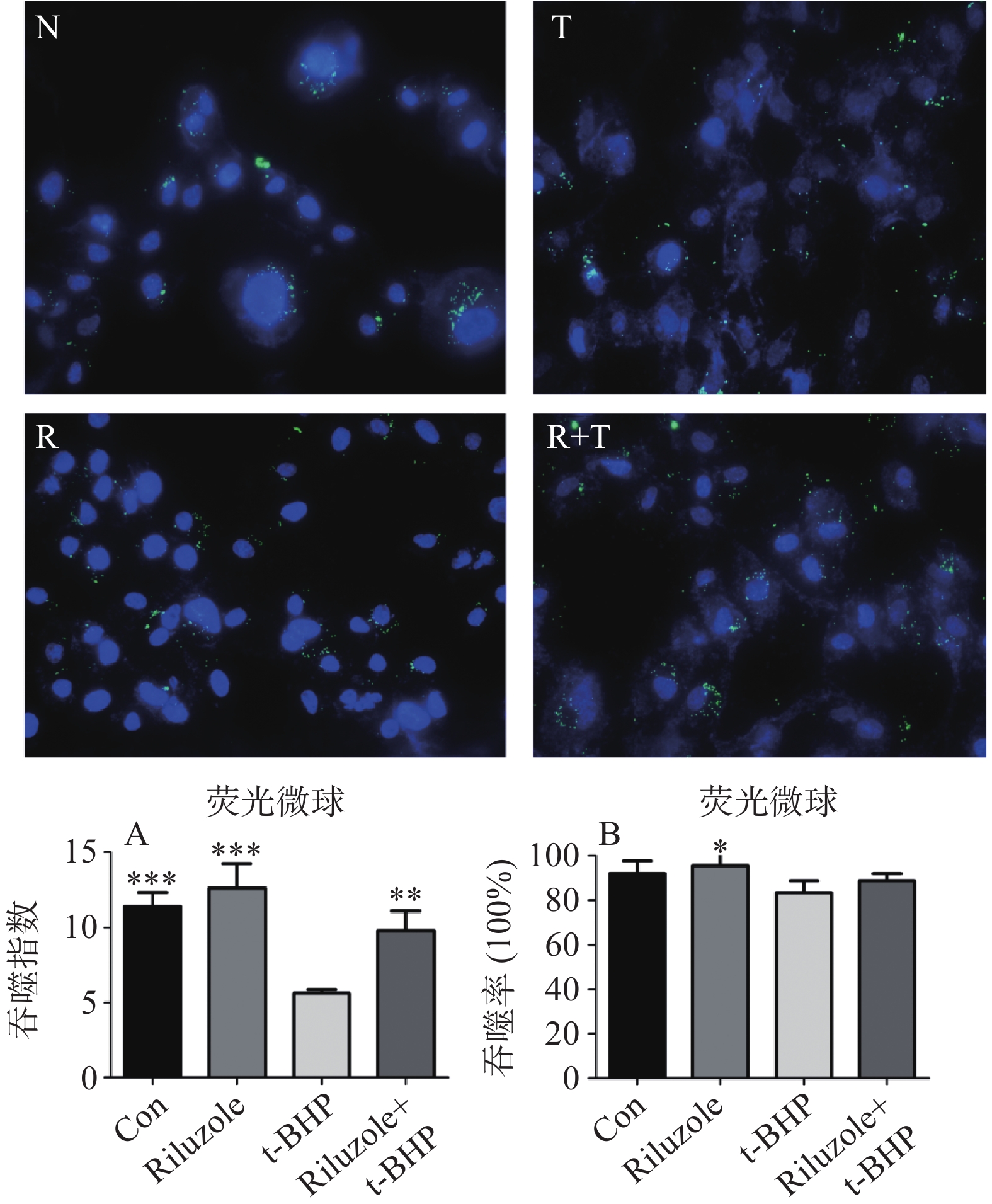
N:对照组,R:利鲁唑组,T:t-BHP组,R+T:利鲁唑加t-BHP组;各组经6 h的吞噬,可见大部分RPE细胞内有荧光微球颗粒。(A) 非特异性吞噬指数:t-BHP组显著低于其他组;(B) 非特异性吞噬率:利鲁唑组稍高于t-BHP组,其他组间差异无统计学意义。*: P<0.05,**: P<0.01,***: P<0.001。
3 讨论
AMD是一种光感受器细胞-RPE细胞-Bruch's膜-脉络膜毛细血管复合体的退行性病变,是65岁以上老年人不可逆盲的首要原因[3]。其最终的病理转归是各类视网膜细胞的凋亡或者坏死,机制复杂[1-2]。氧化应激导致的RPE细胞损伤被认为是AMD的重要发病因素[4]。AMD患者视网膜的玻璃膜疣成分中存在大量氧化的脂质和蛋白质[11],而在AMD患者的RPE细胞中抗氧化物酶的表达和相关的受体大量增加[12],这些都直接或间接表明氧化损伤参与了AMD的发生和发展。本研究使用不同浓度梯度的t-BHP干预不同时间体外诱导RPE细胞氧化损伤,结果和既往文献报道一致,细胞存活率呈现时间和剂量依赖性[13]。视网膜处于高代谢状态,大量耗氧过程中产生大量活性氧并产生代谢产物。在AMD早期,主要病理改变为RPE细胞和Bruch's膜间出现玻璃膜疣,黄斑区色素紊乱,随着病情的进展,玻璃膜疣增多,又进一步导致RPE细胞脱离、凋亡、坏死,在这个过程中坏死的RPE细胞可进一步募集各种炎症反应因子参与其中,分泌VEGF增加,RPE细胞功能障碍,特别是吞噬功能障碍进一步继发感光细胞凋亡坏死、脉络膜萎缩,出现典型的地图样萎缩,少部分最终可发展为CNV[2,14-15]。
TREK-TRAAKK2P家族是新近发现的一个钾离子通道亚家族,包括TREK-1、TREK-2和TRAAK三个亚型成员,在中枢神经系统高表达,主要维持细胞的背景电流,参与细胞正常生理功能维持和病理状态调节[16-17]。既往也有研究发现该家族通道蛋白在müller细胞及小胶质细胞上表达[18-19]。本研究发现TREK-1、TREK-2和TRAAK蛋白在人RPE细胞均有明显表达。研究发现,TREK-TRAAK K2P参与了细胞凋亡的调控,在凋亡早期介导细胞内钾离子浓度改变以维持细胞内外环境的稳态,拮抗细胞凋亡[20]。研究显示,中国仓鼠卵巢细胞过表达TREK-1能够拮抗H2O2氧化损伤所致的细胞凋亡,表现出明显的细胞保护作用,但具体的机制尚不清楚。在我们的前期研究中也发现TRAAK与视网膜的发育密切相关,并且TREK-TRAAK K2P激动剂能够减少氧化损伤的RPE早期凋亡,推测可能和TRAAK通道开放维持细胞稳态相关及影响凋亡相关信号通路有关[21]。
RPE细胞的吞噬作用对维持视网膜稳态具有重要意义。RPE细胞除对感光细胞外节膜盘的特异性吞噬作用外还具有吞噬细胞碎片、酵母菌、色素颗粒、乳胶微球的非特异性吞噬作用[9,22]。其中,RPE细胞吞噬功能和感光细胞的外节更新密切相关,RPE吞噬功能障碍将导致视网膜变性疾病(包括AMD)的发生。研究表明,感光细胞的外节膜盘每天约更新10%,脱落的POS直接被与之相邻的RPE细胞吞噬,吞噬过程包括识别、结合、内吞、消化等步骤,最终被RPE细胞消除,部分不能完全消化的将被沉积下来形成脂褐质或被排出细胞外,成为玻璃膜疣的一部分[23]。本研究中,200 μmol/L干预6 h非致死量的t-BHP诱导人RPE细胞氧化损伤后,与对照组相比,细胞对POS的吞噬量下降了75%,对荧光乳胶微球的吞噬率下降了50%。该结果说明,氧化损伤抑制了RPE细胞的吞噬功能,且对特异性吞噬功能的抑制明显强于非特异性吞噬功能。由于吞噬过程是一个大量酶活化,信号传导和肌球蛋白运动的过程,所以消耗大量的ATP。一方面,氧化损伤可以导致RPE细胞膜表面吞噬相关受体的表达下降,影响结合、内吞等过程[24];另一方面,氧化损伤影响RPE细胞线粒体功能,干扰能量代谢,从而使得吞噬这个大量消耗能量的过程受阻[25]。在本研究中,利鲁唑作用下RPE细胞吞噬功能并没有明显变化,但利鲁唑预处理却能明显地提高氧化应激损伤RPE细胞的吞噬功能,提示利鲁唑并没有上调吞噬相关的蛋白分子的表达,可能的机制是TREK-TRAAK K2P通道的开放调节了细胞内外的钾离子平衡,维持了细胞的稳态,是否还与进一步减少了氧化损伤所致的吞噬相关蛋白表达下降有关,具体的机制有待进一步研究。
本研究的局限性:1)主要是体外实验,还需要体内实验进一步验证;2)对TREK-TRAAK K2P通道开放保护氧化损伤的人RPE细胞吞噬功能的具体分子机制需要进一步深入研究。
综上所述,TREK-TRAAK K2P通道的激活不但可以维持氧化损伤导致的RPE细胞存活,而且可以保护RPE细胞吞噬功能,为其作为AMD治疗的潜在靶点提供了科学依据。