累及双眼持续进展的Stevens-Johnson综合征1例
阅读量:3126
DOI:doi: 10.3978/ j.issn.1000-4432.2017.12.05
发布日期:2024-12-05
作者:
范薇 ,钟敬祥
展开更多 '%20fill='white'%20fill-opacity='0.01'/%3e%3cmask%20id='mask0_3477_29692'%20style='mask-type:luminance'%20maskUnits='userSpaceOnUse'%20x='0'%20y='0'%20width='16'%20height='16'%3e%3crect%20id='&%23232;&%23146;&%23153;&%23231;&%23137;&%23136;_2'%20x='16'%20width='16'%20height='16'%20transform='rotate(90%2016%200)'%20fill='white'/%3e%3c/mask%3e%3cg%20mask='url(%23mask0_3477_29692)'%3e%3cpath%20id='&%23232;&%23183;&%23175;&%23229;&%23190;&%23132;'%20d='M14%205L8%2011L2%205'%20stroke='%23333333'%20stroke-width='1.5'%20stroke-linecap='round'%20stroke-linejoin='round'/%3e%3c/g%3e%3c/g%3e%3c/svg%3e)
关键词
Stevens-Johnson综合征
眼部并发症
持续进展
摘要
一名36岁的女性于16年前因静脉滴注“青霉素”引发Stevens-Johnson综合征,出现皮肤剥脱,口、鼻腔黏膜破损出血,双眼红肿伴分泌物增多等症状,当时经过治疗症状基本缓解。数月后开始反复出现眼部不适,2010年患者的视力明显下降,眼部疼痛加重,伴畏光流泪。至2016年入暨南大学附属第一医院时双眼最佳矫正视力仅0.1(右眼)、光感(左眼),双眼角膜混浊,新生血管长入,甚至出现睑球粘连。80%的SJS患者可伴有眼部并发症,经过治疗症状缓解后,眼部病变仍可能继续进展,最终导致视力障碍甚至更严重的后遗症。因此患者病情稳定后仍须随诊,密切关注眼部、皮肤及黏膜的变化情况。
全文
Stevens-Johnson综合征(Stevens-Johnson
syndrome,SJS)是一种累及皮肤和黏膜的眼皮肤黏膜综合征,年发病率为每百万人口1.2~6/100万[1],是
一种严重且潜在致命的疾病。SJS的发病与药物、感染或恶性肿瘤等多种因素相关,其发病急、病情重,眼部常受累。暨南大学附属第一医院于2016年8月接诊了1例眼部并发症持续进展的SJS患者,其临床资料报告如下。
1 病例资料
患者,女性,36岁,于2001年在当地医院静脉滴注“青霉素”后出现休克,次日面部、颈部出现红斑丘疹,逐渐形成水疱并发生局部皮肤剥脱,数日后出现口腔、鼻腔黏膜轻度破损出血,
双眼轻度红肿、分泌物增多,当时眼部症状较轻未予重视,诊断为“过敏性休克、剥脱性皮炎(药物过敏性皮炎)”,患者经抢救后予抗过敏、抗感染等治疗(具体治疗不详),皮肤损伤有所控制,
眼部症状基本缓解,病情稳定出院。患者出院后数月开始反复出现双眼红、痛,分泌物增多,视力逐渐下降,伴鼻塞、流脓涕,曾于多个医院就诊,用药缓解后未继续治疗,至2010年患者视力明显下降,眼部症状加重。2013年患者曾在北京某医院诊断为“干眼症”,予以罗红霉素、红霉素眼膏及人工泪液等治疗(病历资料缺如)。近5年来患者眼部症状反复发作并逐渐加重,视力进行性下降,遂因“双眼肿痛、畏光流泪,分泌物多,伴视力下降16年,加重5年余”入住暨南大学附属第一医院。体格检查:面部及颈部可见皮损遗留的色素瘢痕(图1),脊柱四肢无畸形。各关节活动正常,无关节红肿、强直及杵状指。眼
部检查:0.1(右眼),光感(左眼),光定位准确;
眼压:右眼12 mmHg(1 mmHg=0.133 kPa),左眼6 mmHg。右眼上睑轻度内翻、红肿,眼睑皮肤粗糙,睑缘变钝,结膜囊较多分泌物,结膜混合性充血(+),颞上1/2角膜片状白色混浊,新生血管由外眦部长入(图2A),前房深度正常,房水清,瞳孔圆,直径约3 mm,对光反应存在,眼内结构窥不清;左眼上睑内翻倒睫,眼睑皮肤粗糙,睑缘变钝,内外眦处上下睑结膜粘连,结膜混合性充血(++),角膜混浊,大量新生血管翳长入(图2B),前房及眼内结构无法窥见。双眼角膜荧光染色阳性(图3A,3B),实验室检查:WBC
6.06×109
/L,RBC 4.5×1012
/L,PLT 211×109
/L,HGB 134 g/L,淋巴细胞百分比:28.2%,嗜酸性粒细胞百分比1.3%,ESR 7 mm/h,超敏C反应蛋白 2.37 mg/L(偏高,中度风险1.0~3.0),循环免疫复合物浊度CIC 118(偏高,参考值80~110),
抗SSA(−),抗SSB(−),HLA-B27阴性。胸部CT:双肺见多个条片状淡薄高密模糊影及散在磨玻璃
影,双上肺尖段见少量条索影,考虑间质性肺炎并肺气肿(图4);最终诊断为“ Stevens-Johnson综
合征”,全身予白芍总苷胶囊(免疫抑制剂)、阿法骨化醇软胶囊(维生素D补充药)、克拉霉素(大
环内酯类抗生素)、乙酰半胱氨酸片(祛痰药)进行免疫调节及对症治疗,局部予以氟米龙、新泪然及唯地息滴眼治疗。本病例报告患者已签署知情同意书。
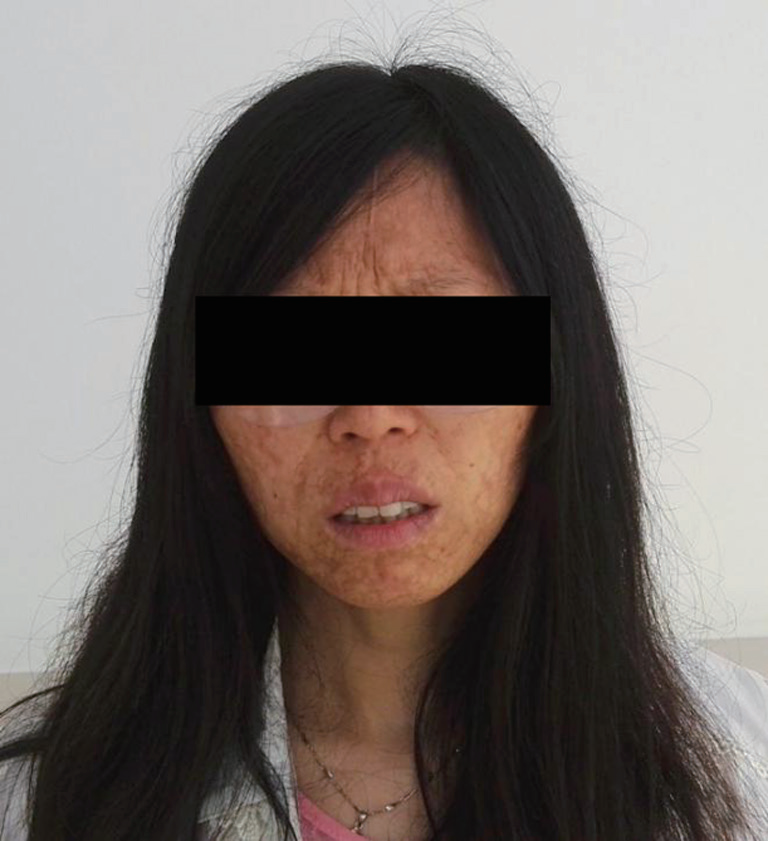
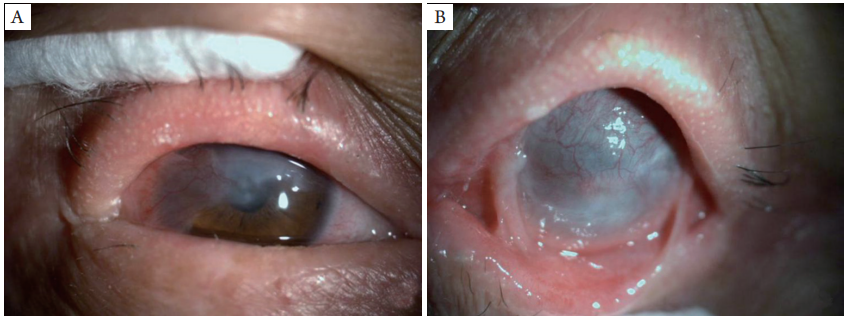
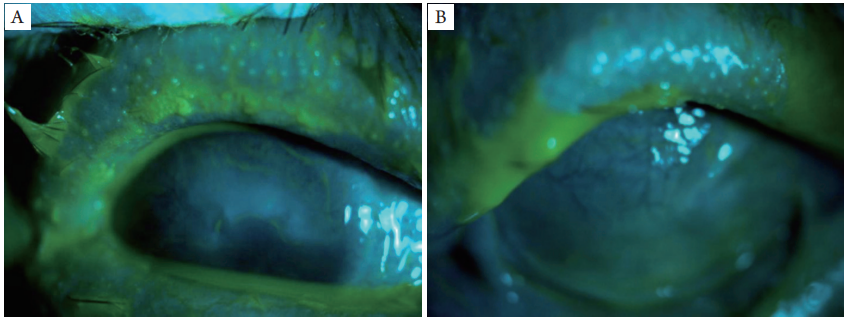
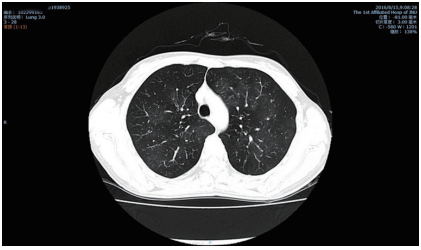

图1 患者面部及颈部皮肤遗留色素瘢痕
Figure 1 The photograph revealing pigment scars in the face
and neck skin of the patient

图2 双眼眼前段照相
Figure 2 Anterior segment eye photograph
Figure 2 Anterior segment eye photograph
(A)右眼上睑轻度内翻、红肿,眼睑皮肤粗糙,睑缘变钝,结膜混合性充血(+),颞上1/2角膜片状白色混浊,新生血管由
外眦部长入;(B)左眼上睑内翻倒睫,眼睑皮肤粗糙,睑缘变钝,内外眦处上下睑结膜粘连,结膜混合性充血(++),角膜
混浊, 大量新生血管翳长入。
(A)Right upper eyelid mild varus, swelling, eyelid skin roughness, eyelid margin dull, conjunctival hyperemia (+), superior temporal
1/2 white opacity, neovascularization; (B) Leff eye upper eyelid varus, trichiasis, eyelid skin rough, eyelid margin dull, upper and lower
conjunctiva adhesion, conjunctival hyperemia (++), corneal opacity, a large number of neovascularization.

图3 双眼角膜荧光素染色
Figure 3 Corneal fluorescein staining
(A)右眼角膜荧光染色(+);(B)左眼角膜荧光染色(+)。
(A) Right corneal ffuorescein staining (+); (B) Leff corneal ffuorescein staining (+).

图4 双肺见多个条片状淡薄高密模糊影及散在磨玻璃影
Figure 4 Multiple band-shaped thin and high-density shadow
and scattered ground glass in bilateral lungs
2 讨论
SJS是一种由免疫复合物介导的眼–皮肤–黏膜疾病,属于IV-c型迟发性超敏反应[2]。SJS的发病与多种因素有关,如全身或局部用药、感染和恶性肿瘤等。虽然有报道由病毒感染(主要是单纯疱疹病毒)或支原体感染引发的病例,但超过90%的病例是由药物诱导,主要包括抗生素(磺胺类和β-内酰胺类等)、非甾体抗炎药、解热镇痛药以及抗癫痫药(主要是苯妥英和卡马西平)[1,3]。本例患者发病前有青霉素注射史,用药后出现皮肤、黏膜病变及相应的眼部症状,表明该患者的发病与β-内酰胺类药物相关。
SJS病理生理机制尚未完全明确,已有证据[1,4]显示其与机体对反应性药物代谢中间产物的解毒能力受损有关,此类产物与某些机体组织形成抗原复合物导致免疫反应,启动本病发生。最近,也有研究[5]证明一些HLA主要组织相容性复合体等位基因与发生该病有关联。SJS组织病理学特征主要是角质形成细胞凋亡而导致广泛的表皮坏死,CD8细胞在该过程中充当介体,目前公认的两条导致凋亡的途径:Fas(CD95,角质形成细胞膜受体)与其FasL配体(CD95L)的结合以及穿孔素和粒酶B的释放[6]。
SJS病理生理机制尚未完全明确,已有证据[1,4]显示其与机体对反应性药物代谢中间产物的解毒能力受损有关,此类产物与某些机体组织形成抗原复合物导致免疫反应,启动本病发生。最近,也有研究[5]证明一些HLA主要组织相容性复合体等位基因与发生该病有关联。SJS组织病理学特征主要是角质形成细胞凋亡而导致广泛的表皮坏死,CD8细胞在该过程中充当介体,目前公认的两条导致凋亡的途径:Fas(CD95,角质形成细胞膜受体)与其FasL配体(CD95L)的结合以及穿孔素和粒酶B的释放[6]。
SJS的实验室检查可能会显示非特异性白细胞增多及嗜酸性粒细胞的增加,部分患者可有血细胞减少。该例患者病史长达16,白细胞、嗜酸性粒细胞及血细胞检测未见明显异常,但超敏C反应蛋白及循环免疫复合物浊度仍偏高,这可能与该例患者病情的持续进展相关。CPR升高可反映体内炎症处于急性活动期或有组织坏死存在;循环免疫复合物浊度大,则说明其血液中的浓度增加,病情活动。循环免疫复合物可较长时间游离于血液和其他体液中,当血管壁通透性增加时,它可随血流沉积在某些部位,激活补体导致免疫复合物沉积的发生。免疫复合物的沉积可能是导致间质性肺炎及眼部症状进行性加重的原因之一。
SJS初期主要表现为急性前驱症状,如发热、 咽痛等,随后皮肤出现红斑或紫癜样皮疹,皮损最早见于躯干胸骨前区、面部及手掌足趾,皮损可融合形成大疱、发生表皮剥脱。口腔、眼鼻和生殖器黏膜均可出现糜烂破溃,严重的病例可出现消化道和呼吸道受损,甚至心、肝、肾的损害。50%~88%的SJS患者可有急性眼部受累[7],初期主要表现为非特异性的眼表炎症:睑缘红肿、溃烂;结膜充血、脓性分泌增多、伪膜形成;角膜水肿及点片状上皮缺损,重者可形成角膜溃疡或穿孔。35%患者可出现慢性眼部后遗症[8],主要特征有眼睑瘢痕化,睑内翻,睑球粘连,角膜新生血管形成及角膜缘干细胞缺乏等,最终导致视力丧失。该例患者已致严重的眼部并发症:睑内翻、睑球粘连、角膜溃疡伴新生血管形成、视力严重下降(右眼0.1,左眼仅光感)。
SJS病死率约为5%[1,3],早期诊断尤为关键。其诊断要点:1)大疱样皮肤坏死伴特征性皮肤靶 样病变;2)表皮剥脱面积<30%体表面积[9];3)严重的皮肤黏膜病变,黏膜病变至少累及两个部位黏膜;4)突出的急性前驱症状;5)80%的患者可同时有眼部症状。SJS应受到皮肤科、眼科和口腔科等各科医生的重视,诊断时需详细询问患者的病史,特别是相关药物的服用史,不仅要注意 皮肤、眼、黏膜的病变,还要注意全身各系统如肺、肾及神经系统的变化,同其他科室密切合作,及时会诊,及早诊断,减少病死率。
SJS初期主要表现为急性前驱症状,如发热、 咽痛等,随后皮肤出现红斑或紫癜样皮疹,皮损最早见于躯干胸骨前区、面部及手掌足趾,皮损可融合形成大疱、发生表皮剥脱。口腔、眼鼻和生殖器黏膜均可出现糜烂破溃,严重的病例可出现消化道和呼吸道受损,甚至心、肝、肾的损害。50%~88%的SJS患者可有急性眼部受累[7],初期主要表现为非特异性的眼表炎症:睑缘红肿、溃烂;结膜充血、脓性分泌增多、伪膜形成;角膜水肿及点片状上皮缺损,重者可形成角膜溃疡或穿孔。35%患者可出现慢性眼部后遗症[8],主要特征有眼睑瘢痕化,睑内翻,睑球粘连,角膜新生血管形成及角膜缘干细胞缺乏等,最终导致视力丧失。该例患者已致严重的眼部并发症:睑内翻、睑球粘连、角膜溃疡伴新生血管形成、视力严重下降(右眼0.1,左眼仅光感)。
SJS病死率约为5%[1,3],早期诊断尤为关键。其诊断要点:1)大疱样皮肤坏死伴特征性皮肤靶 样病变;2)表皮剥脱面积<30%体表面积[9];3)严重的皮肤黏膜病变,黏膜病变至少累及两个部位黏膜;4)突出的急性前驱症状;5)80%的患者可同时有眼部症状。SJS应受到皮肤科、眼科和口腔科等各科医生的重视,诊断时需详细询问患者的病史,特别是相关药物的服用史,不仅要注意 皮肤、眼、黏膜的病变,还要注意全身各系统如肺、肾及神经系统的变化,同其他科室密切合作,及时会诊,及早诊断,减少病死率。
SJS的治疗首先应去除可疑的病因,及时停用可疑药物,延迟停药可使病死率上升。及早足量使用糖皮质激素也是关键,病情稳定激素可逐步减量,病情迁延反复者酌情用一段时间维持量。
另外,静脉免疫球蛋白注射可选择性阻断角质形成细胞凋亡。对症支持措施包括:控制体温,保持气道通畅及水、电解质平衡,减轻疼痛,早期口服营养或肠外营养等[1]。对于SJS眼部损害的
治疗,急性期需要保持患者眼部清洁,预防性使用抗生素,糖皮质激素可以缓解炎症、减少并发症的发生,人工泪液有利于维持角膜上皮的完整性,也可局部使用免疫抑制剂。慢性期SJS眼部并
发症患者常发生睑球粘连、角膜新生血管形成、角膜缘干细胞缺乏等,主要采取手术方式来治疗,比如羊膜移植、角膜缘干细胞移植、角膜移植等[2]。该例患者主要考虑手术治疗,但术后效果
可能欠佳。
此病严重期约为10 d左右,15~30 d可愈。但即使治愈后仍可能继续进展,迁延反复,最终导致视力障碍甚至更严重的后遗症。本例患者初发病时眼部症状较轻,仅表现为眼红眼痛,分泌增多等症状,经用药症状缓解后未予以重视,而后出现病情反复,未进行充分的治疗,导致视力进行性下降(右眼0.1,左眼仅遗留光感),眼表病变逐渐加重(角膜溃疡伴新生血管形成,甚至出现睑球粘连)。超敏C反应蛋白2.37 mg/L(偏高),循环免疫复合物浊度CIC 118(偏高)可能也提示患者的病情仍在进展中。因此患者病情稳定、症状缓解后仍须定期复查,不充分的治疗可能延误病情,导致严重后果。切勿擅自减量或停用药物,注意观测眼、皮肤、 黏膜的变化情况,必要时复查实验室相关指标(如 循环免疫复合物浊度、C反应蛋白、血沉及血常规等),一旦出现病情反复则须及时干预和治疗。
此病严重期约为10 d左右,15~30 d可愈。但即使治愈后仍可能继续进展,迁延反复,最终导致视力障碍甚至更严重的后遗症。本例患者初发病时眼部症状较轻,仅表现为眼红眼痛,分泌增多等症状,经用药症状缓解后未予以重视,而后出现病情反复,未进行充分的治疗,导致视力进行性下降(右眼0.1,左眼仅遗留光感),眼表病变逐渐加重(角膜溃疡伴新生血管形成,甚至出现睑球粘连)。超敏C反应蛋白2.37 mg/L(偏高),循环免疫复合物浊度CIC 118(偏高)可能也提示患者的病情仍在进展中。因此患者病情稳定、症状缓解后仍须定期复查,不充分的治疗可能延误病情,导致严重后果。切勿擅自减量或停用药物,注意观测眼、皮肤、 黏膜的变化情况,必要时复查实验室相关指标(如 循环免疫复合物浊度、C反应蛋白、血沉及血常规等),一旦出现病情反复则须及时干预和治疗。
基金
暂无基金信息
参考文献
1. Wong A, Malvestiti AA, Hafner Mde F. Stevens-Johnson syndrome and toxic epidermal necrolysis: a review[J]. Rev Assoc Med Bras (1992), 2016, 62(5): 468-473.
2. Stephen Foster C, Ba-Abbad R. Stevens-Johnson Syndrome[EB/OL]. Medscape. Drugs & Diseases Ophthalmology. Updated: Dec 15, 2016.
3. Laun J, Laun K, Muftah M, et al. Stevens-Johnson Syndrome[J]. Eplasty, 2016, 16: ic47.
4. Rufini S, Ciccacci C, Politi C, et al. Stevens-Johnson syndrome and toxic epidermal necrolysis: an update on pharmacogenetics studies in drug-induced severe skin reaction[J]. Pharmacogenomics, 2015, 16(17): 1989-2002.
5. Van Zyl L, Carrara H, Lecuona K. Prevalence of chronic ocular complications in Stevens-Johnson syndrome and toxic epidermal necrolysis[J]. Middle East Afr J Ophthalmol, 2014, 21(4): 332-335.
6. Schneider JA, Cohen PR. Stevens-Johnson syndrome and toxic epidermal necrolysis: a concise review with a comprehensive summary of therapeutic interventions emphasizing supportive measures[J]. Adv Ther, 2017, 34(6): 1235-1244.
7. Kohanim S, Palioura S, Saeed HN, et al. Acute and chronic ophthalmic involvement in Stevens-Johnson syndrome/toxic epidermal necrolysis - a comprehensive review and guide to therapy. II. ophthalmic disease[J]. Ocul Surf, 2016, 14(2): 168-188.
8. Jongkhajornpong P, Lekhanont K, Siriyotha S, et al. Factors contributing to long-term severe visual impairment in Stevens-Johnson syndrome and toxic epidermal necrolysis[J]. J Ophthalmol, 2017, 2017: 2087578.
9. Chow LLW, Shih KC, Chan JCY, et al. Comparison of the acute ocular manifestations of Stevens-Johnson syndrome and toxic epidermal necrolysis in Chinese eyes: a 15-year retrospective study[J]. BMC Ophthalmol, 2017, 17(1): 65.