银杏去甲基酮酯对激光诱导脉络膜新生血管恒河猴模型的药效学研究
关键词
摘要
目的:探讨银杏去甲基酮酯对恒河猴激光致脉络膜新生血管(choroidal neovascularization, CNV)生成的抑制作用。方法:16只健康恒河猴进行双眼眼底激光光凝形成CNV造模后,设安慰剂组(n=6)、康柏西普眼内注射液组(n=3)、银杏叶提取物组(n=3)、银杏去甲基酮酯组(n=4)。分别在造模第21天(D0)给药前及给药后的第28天(D28)进行眼底摄影(fundus photography, FP)、眼底荧光素血管造影(fundus fluorescein angiography, FFA)、光学相干断层扫描(optical coherence tomography, OCT)检查;主要疗效指标包括给药前后Ⅳ级光斑数量、Ⅳ级光斑荧光渗漏面积变化率,Ⅳ级光斑视网膜厚度变化率。结果:Ⅳ级光斑数量、Ⅳ级光斑荧光渗漏面积变化率和Ⅳ级光斑视网膜厚度变化观测指标,安慰剂组结果分别为30个、(101.7±84.3)%、(64.7±91.5)%,康柏西普眼内注射液组结果分别为20个、(−100.0±0.0)%、(−94.1±14.3)%,银杏叶提取物组分别为24个,(19.9±76.23)%、(3.0±102.03)%,银杏去甲基酮酯组结果分别为26个、−(34.7±53.3)%、−(58.6±48.5)%,银杏去甲基酮酯组与安慰剂组比较差异均有统计学意义(P<0.05)。结论:银杏去甲基酮酯对恒河猴CNV模型的荧光渗漏和视网膜增厚有显著的改善作用。
全文
文章亮点
1. 关键发现
• 通过激光诱导脉络膜新生血管 (choroidal neovascularization, CNV) 恒河猴模型实验证实,银杏去甲基酮酯对 CNV 相关病理改变具有显著改善作用。与安慰剂组相比,其能减少 Ⅳ 级光斑数量,降低荧光素渗漏面积[变化率为(−34.7±53.3)%],减轻视网膜增厚[变化率为 (−58.6±48.5)%],且各项指标差异均有统计学意义 (P<0.05),呈现多维度的治疗效果。
2. 已知与发现
• 已知银杏叶提取物 (如 EGb 761) 具有抗氧化、改善微循环等作用,可能延缓年龄相关性黄斑变性 (age-related macular degeneration, AMD) 进展,但疗效有限且需更多验证;抗 VEGF 药物 (如康柏西普) 是湿性 AMD 一线疗法,但存在给药方式复杂、耐药性等问题。本研究发现,作为高浓度银杏叶提取物的银杏去甲基酮酯,其药效显著优于普通银杏叶提取物,能有效抑制灵长类动物 CNV 病理进程,且为口服制剂,弥补了现有药物的部分局限性。
3. 意义与改变
• 为湿性 AMD 提供了潜在治疗方向,银杏去甲基酮酯的口服给药特性的多重作用机制,有望成为抗 VEGF 药物的辅助或替代方案,解决临床中频繁注射、成本高等问题。
• 首次在恒河猴 (与人类眼部生理高度相似的灵长类模型) 中证实银杏去甲基酮酯的药效,实验体系稳定可靠,为后续临床转化提供了坚实的临床前数据支持。拓展了银杏叶提取物在眼科疾病治疗中的应用深度,为基于天然活性成分的 AMD 创新药物研发奠定基础。
年龄相关性黄斑变性(age-related macular degeneration, AMD)是一种随年龄增加而发病率上升并导致患者中心视力下降的疾病,主要表现为视力下降、视物模糊、变形[1]。AMD病变主要累及黄斑区,临床分为两种类型:干性和湿性,“湿性”又称作“渗出性”或“新生血管性”AMD (neovascular age-related macular degeneration, nAMD),以视网膜色素上皮细胞(retinal pigment epithelium, RPE)下有新生血管膜存在,引起渗出、出血、后期瘢痕形成为主要特点[2]。nAMD的治疗主要针对脉络膜新生血管(choroidal neovascularization, CNV),玻璃体腔注射抗血管内皮生长因子(vascular endothelial growth factor, VEGF)药物已被认为是nAMD的一线治疗方案,但该方案并不能使所有患者获益[3]。银杏叶提取物(如EGb 761包括24%银杏黄酮苷和6%萜类内酯)因其抗氧化和改善血流的作用,被认为可能延缓AMD进展,研究提示其可能改善视功能可以用来防治nAMD的氧化应激[4],但仍需要更大规模、长期随访的试验[5]。既往认为银杏叶提取物的药理作用是通过清除自由基,消除过氧化物对血管内皮细胞脂质层的超氧化攻击,维护血管内膜光滑及柔韧性,防止血管老化[6-7];拮抗血小板活化因子(platelet-activating factor receptor antagonist, PAF),抑制血小板凝聚,解聚血小板、红细胞、白细胞聚集,抗血栓形成[8]。降低红细胞刚性指数,增加其可塑性,加快血液流速,改善血液流变学,改善微循环,抗休克[9-10];促进一氧化氮(nitric oxide, NO) 合成及释放,诱导上皮细胞凋亡,解除平滑肌痉挛。
本研究中的银杏去甲基酮酯为银杏叶提取物,主要成分与银杏叶提取物一致,但是浓度比已上市的银杏叶提取物的浓度要高,具有一定的潜在的研究价值。另外,恒河猴因其视网膜解剖结构、免疫系统及血管生成调控机制与人类高度相似,成为构建CNV模型的理想物种。因此,本研究采用激光诱导CNV恒河猴模型来评估银杏去甲基酮酯的药效学,为年龄相关性黄斑变性提供可能的诊疗方向。
1 材料与方法
1.1 动物
16只恒河猴,雌雄各半,年龄为3~5 岁,体质量为3.95~6.31 kg,购自雅安普莱美生物科技有限公司,许可证号:SCXK(川)2019-027。饲养房间:动物饲养条件:温度18~26 ℃,相对湿度40%~70%。
1.2 供试品和对照品
供试品:银杏去甲基酮酯(批号:20190109,规格40 g/袋,河北荃美生物科技有限公司)。安慰剂:明胶空心胶囊(批号:200536,浙江省浦江县恩尔康胶囊有限公司)。阳性对照药1:康柏西普眼用注射液(批号:201909b20,规格:0.2 mL/支,成都康弘生物科技有限公司);阳性对照药2:银杏叶提取物片(批号:6970419,规格:每片含有银杏叶提取物40 mg,德国威玛舒培博士药厂)。
1.3 试验试剂和仪器
1.3.1 试验试剂
复方托吡卡胺滴眼液(美多丽)(规格:10 mL/支,批号:MP2116,日本Santen Pharmaceutical Co., Ltd. Shiga Plant),荧光素钠注射液(规格:5 mL/支,批号:314036F,Alcon Laboratories, Inc.),复方氯胺酮(规格:2 mL/支,批号:190304,江苏中牧倍康药业有限公司),聚维酮碘(规格:200 mL/瓶,批号:190712B,成都永安制药有限公司),红霉素眼膏[规格:2 g/支,批号:1904091,辰欣佛都药业(汶上)有限公司],潇莱威(规格:0.4 mL/支,批号:E86709G,爱尔兰艾尔建制药公司),生理盐水(规格:500 mL/瓶,批号:L219042602,四川科伦药业股份有限公司),盐酸氯胺酮(规格:2 mL/支,批号:190302,江苏中牧倍康药业有限公司),丙泊酚注射液(规格:10 mL/支,批号:1908203,四川国瑞药业有限公司)。
1.3.2 仪器
VX-20眼底照相机(KOWA Company Ltd.),Spectralis OCT Plus OCT(Heidelberg Engineering GmbH),Vitra 532nm激光仪(Quantel Medical),Area Centralis接触式眼底镜(Volk Optical, Inc.),XK3124/IND245体重秤(Mettler Toledo, LLC.),Roche Cobas6000 Analyzer Series C501生化模块全自动生化仪(Roche Diagnostics GmbH)。
1.4 试验周期
检疫期31 d,造模期21 d,给药观察期28 d。
1.5 造模
动物经复方氯胺酮8 mg/kg肌内注射麻醉后,双眼滴加美多丽(复方托吡卡胺滴眼液)散瞳。双眼瞳孔大于6 mm后,将动物头部固定于眼科激光光凝仪前,操作人员通过眼底镜窥清视网膜结构后,围绕黄斑中心一个视盘距离进行激光光凝,每眼9个点。激光参数:波长532 nm,能量650~675 mW,光斑直径50 μm,曝光时间0.1 s。激光光凝19 d后进行眼底血管荧光造影和OCT检查。形成Ⅳ级荧光渗漏光斑认为造模成功。
1.6 动物纳排标准
1.6.1 动物入选标准
至少一只眼睛中具有1个的Ⅳ级荧光渗漏斑点。
1.6.2 动物排除标准
严重眼部炎症或眼底病变。
1.6.3 中止试验标准及剩余动物的处理
中止试验标准:1)严重外伤和感染;2)兽医根据相关标准操作规程(standard operating procedure, SOP)判断需要中止试验的情况。
剩余动物的处理:实验结束后所有动物返还本动物管理部门。
1.7 分组及给药方法
1.7.1 分组
本实验设置4个组,每只动物至少有1只眼球符合入选标准。给药剂量见表1。阳性对照组(康柏西普眼用注射液组和银杏叶提取物组):因康柏西普眼用注射液和银杏叶提取物作为已获批药物,其疗效已有充分文献支持,故采用较少动物(3只)以减少不必要的资源消耗。实验组(银杏去甲基酮酯组):为初步探索药效,选择中等样本量(4只)以平衡统计功效与伦理要求。安慰剂组(6只):增加样本量以提高基线数据的稳定性。
|
组别 |
给予药物 |
给药剂量 |
给药途径 |
给药频率 |
动物数 |
符合入选标准眼球数 |
|
安慰剂组 |
空胶囊 |
|
口服 |
每天2次 |
6 |
10 |
|
康柏西普眼用注射液组 |
康柏西普眼用注射液 |
0.5 mg/眼 |
玻璃体腔注射 |
单次 |
3 |
5 |
|
银杏叶提取物组 |
银杏叶提取物片 |
6 mg/kg |
口服 |
每天2次 |
3 |
5 |
|
银杏去甲基酮酯组 |
7-去甲基银杏双黄酮/银杏酮酯 |
6 mg/kg |
口服 |
每天2次 |
4 |
6 |
1.7.2 给药方法
安慰剂组、实验组、银杏叶提取物组,口服给药,每天2次,连续给药28 d;康柏西普眼用注射液,单次给药,玻璃体内注射。剂量依据:阳性药银杏叶提取物 6 mg/kg(金纳多,按说明书给药6 mg/kg),另外实验组也按照 6 mg/kg进行给药研究,康柏西普眼用注射液按照说明书剂量计算为0.5 mg/眼。
1.8 观察指标
1.8.1 主要药效指标
FP、FFA、OCT检查:在造模前1次,给药前1次,给药第28天(D28)各1次。另外,造模当天进行1次FP检查。FP共计4次,FFA、OCT共计3次。
评价指标:1) Ⅳ级光斑的数量。按照表2,对FFA图片中的激光斑进行分级,将各组动物的Ⅳ级光斑总数作为药效评价指标之一。2)荧光素渗漏面积的变化率。采用Image J 软件(版本 1.52a, NIH, Wayne, Rasband, USA)测量FFA晚期(10 min)Ⅳ级光斑的荧光素渗漏面积,作为FFA的药效评价指标之一。Ⅳ级光斑荧光素渗漏面积的变化率计算方式如下所示。
荧光素渗漏面积的变化率(%)=(给药后荧光素渗漏面积−给药前荧光素渗漏面积) /给药前荧光素渗漏面积×100%
3)视网膜厚度的变化率。
视网膜厚度的变化率(%)= (给药后视网膜厚度−给药前视网膜厚度)/给药前视网膜厚度×100%
|
光斑分级 |
光斑表现 |
|
I级 |
光斑无强荧光 |
|
Ⅱ级 |
光斑强荧光但无渗漏 |
|
Ⅲ级 |
光斑强荧光,轻度荧光素渗漏,但渗漏不超过光斑边缘 |
|
Ⅳ级 |
光斑强荧光,显著荧光素渗漏,且渗漏超过光斑边缘 |
1.8.2 数据处理
采用Microsoft Office Excel 2013和 SPSS Statistics 13.0 软件进行数据处理和统计分析。计量资料统计结果以个体数据形式表示。Ⅳ级光斑荧光素渗漏面积变化率、视网膜厚度变化率指标均采用均数±标准差( Mean ± SD)进行描述。Ⅳ级光斑荧光素渗漏面积变化率及视网膜厚度变化率先进行LEVENE方差齐性检验,若方差齐性则采用单因素方差分析(ANOVA)比较均数的组别差异,均数组别差异有统计学意义时(P< 0.05),采用最小显著差异法(LSD-t法)对各组间差异进行比较;若方差不齐,采用Kruskal-Wallis检验(K-W法)对各组间差异进行比较。各给药组Ⅳ级光斑数量的发生率比较采用χ2检验,所有检验均为双侧检验α=0.05。
1.8.3 动物福利
动物福利符合国际AAALAC要求,所有实验方案都经过四川普莱美行之生物科技有限公司IACUC委员会的审查和同意,批准号:AW2007;AW2027。
兽医对所有动物在整个项目期间的状态进行监护评估,在整个试验期间,对动物进行临床观察,当出现严重不适症状时由兽医进行相应处理。
2 结果
2.1 Ⅳ级光斑数量
各组动物给药前后,Ⅳ级光斑数量变化结果见表3。安慰剂组:Ⅳ级光斑数量增多,表明安慰剂组的CNV病情继续发展(图1)。康柏西普眼用注射液组:Ⅳ级光斑数量比安慰剂组减少(P<0.01)(图2)。银杏叶提取物组,Ⅳ级光斑数量未见明显增多(图3)。银杏去甲基酮酯组:Ⅳ级光斑数量比安慰剂组减少(P<0.01)(图4)。
|
组别 |
给药前光斑数量 |
给药第28天光斑总数 |
|
安慰剂组 |
30 |
34 |
|
康柏西普眼用注射液组 |
20 |
0** |
|
银杏叶提取物组 |
23 |
24 |
|
银杏去甲基酮酯组 |
26 |
17** |
|
与安慰剂组比较,**P<0.01。 Compared with the placebo group, **P<0.01. |
||
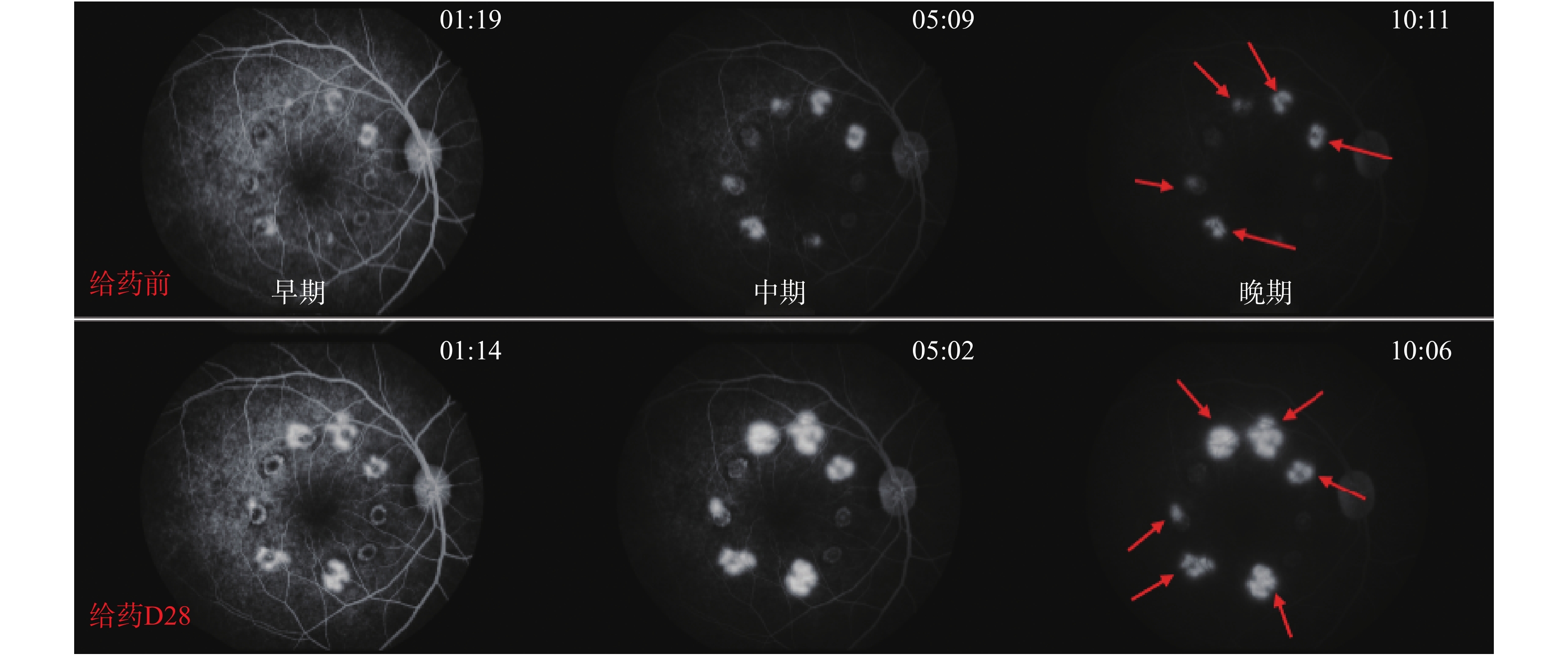
红色箭头表示Ⅳ级光斑。
The red arrows indicate grade IV spots.
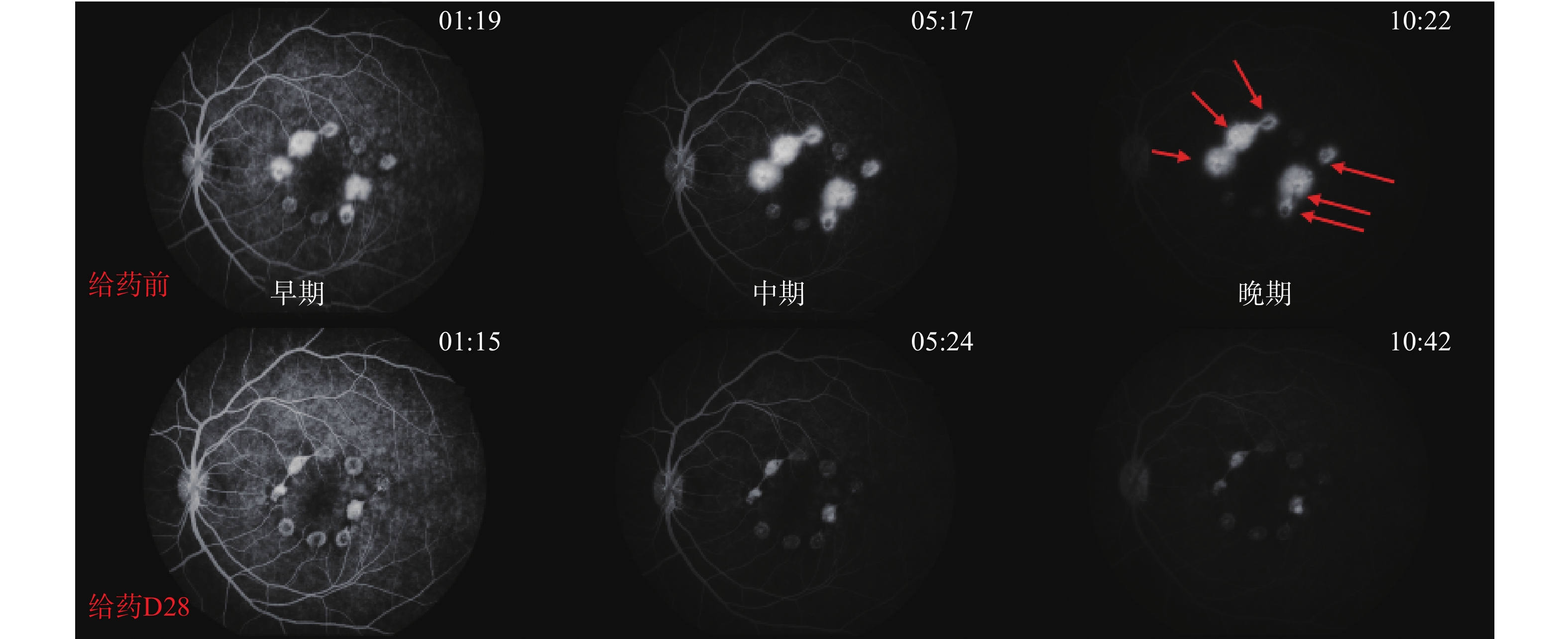
红色箭头表示Ⅳ级光斑。
The red arrows indicate grade IV spots.
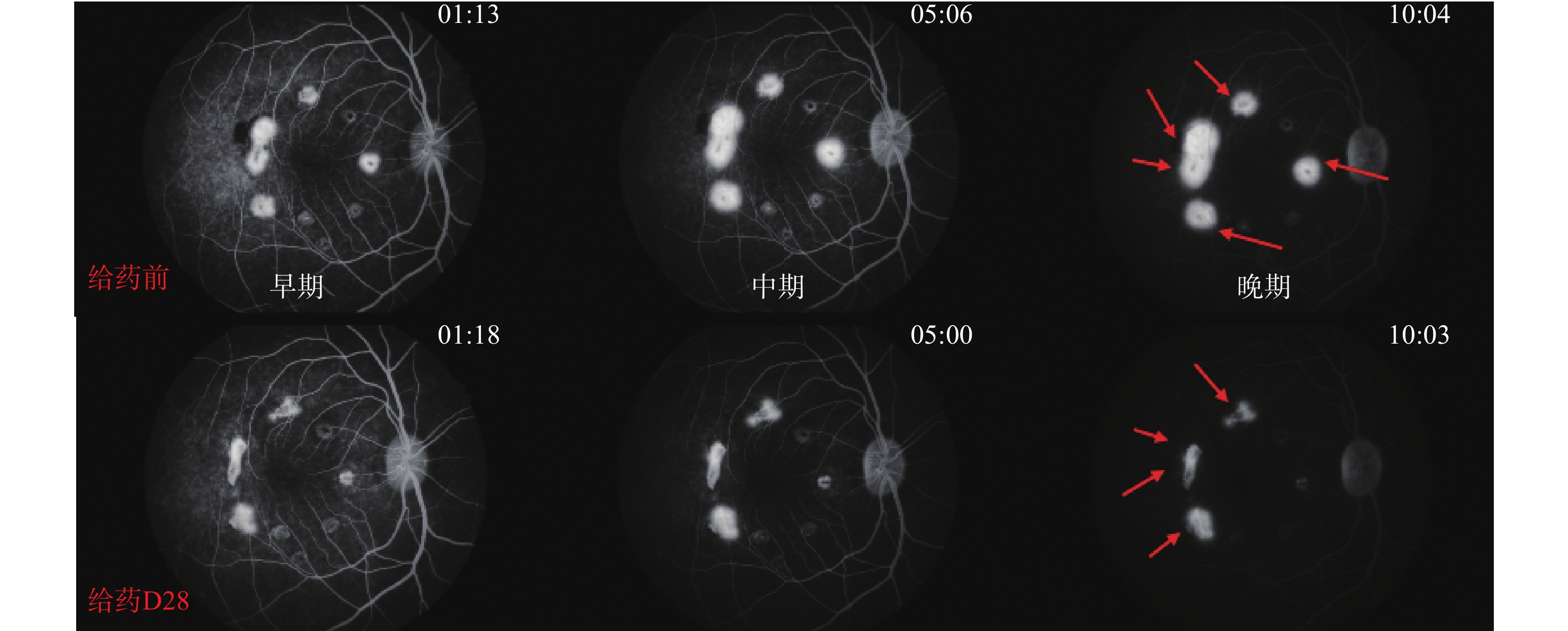
红色箭头表示Ⅳ级光斑。
The red arrows show the Ⅳ-degree spots.
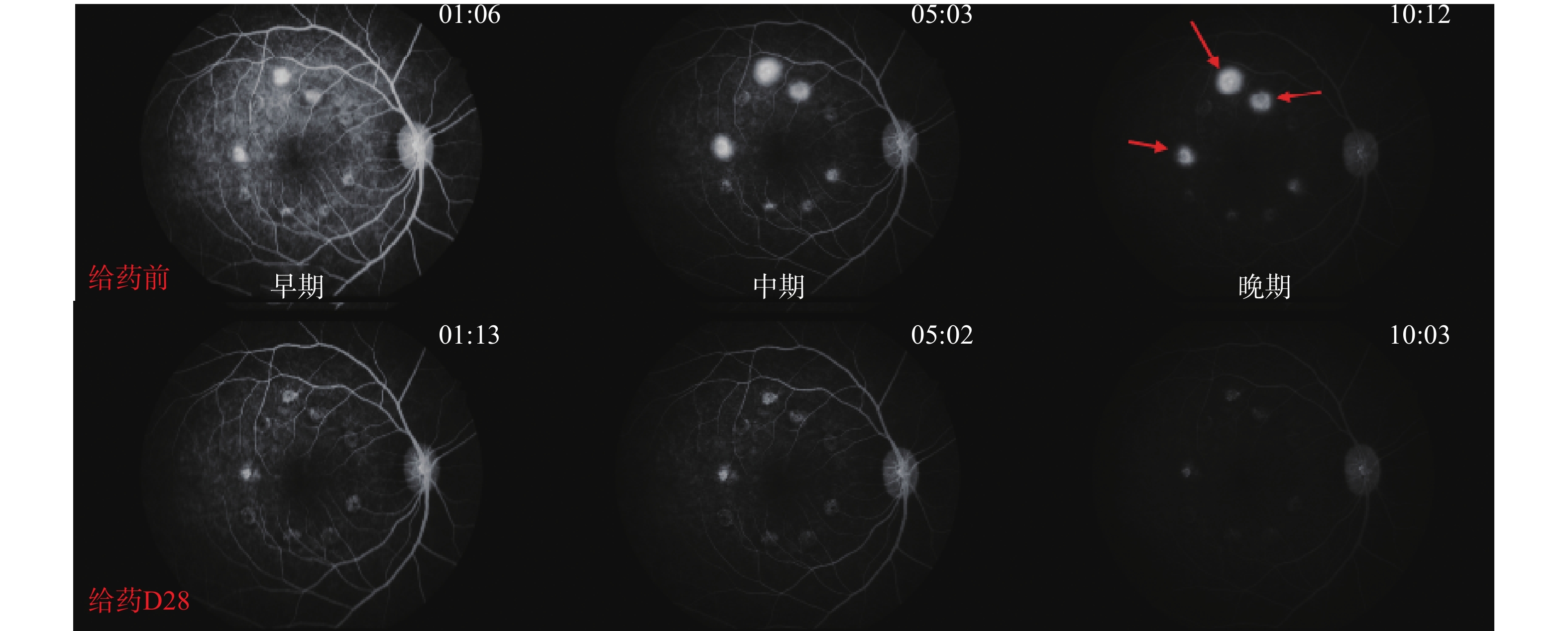
红色箭头表示Ⅳ级光斑
The red arrows indicate grade IV spots.
2.2 Ⅳ级光斑渗漏面积变化率
各组动物给药后,Ⅳ级光斑渗漏面积变化率见表4。安慰剂组:Ⅳ级光斑渗漏面积增加,CNV病情继续发展(图1)。康柏西普眼用注射液组:Ⅳ级光斑渗漏面积与安慰剂组明显缩小(P<0.01)(图2)。银杏叶提取物组:Ⅳ级光斑渗漏面积略有增加,但增加幅度小于安慰剂组(图3)。银杏去甲基酮酯组:Ⅳ级光斑渗漏面积比安慰剂组缩小(P<0.05)(图4)。
|
组别 |
给药第28天Ⅳ级光斑的渗漏面积变化率/% |
|
安慰剂组(n=6) |
101.7±84.3 |
|
康柏西普眼用注射液组(n=3) |
−100.0±0.0** |
|
银杏叶提取物组(n=3) |
19.9±76.2 |
|
银杏去甲基酮酯组(n=4) |
−34.7±53.3* |
|
与安慰剂组比较,*P<0.05, **P<0.01。 Compared with the placebo group, *P<0.05, **P<0.01. |
|
2.3 Ⅳ级光斑视网膜厚度变化率
各组动物给药后,Ⅳ级光斑视网膜厚度变化率见表5。安慰剂组:Ⅳ级光斑视网膜厚度增加,与给药前比较,Ⅳ级光斑视网膜厚度变化率为(64.7±91.5)%,安慰剂组的CNV病情继续发展(图5)。康柏西普眼用注射液组:Ⅳ级光斑视网膜厚度明显减少,与给药前比较,Ⅳ级光斑视网膜厚度变化率为(−94.1±14.3)%,与安慰剂组比较差异有统计学意义(P<0.01)(图6)。银杏叶提取物组:Ⅳ级光斑视网膜厚度未见明显发展(图7)。银杏去甲基酮酯组:Ⅳ级光斑视网膜厚度明显减少,与给药前比较,Ⅳ级光斑视网膜厚度变化率为(−58.6±48.5)%。与安慰剂组比较差异有统计学意义(P<0.05)(图8)。
|
组别 |
给药第28天Ⅳ级光斑的视网膜厚度变化率/% |
|
安慰剂组 |
64.7±91.5 |
|
康柏西普眼用注射液组 |
−94.1±14.3** |
|
银杏叶提取物组 |
3.0±102.0 |
|
银杏去甲基酮酯组 |
−58.6±48.5* |
|
与安慰剂组比较,*P<0.05, **P<0.01。 Compared with the placebo group, *P<0.05, **P<0.01. |
|
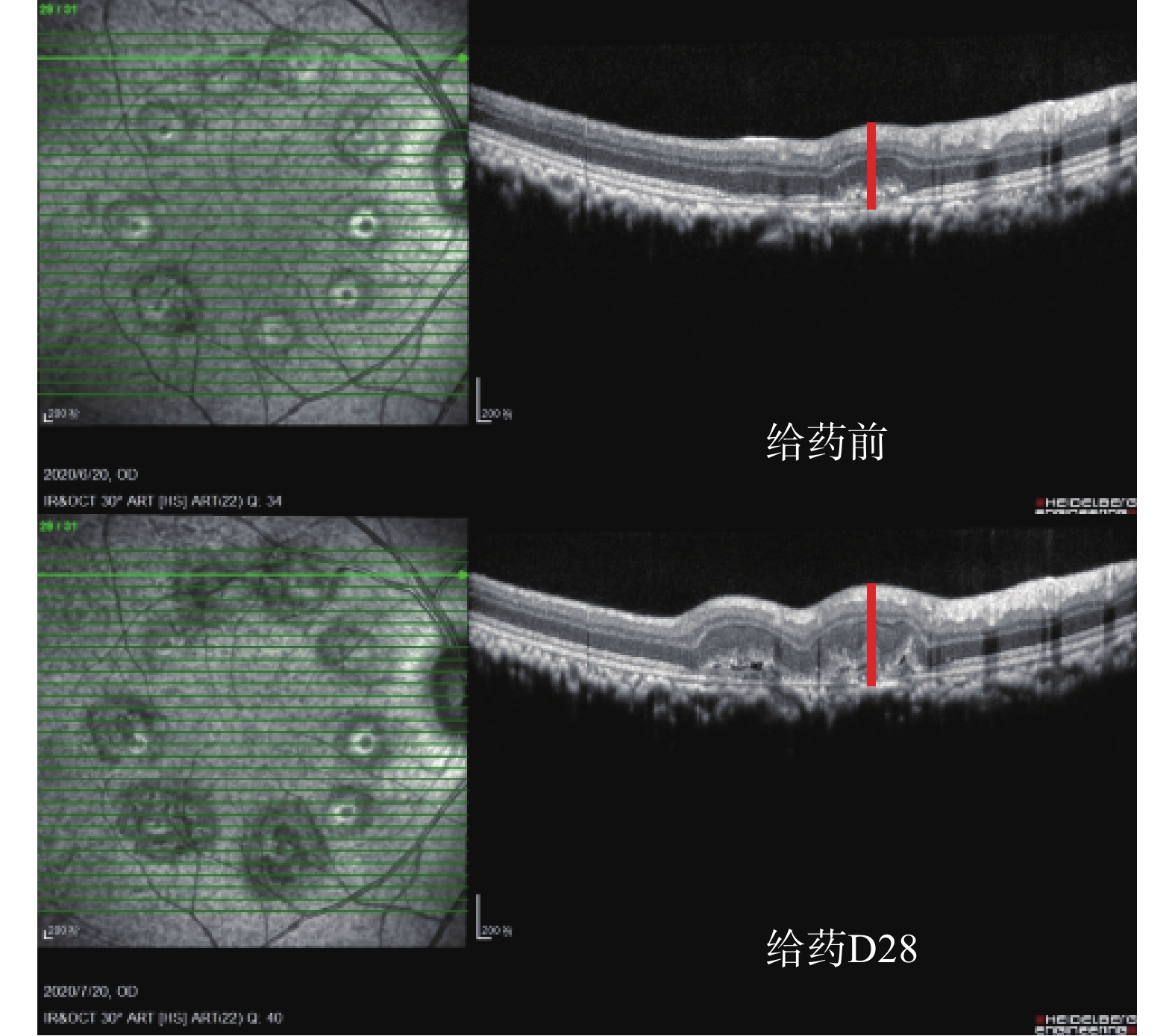
红线表示Ⅳ级光斑的视网膜厚度测量位置。
The red lines indicate the locations of retinal thickness measurement of grade IV lesion.
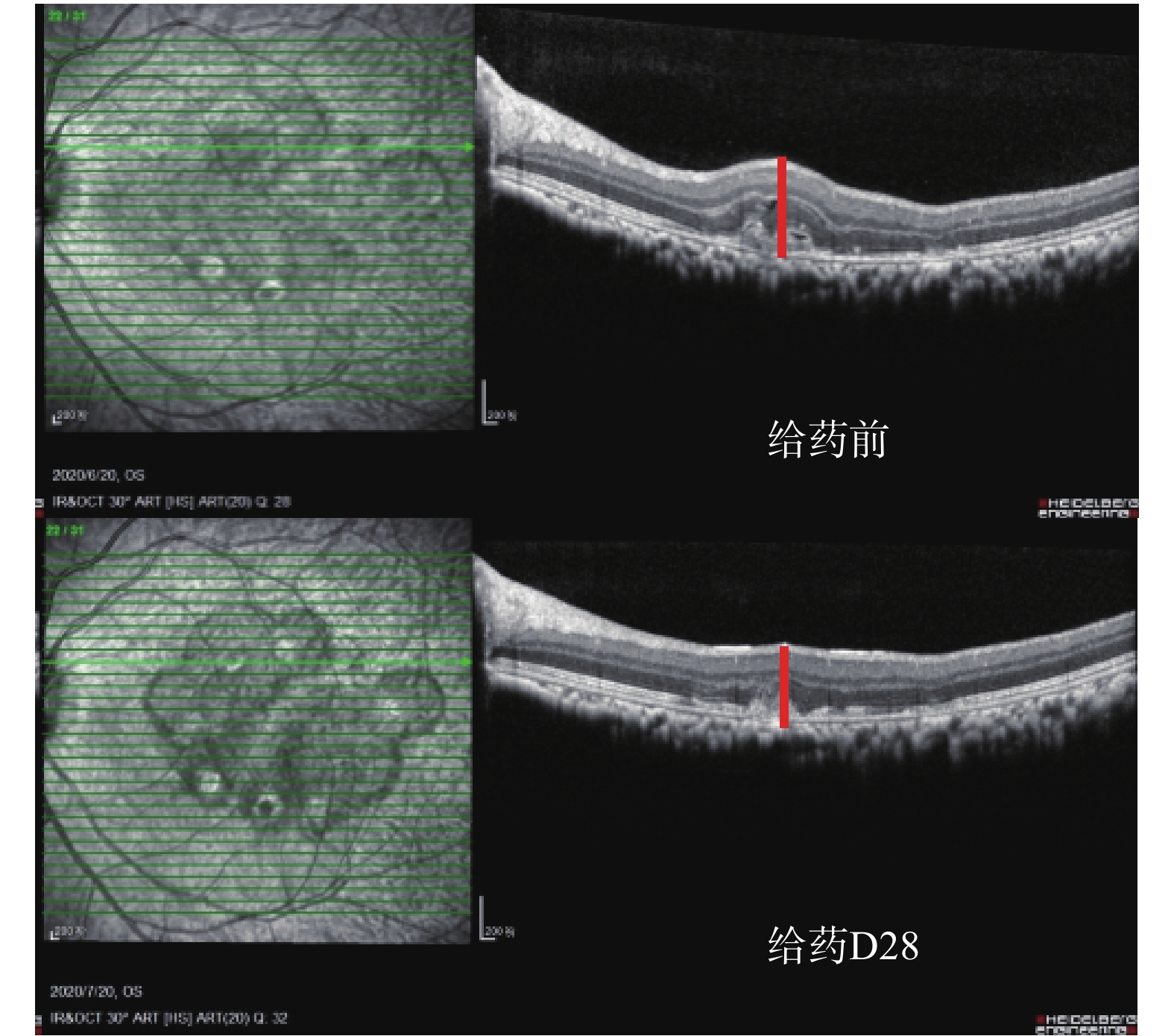
红线表示Ⅳ级光斑的视网膜厚度测量位置。
The red lines indicate the locations of retinal thickness measurement of grade IV lesion.
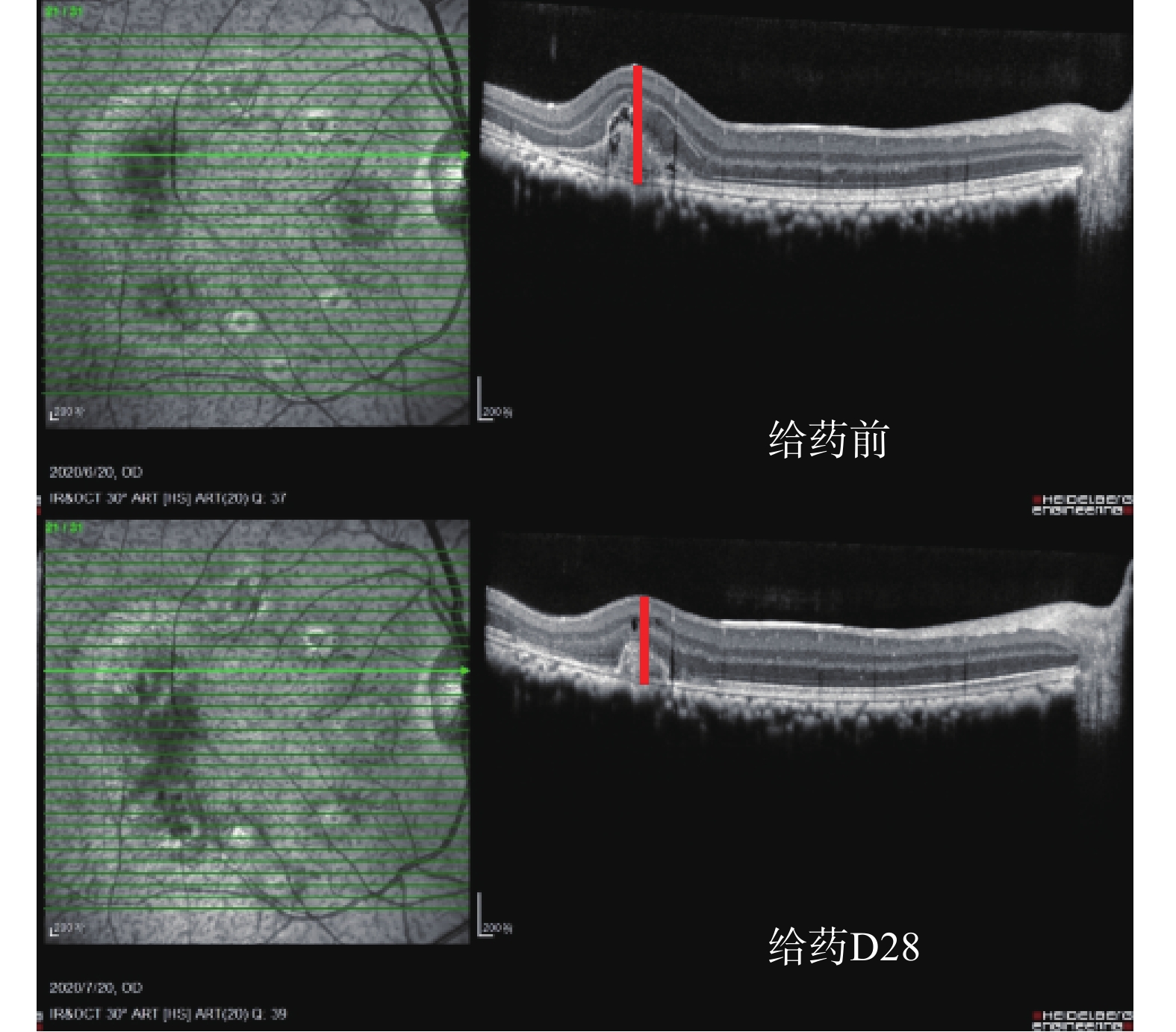
红线表示Ⅳ级光斑的视网膜厚度测量位置。
The red lines indicate the locations of the retinal thickness measurement of the IV grade light spot.
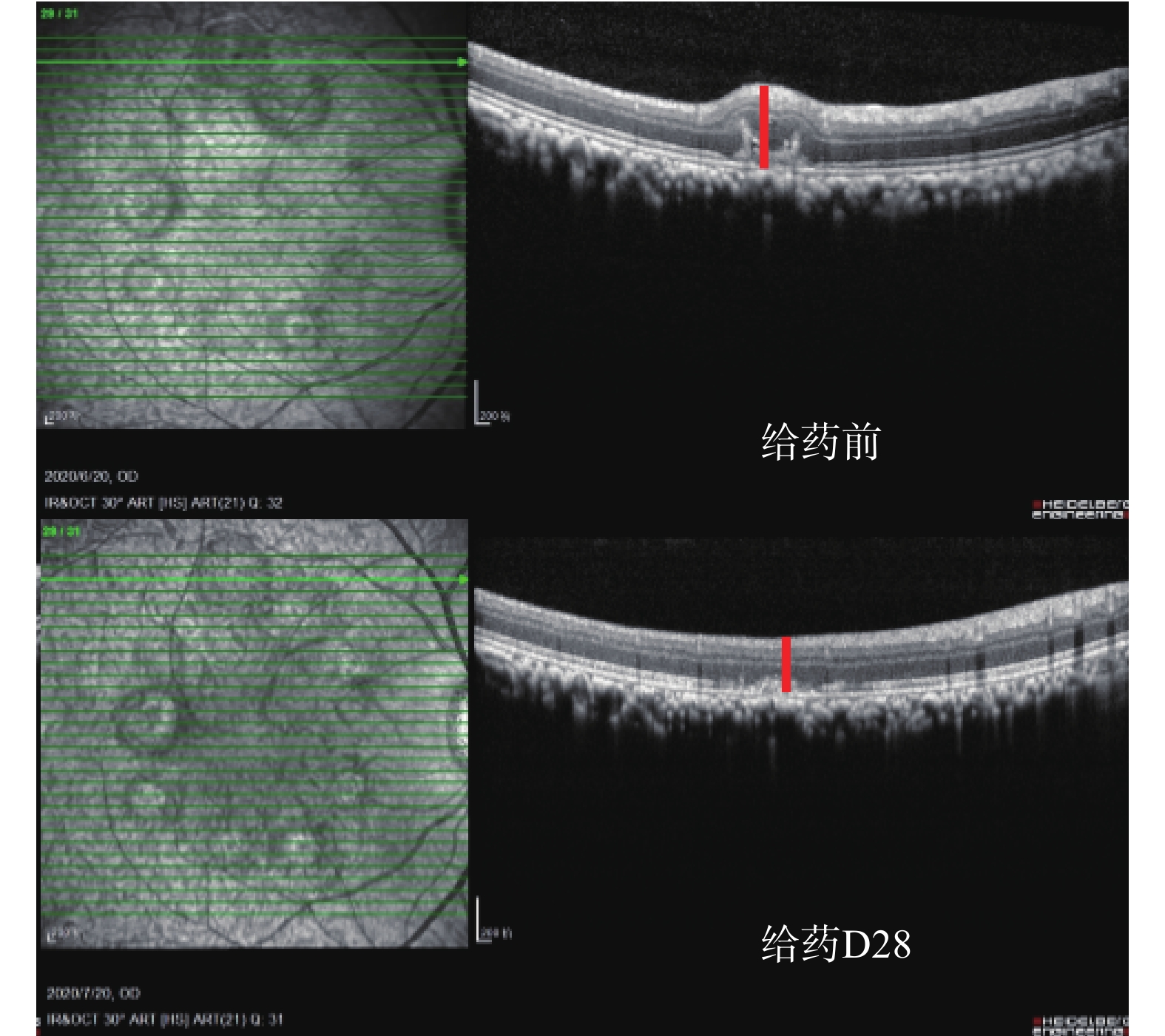
红线表示Ⅳ级光斑的视网膜厚度测量位置。
The red lines indicate the locations of the retinal thickness measurement of grade IV spots.
3. 讨论
本研究成功构建具有临床相关性的恒河猴CNV模型,非人灵长类动物激光诱导的 CNV 模型是临床前评估湿性 AMD 的首选模型[11-12],激光诱导 CNV 模型因其建模方法简单、耗时短、成本相对较低等优点而得到广泛应用。恒河猴与人类有许多共同的眼部和视觉特征,其病理特征与人类AMD临床表现高度吻合[13-14]。
本实验中阳性对照组康柏西普的药效结果与文献报道相似[15-16],充分验证了实验体系的可靠性。银杏叶提取物组,Ⅳ级光斑数量未见明显增多,Ⅳ级光斑渗漏面积略有增加但增加幅度小于安慰剂组,Ⅳ级光斑视网膜厚度未见明显发展,表明银杏叶提取物6 mg/kg剂量对CNV的发展有一定的抑制作用,但各药效指标与安慰剂组比较差异未见统计学意义(P>0.05)。实验结果表明,银杏去甲基酮酯干预组呈现显著的时间依赖性治疗效果:不仅Ⅳ级光斑数量呈现持续下降趋势,同时模型动物的荧光渗漏强度显著降低和视网膜厚度显著减少(P<0.05),提示该化合物对CNV病理进程具有多维度改善作用。值得注意的是,银杏制剂在传统应用中的血管调节特性(包括微循环改善、血小板活化因子拮抗及自由基清除等),与AMD的核心病理机制形成多重靶向关联[5]。相关研究表明,银杏叶提取物可通过细胞外信号调节激酶1/2-核因子E2相关因子2(extracellular-regulated protein kinases 1/2-nuclear factor erythroid 2-related factor 2, ERK1/2-Nrf2) 调控[17]、血管活性调节[18]等机制减轻氧化应激对RPE细胞的损伤[19]而发挥视网膜保护作用,这与EGb 761在神经保护[20]、抗氧化损伤[21-22]、抑制血小板活化因子(inhibit platelet-activating factor, PAF)[23]、改善线粒体功能而延缓光感受器细胞凋亡[24]及视网膜功能改善[25]等方面的已有证据表明机制互补。
抗VEGF药物(如康柏西普)虽为nAMD的一线疗法,但存在频繁注射、耐药性及高成本等问题[3,26]。银杏去甲基酮酯作为口服制剂,具有给药便捷和多重机制的优势,可能成为辅助或替代治疗的候选药物。此外,其改善微循环的作用或可弥补抗VEGF药物对脉络膜血流不足的局限性[27-28]。
尽管本研究首次证实银杏去甲基酮酯在灵长类CNV模型中的治疗潜力,但其具体的剂量与药效的关系仍待研究,具体作用靶点和作用机制仍待进一步研究阐明。银杏去甲基酮酯的研究可进一步通过转录组学或蛋白质组学解析银杏去甲基酮酯的分子靶点[4,29]。另外,有的研究周期短,需延长疗程以评估其持续性和安全性[30],可通过临床前药代动力学研究优化给药方案,为开发基于银杏活性成分的AMD创新疗法提供完整证据链 。
声明
本稿件在研究和论文撰写中未使用生成式人工智能,所有作者对内容的真实性、完整性和科学性负责。所有科学贡献和智力劳动均由所有作者共同完成。
利益冲突
所有作者均声明不存在利益冲突。
开放获取声明
本文适用于知识共享许可协议(Creative Commons),允许第三方用户按照署名(BY)-非商业性使用(NC)-禁止演绎(ND)(CC BY-NC-ND)的方式共享,即允许第三方对本刊发表的文章进行复制、发行、展览、表演、放映、广播或通过信息网络向公众传播,但在这些过程中必须保留作者署名、仅限于非商业性目的、不得进行演绎创作。
基金
参考文献
Li XY. Clinical study and mechanism discussion of mingjing granule in the treatment of wet age-related macular degeneration[D]. Beijing: China Academy of Chinese Medical Sciences, 2023. DOI: 10.27658/d.cnki.gzzyy.2023.000110.
Cui GC, SAIK Amy Yi Hsan, Zhang XH, et al. Analysis of oxidative stress-related genes in wAMD based on bioinformatics and screening of targeted traditional Chinese medicine for prevention and treatment[J]. Chin Tradit Herb Drugs, 2024, 55(1): 181-189. DOI: 10.7501/j.issn.0253-2670.2024.01.019.
Li ZN. [D]. Inhibition of STAT3 Pathway Activation by Ginkgo BilobaExtract on ARDS Mechanistic Studies of Protective Effects[D]. Nanning: Guangxi Medical University, 2022. DOI: 10.27038/d.cnki.ggxyu.2022.000928.
Chen HQ. Research progress of Panax notoginseng saponins and Ginkgo biloba extract and their combination on cardiovascular protection[J]. J Ningde Norm Univ (Nat Sci), 2019, 31(3): 286-291. DOI: 10.15911/j.cnki.35-1311/n.2019.03.016.
Tian JF, Luo HZ, Liu LB, et al. Progress in mechanism and clinical application of ginkgo biloba extract in anti-atherosclerosis[J]. China Med, 2024, 19(11): 1732-1736. DOI: 10.3760/j.issn.1673-4777.2024.11.029.
Wang ZQ. Study on the effect and mechanism of ginkgolide B on no-reflow phenomenon after cerebral ischemia-reperfusion basedon PI3K/AKT pathway[D]. Chengdu: Chengdu University of TCM, 2023.
Zheng YC, Du HC, Hong YC, et al. Research progress of ginkgo biloba preparation in off-label drug use[J]. Chin J Mod Appl Pharm, 2023, 40(15): 2167-2176. DOI: 10.13748/j.cnki.issn1007-7693.20222891.
Xie JH, Song S, Xiong YN, et al. Animal models of choroidal neovascularization in ophthalmic membrane and their correlation with clinical pathogenesis[J]. Chin J New Drugs, 2022, 31(23): 2369-2376. DOI: 10.3969/j.issn.1003-3734.2022.23.015.
Dai YC. An experimental study on the treatment of choroidal neovascularization in rhesus monkeys with conbercept and triamcinolone[D]. Luzhou: Southwest Medical University, 2020. DOI: 10.27215/d.cnki.glzyu.2020.000174.
Tong H, Zhu SJ, Yao DL, et al. Effect, frequency, visual acuity and macular thickness of different administration schemes of Compaxim in the treatment of wet senile macular degeneration[J]. J Inn Mong Med Univ, 2024, 46(2): 176-179. DOI: 10.16343/j.cnki.issn.2095-512x.2024.02.021.
Chen Y. The effect and mechanism of Ginkgo biloba extract against light-induced retinal photoreceptor degeneration[D]. Nanjing: Nanjing Medical University, 2022.
Tang FM, Huang TM. Progress in clinical application research of intravitreal injection drugs in ophthalmology[J]. Chin J Clin Pharm, 2025, 34(1): 71-76. DOI: 10.19577/j.1007-4406.2025.01.015.
Wang SS, Li YN, Dai YB, et al. Mechanism of ginkgo biloba extract in repairing blue light-damaged retinal pigment epithelial cells based on network pharmacology[J]. Fujian Med J, 2024, 46(4): 103-106. DOI: 10.20148/j.fmj.2024.04.030.