可视化角膜生物力学分析仪在眼科中的应用
关键词
摘要
可视化角膜生物力学分析仪(corneal visualization scheimpflug technology, Corvis ST)结合超高速Scheimpflug成像与非接触式眼压测量技术,能够动态监测角膜形变和恢复过程,提供最大凹陷(highest concavity, HC)、曲率半径参数(radius, R)、应力-应变指数(stress-strain index, SSI)、第一次压平硬度参数(stiffness parameter at the first applanation, SP-A1)和最大凹陷硬度参数(stiffness parameter at the highest concavity, SP-HC)等多项关键生物力学参数。这些功能有助于眼科疾病的诊断和治疗。该设备在圆锥角膜的早期筛查与评估、屈光手术的术前筛查与术后监测、青光眼分型及视神经监测中具有重要价值。此外,Corvis ST还可用于甲状腺相关眼病、糖尿病性视网膜病变、中心性浆液性脉络膜视网膜病变等多种眼部疾病的生物力学特征分析,并为非感染性葡萄膜炎、遗传性视网膜病变等系统性疾病的角膜并发症提供早期预警。本文系统综述了Corvis ST的测量原理、关键参数及最新临床应用进展,旨在为眼科疾病的诊治提供支持。
全文
文章亮点
1. 关键发现
• 系统梳理现有研究证实,可视化角膜生物力学分析仪(corneal visualization scheimpflug technology, Corvis ST)的临床应用已覆盖青光眼、甲状腺相关眼病、糖尿病性视网膜病变、非感染性葡萄膜炎等眼病,为这类眼病的筛查、诊断及治疗评估等提供新方向。
• 现有研究提示角膜与巩膜生物力学特性存在关联,或可通过 Corvis ST 检测的角膜动态形变参数,间接评估巩膜相关眼病的生物力学状态,为巩膜疾病的无创评估提供潜在新方向。
2. 已知与发现
• Corvis ST 融合超高速 Scheimpflug 成像与非接触式眼压测量技术,可动态监测角膜形变与恢复过程,提供更丰富、稳定的测量数据。
• Corvis ST 在圆锥角膜与屈光手术领域具备明确临床应用价值,可通过捕捉圆锥角膜生物力学改变早于形态学异常的特征助力早期筛查,同时可为屈光手术术前筛查及术后角膜生物力学动态监测提供支撑。
3. 意义与改变
• 本综述梳理 Corvis ST 的临床应用价值,完善了角膜生物力学在眼科疾病诊断中的理论参考,其无创、高效的评估优势可优化常见眼病的临床诊疗流程,为个性化诊疗提供了新路径。
眼部疾病与眼球及其内容物的生理变化密切相关。生物力学研究可从器官到细胞水平揭示生物过程中的机械力信息[1-2]。眼球内外的组织均具有固有张力,且在封闭的球形结构中相互关联、相互作用[3]。运用生物力学方法探究眼部组织结构与功能之间的关系,有助于揭示病理过程。角膜和巩膜作为眼球的最外层,是目前生物力学研究最多的部位。
角膜是位于眼球最前端的一层薄的透明的组织,在组织学上角膜可分为5层,分别具有不同的角膜生物力学特性[4]。角膜的生物力学测量包括离体测量和活体测量。离体测量方法主要包括角膜轴向拉伸试验、角膜膨胀试验及离体全眼球测量等[2]。活体测量仪器主要包括眼反应分析仪(ocular response analyzer, ORA)、可视化角膜生物力学分析仪 (corneal visualization scheimpflug technology, Corvis ST)、布里渊显微镜(brillouin microscopy)、光学相干弹性成像(optical coherence elastography, OCE)、超声剪切波弹性成像术(ultrasonic shear wave elastography, USWE)等[5]。与传统的ORA相比,Corvis ST能够提供更加直观的动态角膜形变图像和更丰富、稳定的测量参数,体现了活体角膜生物力学测量技术的显著进步,有助于临床更精准地评估角膜的生物力学特征及其动态变形过程。基于眼球的整体性以及角膜与巩膜相似的细胞外基质成分[6–8],有学者提出角膜和巩膜可能具有相似生物力学特性[9]。因此,越来越多研究者使用Corvis ST研究巩膜相关眼病。
巩膜是一种坚韧的结缔组织,具有复杂的胶原纤维组织[10]。目前,体外巩膜生物力学特性的研究已经采用了多种方法,包括单轴条带测试[11]、巩膜样本的双轴测试[12]以及整体膨胀测试[10–13]等。体内测量巩膜生物力学特性可以通过逆向计算法[14]、三维跟踪算法[13]、虚拟场法[15]、预拟合法[16]等方法。然而,体内巩膜生物力学仍处于起步阶段。通过定量分析捐赠眼的研究证实[17],在一定的眼压范围内,Corvis ST测得的部分生物力学参数与巩膜杨氏模量(Young's modulus)显著相关。目前,Corvis ST已被用于青光眼[18]、中心性浆液性脉络膜视网膜病变(central serous chorioretinopathy, CSC)[9] 、甲状腺相关眼病(thyroid-associated ophthalmopathy, TAO)[19]等。
1. Corvis ST的测量原理
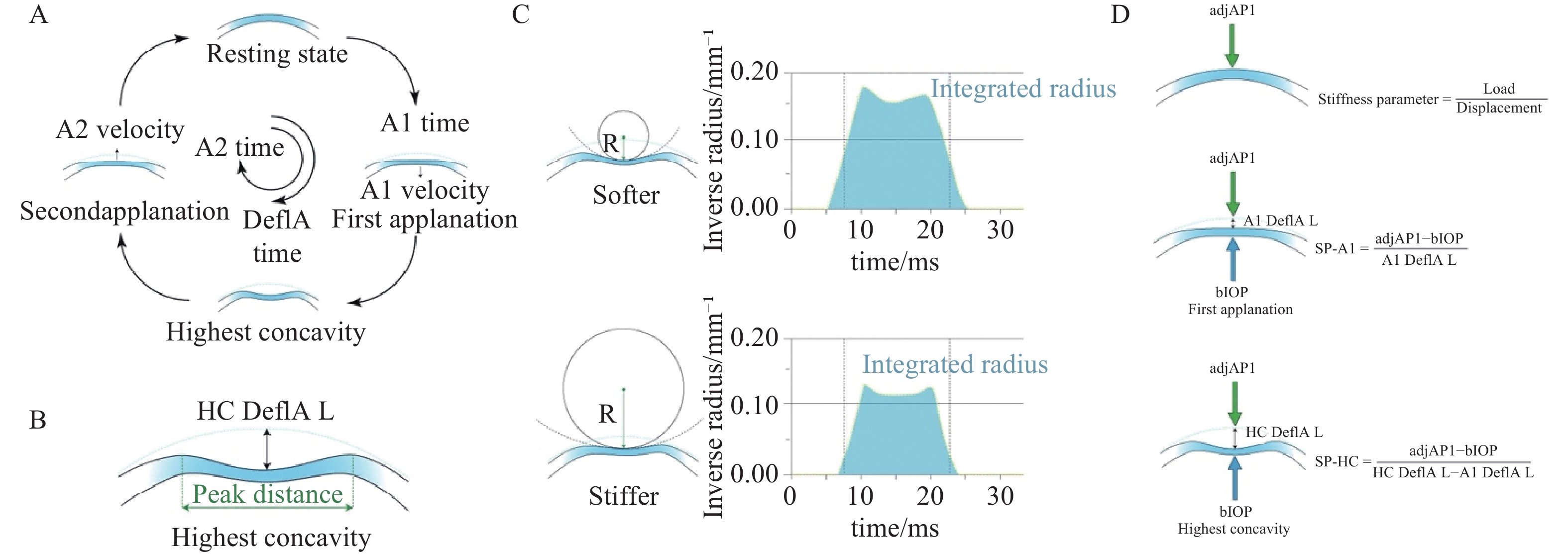
Corvis ST是一种非接触、可视化的动力学眼压分析仪,融合了超高速Scheimpflug技术,以研究角膜在外力作用下的动态变形过程。其测量原理基于空气脉冲诱导角膜形变,并利用高速Scheimpflug相机在31 ms内采集140帧断层图像,记录并分析角膜的生物力学特性。在测量过程中,设备发射脉冲气流,使角膜由凸向凹发生形变,并依次经历第一次压平(the first applanation, A1)、最大凹陷(highest concavity, HC)和第二次压平(the second applanation, A2),最终恢复至初始形态(图1)。系统软件对捕捉到的图像进行分析,提取关键生物力学参数。此外,角膜的两次压平状态由于其黏弹性、空气脉冲动力学特性及眼压作用,往往存在细微差异[20]。基于这些参数,Corvis ST可用于圆锥角膜早期筛查、屈光手术评估、青光眼风险管理等眼病诊断,为临床提供精确的角膜生物力学分析。
2. Corvis ST的测量参数
Corvis ST是一种先进的活体生物力学测量仪器,具有无需表面麻醉、无感染风险、不接触角膜、快速自动化采集等优点。通过标准的测量过程,可以获得涉及不同的阶段、时间、速度、距离、曲率等的生物力学参数。
其中,阶段相关参数(表1)包括A1、HC以及A2。时间参数记录了从气流脉冲开始到各个阶段所经历的时间,用于评估角膜的反应速度,包括A1T和A2T。速度参数反映了角膜顶点在垂直方向上的速度变化,包括第一次压平速度(the first applanation velocity, A1V)和第二次压平速度(the second applanation velocity, A2V)。峰值距离(peak distance, PD)是在最大凹陷时角膜两个最高点之间的水平距离,用于评估角膜的形变程度。曲率半径参数(radius, R)和最大倒数曲率半径(max inverse radius)分别反映了角膜的弯曲程度及其倒数,用于量化角膜凹陷的曲率特性。综合半径(integrated radius, IR)是角膜顶点倒数曲率半径的积分面积,用于评估角膜的整体变形情况。偏转幅度(deflection amplitude, DeflAmp)、整眼运动(whole eye movement, WEM)和变形幅度(deformation amplitude, DA)分别反映了角膜顶点的位移、整个眼球的垂直位移以及两者的总和,全面评估了角膜和眼球的位移情况。偏转幅度长度(deflection length, DeflAmp L)和偏转幅度时间(deflection time, DeflAmp T)则分别反映了角膜变形的长度和时间。D弧长(DArc length)指角膜中心鼻侧和颞侧3.5 mm处水平弧长的变化。变形幅度比最大值(maximum deformation amplitude ratio, DA ratio max)指角膜顶点处与距离角膜顶点1 mm或2 mm处的变形幅度之比。角膜厚度斜率(pachy slope)反映角膜厚度从中心到边缘的变化。角膜厚度比值(Ambrósio's relational thickness in the horizontal profile, ARTh)则是角膜最薄点厚度与水平方向厚度进展指数的比值。角膜生物力学指数(corvis biomechanical index, CBI)是基于多个参数计算得出的综合指数,用于全面评估角膜的生物力学特性。这些参数共同构成了Corvis ST对角膜生物力学特性的全面评估,为眼科临床实践和研究提供了丰富的数据支持。应力-应变指数(stress-strain index, SSI)[21]是基于眼睛物理行为的数值模型开发的,旨在评估角膜的材料刚度。第一次压平硬度参数(SP-A1)和最大凹陷硬度参数(SP-HC)是用于检测眼球生物力学的两个新开发参数[22],分别使用公式:
SP−A1=adjAP1−bIOPA1DeflAmpL
SP−HC=adjAP1−bIOPHCDeflAmpL−A1DeflAmpL
其中,adjAP1是Corvis设备生成的内部参数,指调整后的气压(25 mmHg);bIOP是基于生物力学的校正眼压;A1 DeflAmp L是第一次压平时的角膜偏转幅度距离。HC DeflAmp L是最大凹陷时的角膜偏转幅度距离。基于上述测量参数,Corvis ST在临床实践中的应用已日趋广泛,下面就其在不同眼病中的应用进行详细综述。
|
状态 |
属性 |
缩写 |
名称 |
描述 |
|
A1 |
时间(time) |
A1T |
A1 time (ms) |
第一次压平时间 |
|
A1 |
速度(velocity) |
A1V |
A1 velocity (m/s) |
角膜顶点在第一次压平时的速度 |
|
A2 |
时间(time) |
A2T |
A2 time (ms) |
第二次压平时间 |
|
A2 |
速度(velocity) |
A2V |
A2 velocity (m/s) |
角膜顶点在第二次压平时的速度 |
|
HC |
水平距离(horizontal) |
PD |
peak distance (mm) |
角膜两侧未形变顶点之间的峰值距离 |
|
HC |
时间(time) |
HCDeflA T |
HCDeflA time (ms) |
角膜由原始状态到最大凹陷的时间 |
|
HC |
垂直距离(vertical) |
HCDeflA L |
HCDeflA (mm) |
角膜由原始状态到达最大凹陷的垂直距离 |
|
Other |
硬度参数(stiffness parameter) |
SSI |
Stress-strain index |
基于角膜动态形变与有限元建模的标准化硬度指数 |
|
A1 |
硬度参数(stiffness parameter) |
SP-A1 |
Stiffness parameter at first applanation (mmHg/mm) |
第一次压平时的硬度参数:(adjAP1 – bIOP) / A1 DeflAmp L |
|
HC |
硬度参数(stiffness parameter) |
SP-HC |
Stiffness parameter at highest concavity (mmHg/mm) |
最大凹陷时的硬度参数:(adjAP1 – bIOP) / (HCDeflA – A1 DeflAmp L) |
3. Corvis ST的临床应用
3.1 Corvis ST在圆锥角膜中的应用
圆锥角膜是一种渐进性的角膜变形性疾病,表现为角膜的中部逐渐变薄和突出,形成圆锥形状,从而导致屈光不正,最终可能导致严重视力障碍。据报道,角膜生物力学的改变往往先于形态学异常的出现[23],这为圆锥角膜(keratoconus, KC)的早期诊断和筛查提供了更加精确的生物力学依据。Corvis ST作为一种非接触式角膜生物力学分析仪,通过评估角膜在空气脉冲作用下的形变特性,为KC的早期筛查、分期诊断及治疗评估提供了重要的临床依据。在KC的筛查方面,多项研究发现KC患者的角膜生物力学特性与正常角膜存在显著差异。Wu等[24]研究比较了KC、亚临床KC及正常角膜的生物力学参数,并采用Fisher判别分析法建立区分KC和亚临床圆锥角膜(subclinical keratoconus, SKC)的模型。研究发现,中央角膜厚度(central corneal thickness, CCT)、最大凹陷曲率半径(highest concavity radius, HCR)、最大凹陷变形幅度(highest concavity deformation amplitude, HCDA)及第二次压平时的最大角膜速度(maximum corneal outward velocity, Vout)在区分三者方面具有较高的判别能力。此外,Choksi等[25]研究进一步证实,HCR值小于6.02 mm的患者,其鉴别KC与正常角膜的灵敏度和特异度均较高,表明该参数在KC诊断中的重要性。同时,Yang等[26]研究发现,ARTh和CBI在鉴别KC与正常角膜方面具有统计学意义,它们的约登指数值高达0.87,提示其可作为KC早期筛查的重要参数。此外,Borderie等[27]研究对比了KC和正常角膜的Corvis ST生物力学参数,发现KC组的角膜硬度显著降低,而CBI在诊断KC时的准确度为92%、灵敏度为91%,但其再现性较弱,并受到角膜厚度变化的影响。相比之下,SSI表现出更高的独立性,不受角膜厚度的显著影响,且具有较高的可重复性,因此被认为是评估角膜生物力学变化的重要参数。
在KC的治疗评估方面,Corvis ST可用于监测角膜交联术(corneal collagen cross-linking, CXL)对角膜生物力学的影响。Jabbarvand等[28]研究发现,CXL术后,患者的第一次压平长度(A1L)和速度(A1V)显著增加,而HCR、SP-A1及CBI均有所改善,表明角膜刚性增加,生物力学性能得到增强。
因此,Corvis ST在KC的诊断、早期筛查及治疗监测方面具有较高的临床价值。其提供的生物力学参数能够有效区分KC与正常角膜,还能用于评估角膜的刚性变化及治疗效果。随着人工智能与大数据分析技术的结合,Corvis ST有望进一步提高KC的筛查精度,并为个性化治疗和长期管理提供更精准的支持。
3.2 Corvis ST在屈光手术中的应用
屈光手术通过改变角膜形态来调整光线的折射,从而改善视力。常见的手术方法包括准分子激光角膜切削术(photorefractive keratectomy, PRK)、激光原位角膜磨镶术(laser-assisted in situ keratomileusis, LASIK)以及小切口角膜基质透镜取出术(small incision lenticule extraction, SMILE),这些手术广泛用于矫正近视、远视和散光。然而,由于这些手术均涉及角膜组织切削或重塑,术后角膜的生物力学稳定性成为影响手术安全性和长期视觉质量的重要因素。Lim 等[29]研究发现,角膜直径(white-to-white, WTW)对 Corvis ST 参数有重要影响,较小的WTW与较高的CBI和较低的ARTh相关,表明屈光手术评估中应考虑角膜直径对角膜生物力学的影响,以优化手术方案。术后角膜生物力学的变化是影响手术安全性及长期效果的重要因素。Younis 等[30]分析了LASIK 和 PRK 术后眼的 Corvis ST 的数据,发现 LASIK 术后 1 个月,角膜的DA、A1T、第二次压平长度(second applanation length, A2L)及HCR均发生显著变化(P<0.05),表明 LASIK 对角膜生物力学特性影响较大,而 PRK 组仅在术后 1 个月出现轻微变化,提示 PRK 对角膜生物力学影响较小。类似的,Qu 等[31]研究了 207 例接受PRK、FS-LASIK 和 SMILE 手术患者的术后角膜生物力学变化,发现术后 3 个月时,所有手术组的第一压平硬度参数(SP-A1)均明显下降,而变形幅度比率(DA Ratio)和积分反半径(integrated inverse radius, IIR)增加,表明术后角膜刚性下降。其中,FS-LASIK 组的硬度降低最明显,而 PRK 组的角膜生物力学受到的影响最小。
屈光手术会影响角膜厚度及硬度,从而影响传统眼压测量的准确性。Salouti 等[32]研究对比了 PRK 术前术后,Corvis ST 测得的生物力学校正眼压(biomechanically-corrected intraocular pressure, bIOP)与 眼反应分析仪(ocular response analyzer, ORA)测得的眼压校正值(corneal compensated intraocular pressure, IOPcc),发现两者术后的一致性较弱,但 bIOP 术后变化较小,这表明bIOP可能是PRK后IOP读数的更好选择,Corvis ST 在术后眼压监测中具有更高的稳定性。
Corvis ST 在屈光手术的术前筛查、术后监测及眼压测量校正方面具有重要临床应用价值。相比 LASIK,SMILE 对角膜生物力学的影响较小,术后角膜稳定性更高。此外,Corvis ST 计算的bIOP 术后变化较小,可为术后眼压监测提供更准确的数据。
3.3 Corvis ST在青光眼中的应用
青光眼是一种由眼内压力增高引起的视神经损伤性疾病,通常伴随视野缺损,最终可导致视力丧失。其发病机制之一与机械压力密切相关。由于眼压升高会影响角膜对压平的抵抗力[33–34],角膜生物力学特性在青光眼研究中越来越受到关注。此外,眼压瞬时升高时角膜生物力学与视神经表面的顺应性有关[35]。
角膜的生物力学参数的差异可能与青光眼的不同类型相关。Pradhan等[36]研究比较了假性剥脱性青光眼(pseudo-exfoliative glaucoma, PXG)、原发性开角型青光眼(primary open-angle glaucoma, POAG)及健康对照组的 Corvis ST 生物力学参数,发现 PXG 组的DA明显低于 POAG 组及健康对照组(P<0.000 1),提示 PXG 角膜的刚性更大。但在调整 IOP 后,3组间的生物力学参数无显著差异。Silva 等[37]研究了高眼压症(ocular hypertension, OHT)、POAG及淀粉样变性青光眼(amyloidotic glaucoma)患者的 Corvis ST 数据,发现 POAG 组SP-A1较 OHT 组更低,而 OHT 组的SSI高于 POAG 组,表明不同类型的青光眼角膜硬度可能有所差异。此外,Chou等[38]研究探讨了 Corvis ST 的生物力学因子(corvis biomechanical factor, CBiF)与原发性闭角型青光眼(primary angle-closure glaucoma, PACG)之间的关系。结果发现,PACG 组的 CBiF 显著低于正常对照组(P<0.001),提示 PACG 角膜的生物力学稳定性降低。在诊断方面,CBiF 与前房容积(anterior chamber volume, ACV)联合评估有助于提高 PACG 的诊断准确性。
角膜生物力学特性不仅影响青光眼的发生,也可能与青光眼的进展相关。Aoki 等[39]研究发现,POAG患者的视神经乳头(optic nerve head, ONH)上下不对称性与Corvis ST测量的角膜生物力学特性之间存在显著关联。其中,A2V与视神经盘边缘体积(rim volume)呈负相关(P<0.05),提示较高的 A2 速度可能与更严重的视神经损害相关。Wu 等[18]研究发现,正常眼压青光眼(normal-tension glaucoma, NTG)角膜比正常对照组和高眼压青光眼(high-tension glaucoma, HTG)角膜更易变形。NTG中较短的WEM时间与更严重的视野缺损独立相关,而HTG中较长的轴长与青光眼损伤相关。
传统的 Goldmann 压平眼压计(goldmann applanation tonometry, GAT)测量 IOP 时受角膜厚度及生物力学特性的影响,可能导致 IOP 读数的偏差。Corvis ST 提供的bIOP通过修正角膜硬度和厚度对 IOP 的影响,进而提高眼压测量的准确性。Halkiadakis等[40]研究比较了 Corvis ST 测得的 bIOP 与GAT测得的 IOP,发现bIOP较 GAT 低(平均差值 -3.1 mmHg),且不受角膜厚度影响,提示 bIOP 可能比 GAT 更适用于厚角膜或薄角膜患者的 IOP 评估。此外,Corvis ST测得的 bIOP和CCT与GAT 测得的IOP具有良好相关性。
Corvis ST 在青光眼的诊断、进展监测及眼压测量校正方面具有重要的应用价值。其生物力学参数可用于区分不同类型的青光眼,监测视神经结构变化,预测视野进展,并提高 IOP 测量的准确性。
3.4 Corvis ST在甲状腺相关眼病中的应用
甲状腺相关眼病(thyroid-associated ophthalmopathy, TAO)是一种与甲状腺功能异常相关的眼病,常表现为眼球突出、上睑退缩和眼睑肿胀等症状。重度病例可能导致视力损害。相关研究表明,TAO患者存在显著的角膜形态和生物力学改变。Zhang等[19]发现,TAO患者角膜后表面隆起、Corvis生物力学指数(corvis biomechanical index, CBI)、断层生物力学指数(tomographic and biomechanical index, TBI)和SP-A1均升高,而最小角膜厚度和DA下降,且这些指标与疾病活动度和NOSPECS评分相关,可作为TAO严重程度的生物力学参考指标。TAO患者角膜形态和生物力学变化可能与炎症的存在有关。Hwang等[41]首次提出,利用Corvis ST测量WEM来量化眶组织生物力学,发现Graves眼病患者WEM显著低于正常人群,且与眼外肌肥大呈负相关。Hsia等[42]研究表明,在TAO患者接受眶减压术后,A2L显著下降,bIOP无显著变化,但IOP-NCT显著降低,提示甲状腺眼病手术后眼部生物力学反应参数可能会发生变化,并且会影响眼压的测量。Kuebler等[43]在比较多种眼压测量设备的研究中发现,TAO患者通过Corvis ST和ORA测量所得的眼压值普遍高于正常人群,提示该疾病可能导致角膜硬度及弹性改变,从而影响眼压的准确测量。此外,Razeghinejad等[44]比较了甲状腺功能亢进无眼病组、TAO组及正常组,发现TAO组A2L和HCR增加,而DA降低,且眼突度与HCR相关。因此,Corvis ST不仅能评估角膜生物力学,还能间接反映眼眶组织的变化,因此可用于TAO患者病情监测和活动度评估。
3.5 Corvis ST在眼底疾病中的应用
3.5.1 Corvis ST 在糖尿病视网膜病变中的应用
糖尿病视网膜病变(diabetic retinopathy, DR)是糖尿病引发的视网膜病变,通常表现为视网膜微血管病变。病变早期无明显症状,但若未得到及时治疗,最终会引起严重视力丧失。有研究发现,糖尿病患者的WEM值较低,且WEM与糖化血红蛋白A1c (glycated hemoglobin A1c, HbA1c)水平呈负相关[45]。即使调整了多种因素,糖尿病患者的角膜和巩膜的变形性仍低于正常对照组,这可能影响患者眼内压测量。Ramm等[46]也进行了相似的研究,发现糖尿病患者的 A1 和 A2 时的DA显著增加,最大凹陷时间 (HC time)延长,同时HbA1c 水平越高,角膜生物力学参数变化越明显。Corvis ST的研究表明,糖尿病患者角膜生物力学行为的变化是显著的,可能与晚期糖基化终产物积累和角膜基质中胶原及蛋白多糖交联增加相关。糖尿病患者尤其是未良好控制的患者,眼压可能会偏高,这对于青光眼的评估和管理至关重要。
3.5.2 Corvis ST 在中心性浆液性脉络膜视网膜病变中的应用
中心性浆液性脉络膜视网膜病变(CSC)是一种影响黄斑区的常见视网膜疾病,主要表现为浆液性视网膜脱离,严重影响视力[47]。CSC常见于年轻男性,可能与压力过大、激素变化等因素相关。该病的病理生理机制复杂,涉及脉络膜及视网膜色素上皮功能障碍,同时可能与精神压力、炎症反应和内分泌紊乱等全身性因素相关。值得注意的是,最近的研究表明,涡静脉充血在 CSC 的发病中起着至关重要的作用[48–49] 。Aoki等[9]利用角膜可视化Scheimpflug技术(Corvis ST)发现CSC患者角膜变形能力弱于对照组。由于角膜和巩膜具有相似的细胞外基质成分,并且巩膜的生物力学特性可能会影响角膜在外力作用下的变形反应,研究假设角膜刚度可作为巩膜刚度的一个指标[6,8]。基于此假设,作者推测CSC患者的巩膜硬度增加,这可能导致涡静脉在穿出巩膜时受到的压力增大,进而引发一系列病理变化:涡静脉回流受阻、侧支吻合、脉络膜静脉淤滞、血管充血扩张、毛细血管损伤,最终累及视网膜色素上皮,成为CSC的发病机制之一。这一发现为CSC的早期诊断和治疗提供了新的生物力学视角,并为进一步探索其发病机制提供了新的思路。
3.5.3 Corvis ST 在非感染性葡萄膜炎中的应用
非感染性葡萄膜炎(non-infectious uveitis)是一种多病因的眼部炎症性疾病,主要影响葡萄膜(包括虹膜、睫状体和脉络膜)和(或)富含胶原蛋白的巩膜,可导致疼痛、组织损伤和视力障碍[50]。前段炎症可能会影响角膜结构,包括内皮细胞数量减少和中央角膜厚度增加的变化[51–52]。此外,在非感染性葡萄膜炎的房水中发现的持续升高的炎症细胞因子和趋化因子也可能对角膜组织产生潜在影响,从而改变这些患者的角膜生物力学行为[53]。Borrego-Sanz等[54]发现活动性葡萄膜炎与非活动性葡萄膜炎在PD、DA、A2V和A2L方面存在差异。葡萄膜炎疾病鉴别能力最好的生物力学参数是在最大凹陷时的曲率半径(radius, R)。未来,结合Corvis ST和OCT技术对非感染性葡萄膜炎患者进行角膜生物力学评估,可有效监测疾病活动性,为早期诊断、治疗决策和个性化治疗提供重要支持。
3.5.4 Corvis ST 在遗传性视网膜病变中的应用
遗传性视网膜病变(inherited retinal diseases, IRDs)是一组视网膜退行性病变,可能与眼前节的改变相关,但其发病率和影响尚不清楚。Marta等[55]研究发现,与对照组相比,IRD患者表现为最大偏转幅度的距离、CBI、TBI和Belin-Ambrósio偏差指数(Belin-Ambrósio deviation index, BAD-D)更大,ARTh更小。此外,在区分健康人和IRD患者方面,ARTh是最敏感的参数。与无病理变化的眼睛相比,IRD患者的角膜表现出更柔软的生物力学行为,这可能使患者更容易发生角膜扩张或青光眼。评估IRD患者的角膜生物力学特性,特别是ARTh等参数,可为早期诊断提供有力支持。此外,该方法还能够帮助识别易发生角膜扩张或青光眼的高风险患者,从而优化治疗和监测策略。
3.6 Corvis ST在全身因素相关眼病中的应用
类风湿关节炎(rheumatoid arthritis, RA)和强直性脊柱炎(ankylosing spondylitis, AS)作为自身免疫性疾病,可能通过炎症介导的组织损伤来影响角膜的生物力学特性。Ozcan等[56]的研究分析了36例RA患者、38例AS患者和36例健康对照者的Corvis ST数据,发现RA和AS组的A1V、A2V和DA均高于健康组,提示角膜的生物力学稳定性下降;RA和AS组的角膜刚性参数SP-A1低于健康组,表明角膜硬度降低,这可能影响眼压测量的准确性,并增加角膜扩张的风险。此外,疾病持续时间越长,SP-A1越低,CBI越高,提示角膜生物力学变化可能随疾病进展而加重。这一研究表明,Corvis ST可用于监测RA和AS患者的角膜生物力学变化,并可能用于预测其眼部并发症风险。
4. 结语
综上所述,Corvis ST作为一种集超高速Scheimpflug成像和非接触式眼压测量于一体的先进仪器,能够精准、直观地评估角膜动态变形中的生物力学特性,并间接反映巩膜的生物力学特性。通过提供丰富的生物力学参数,Corvis ST在圆锥角膜早期筛查与治疗评估、屈光手术方案优化与术后监测、青光眼诊断与进展评估、甲状腺相关眼病的活动情况、眼底疾病和全身免疫相关眼病中取得一定的进展,但其在不同疾病及人群中的普适性,以及特定参数诊断的准确性和特异性,仍需进一步研究和验证。随着技术的不断进步以及大数据与人工智能的深度融合,未来,Corvis ST在眼科临床实践中的应用前景十分广阔,尤其是在早期诊断和疾病监测中。通过与大数据和人工智能技术的深度融合,Corvis ST有望为个性化诊疗和病程监测提供更为科学、可靠的依据,进而提升临床医生在疾病管理中的决策效率和准确性。
声明
在本作品的准备过程中,作者使用了OpenAI的GPT-4语言模型来辅助完成文献调研。使用此工具后,作者根据需要对内容进行了审查和编辑,并对出版物的内容承担全部责任。
利益冲突
所有作者均声明不存在利益冲突。
开放获取声明
本文适用于知识共享许可协议(Creative Commons),允许第三方用户按照署名(BY)-非商业性使用(NC)-禁止演绎(ND)(CC BY-NC-ND)的方式共享,即允许第三方对本刊发表的文章进行复制、发行、展览、表演、放映、广播或通过信息网络向公众传播,但在这些过程中必须保留作者署名、仅限于非商业性目的、不得进行演绎创作。
基金
1. 广州市科技计划项目(SL2022A03J00452);广东省本科教育高等教学质量与教学改革工程建设项目(粤教高函〔2024〕9号);中山大学2023年校级本科教学质量工程项目(教务2023-394-39);白求恩·朗沐中青年眼科科研基金(BJ-LM2021014J);2024年度眼科新技术孵化基金。 This work was supported by the Science and Technology Program of Guangzhou, China (SL2022A03J00452); Higher Education Quality and Teaching Reform Construction Project for Undergraduate Education in Guangdong Province, China (〔2024〕9); Sun Yat-sen University’s 2023 University-level Undergraduate Teaching Quality Engineering Project, China (2023-394-39); the Bethune·Lumitin Research Funding for the young and middle-aged Ophthalmologists, China (BJ-LM2021014J) and Ophthalmology New Technology Incubation Fund.
参考文献
Zhai YH, Pang CJ, Ren SW, et al. Evaluation of the sensitivity and specificity of corneal visualization scheimpflug technology biomechanical index in the diagnosis of keratoconus[J]. Chin J Exp Ophthalmol, 2019, 37(7): 527-531. DOI: 10.3760/cma.j.issn.2095-0160.2019.07.007.
Wu Y, Li XL, Yang SL, et al. Examination and discriminant analysis of corneal biomechanics with CorVis ST in keratoconus and subclinical keratoconus[J]. J Peking Univ Health Sci, 2019, 51(5): 881-886. DOI: 10.19723/j.issn.1671-167X.2019.05.015.