循环肿瘤 DNA 在视网膜母细胞瘤中的研究进展
关键词
摘要
视网膜母细胞瘤(retinoblastoma, RB)是儿童最常见的原发性眼内恶性肿瘤,起源于视网膜感光前体细胞,具有高度恶性,若不及时治疗可危及生命。目前,RB 的诊断主要依赖眼底检查、超声、计算机断层扫描(computed tomography, CT)、磁共振成像(magnetic resonance imaging, MRI)等临床特征和影像学表现,预后评估则主要基于疾病分期和治疗反应。由于直接进行肿瘤活组织检查(活检)存在肿瘤扩散风险,尤其对于需保留眼球的患者,直接活检被视为绝对禁忌,因此寻找能准确反映肿瘤状态的替代标志物,对 RB 的诊断、治疗决策、疗效监测及预后评估具有重要意义。近年来,循环肿瘤 DNA(circulating tumor DNA, ctDNA)作为液体活检的关键标志物,在 RB 中的研究逐步深入。ctDNA 是肿瘤细胞凋亡或坏死时释放到体液中的 DNA 片段,携带肿瘤特异性遗传变异,可反映基因突变、拷贝数变异等分子特征。其检测方法主要包括聚合酶链反应(polymerase chain reaction, PCR)相关技术,如实时荧光定量 PCR(quantitative real-time PCR, qPCR)、 数字PCR(digital PCR, dPCR)和下一代测序(next-generation sequencing, NGS)技术,其中dPCR 检测限可达0.01%的突变频率,NGS 可全面检测遗传变异。在临床应用中,房水、血液、脑脊液等体液中的 ctDNA 均展现价值:房水 ctDNA 含量高、干扰小,能准确反映肿瘤分子特征;血液 ctDNA 便于获取,适用于晚期或转移性 RB 监测;脑脊液 ctDNA 可监测中枢神经系统转移。具体而言,ctDNA 在 RB 的早期诊断(补充传统方法不足)、预后评估[RB1 基因突变类型、肿瘤分数(tumor fraction, TFx)与预后相关]、治疗反应监测(动态变化反映疗效及耐药性)及产前诊断(非侵入性检测遗传风险)中均显示出潜在应用价值。本文综述了 ctDNA 在 RB 中的检测方法、不同体液中的研究特点、临床应用及研究进展,探讨了其面临的检测灵敏度不足、样本量小、标准化缺失等挑战,展望了技术优化、大规模临床试验及多组学结合等发展方向,旨在为 RB 的精准诊疗提供新思路。
全文
文章亮点
1. 关键发现
• 房水是视网膜母细胞瘤(retinoblastoma, RB)循环肿瘤 DNA (circulating tumor DNA, ctDNA)液体活组织检查(活检)的理想样本,检测价值显著优于血液;数字PCR (digital polymerase chain reaction, dPCR) 和 下一代测序(next-generationsequencing, NGS)是 ctDNA 核心检测技术,分别具备高灵敏度和全维度检测优势;RB1 基因突变类型、肿瘤分数(tumorfraction, TFx)等 ctDNA 分子指标与 RB 预后密切相关;房水、血液、脑脊液 ctDNA 各有专属临床应用价值,前分析变量对 ctDNA 检测结果影响显著,目前缺乏统一标准化流程。
2. 已知与发现
• 已知对RB 直接进行活检为禁忌,ctDNA 可反映肿瘤分子特征;新发现房水 ctDNA 可替代肿瘤活检完成 RB 诊断,双侧 RB 存在独立遗传起源,ctDNA 动态变化可早于传统检查监测治疗效果和耐药性,房水 ctDNA 的 TFx 可预测肿瘤复发,孕妇血浆 游离 DNA (cell-free DNA, cfDNA) 能实现 RB 的非侵入性产前诊断。
3. 意义与改变
•弥补了 RB 传统诊断、预后评估和疗效监测的不足,推动 RB 诊疗向分子精准化转变;解决了保眼患者无法进行肿瘤基因分析的临床难题,建立了 RB 分子预后指标体系;为临床选择 ctDNA 检测样本提供明确指导,也为 RB 精准诊疗的后续研究指明方向,有望提升 RB 患者的保眼率和生存率。
视网膜母细胞瘤(retinoblastoma, RB)是儿童最常见的原发性眼内恶性肿瘤,起源于视网膜感光前体细胞,具有高度恶性,若不及时治疗可危及患者生命[1-2]。目前,RB 的诊断主要依靠眼底检查、影像学检查[如超声、计算机断层扫描(computed tomography, CT)、磁共振成像(magnetic resonance imaging, MRI) 等]等临床特征和影像学特征[3],预后判断则主要依据疾病分期和对治疗的反应[4]。针对保留眼球的患者的治疗中,为避免肿瘤细胞眼外扩散,直接肿瘤活检用于基因分析和预后评估通常认为是绝对禁忌的[5]。因此,寻找能够准确反映肿瘤状态的替代标志物,对于RB的诊断、治疗决策、疗效监测及预后评估具有重要意义。
液体活检技术的出现和临床应用,为解决这一问题提供了新的解决办法,目前在临床中应用于多种肿瘤的诊断及预后监测等[6]。液体活组织检查(活检)是指通过检测血液、脑脊液、房水等体液中的肿瘤衍生成分,如循环肿瘤细胞、循环肿瘤DNA (circulating tumor DNA, ctDNA)、细胞外囊泡等,来评估肿瘤状态的一种非侵入性或微创性技术[7]。在这些肿瘤衍生成分中,ctDNA 是肿瘤细胞凋亡或坏死时释放到体液中的 DNA 片段,携带肿瘤特异性的遗传变异信息,这些 DNA 片段信息能够反映肿瘤的基因突变、拷贝数变异等分子特征[8]。近年来,ctDNA 在 RB 中的研究逐渐受到关注,多项研究表明其在 RB 的诊断、预后评估和治疗监测等方面具有潜在的应用价值[9-11],为解决 RB 临床诊疗中直接肿瘤活检禁忌、传统评估手段缺乏分子层面支撑、早期复发与耐药难以精准识别等关键问题提供了全新的分子技术路径,也为 RB 精准诊疗体系的构建奠定了重要的研究基础,本研究正是基于此背景,系统梳理 ctDNA 在 RB 中的研究进展,旨在为其临床转化与应用提供理论参考和实践指导。本文将对 ctDNA 在 RB 中的研究进展进行综述。
1. ctDNA的生物学特性
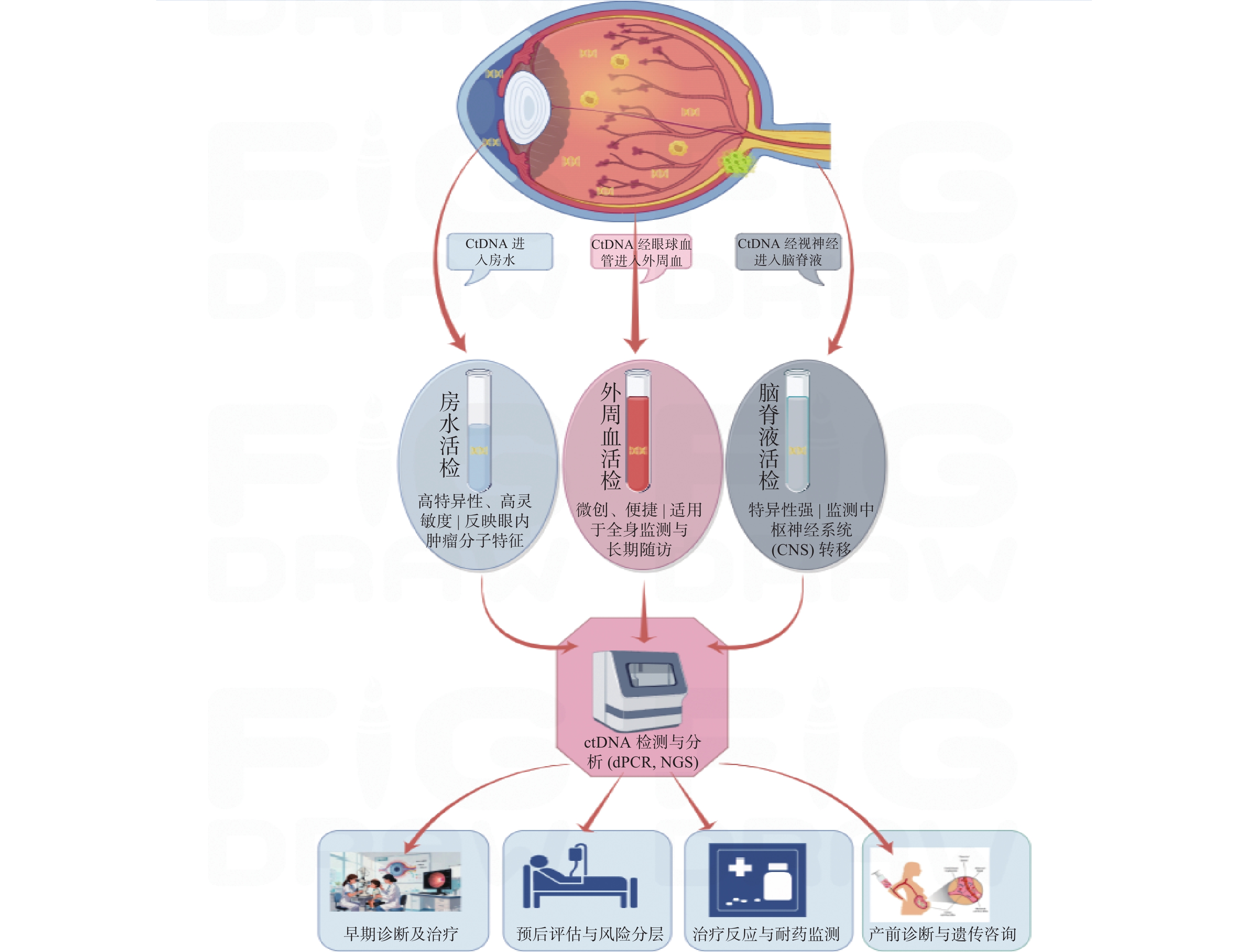
ctDNA是肿瘤细胞通过凋亡、坏死或主动分泌等机制释放到外周循环或其他体液中的双链DNA片段。其片段长度通常集中在160~200 bp,与核小体保护下的DNA降解模式一致,半衰期较短(约几分钟至2小时),这使其能近乎实时地反映肿瘤的动态变化。ctDNA的释放机制受多种因素影响,包括肿瘤类型、负荷、位置、血管生成状态、治疗干预等。在RB中,ctDNA主要携带与肿瘤发生、发展密切相关的遗传改变,如RB1基因的失活突变、体细胞拷贝数变异(somatic copy number variations, SCNAs)。这些变异信息使得ctDNA能够作为肿瘤的分子“指纹”。此外,ctDNA在体液中的水平与肿瘤负荷通常呈正相关,但在早期或眼内局限性RB中,由于肿瘤体积小且血眼屏障的存在,ctDNA水平极低,检测难度较大。深入理解ctDNA的生物学特性,对于优化其在RB中的检测策略、结果解读和临床应用至关重要(图1)。
2. ctDNA 的检测方法
ctDNA的检测是液体活检技术应用的关键环节,由于 ctDNA 在体液中的含量极低,且受正常细胞释放的游离 DNA(cell-free DNA, cfDNA)干扰,需要高灵敏度和高特异度的检测方法。目前,用于检测 ctDNA 的方法主要包括聚合酶链反应(polymerase chain reaction, PCR)相关技术、下一代测序(next-generation sequencing, NGS)技术等。
2.1 PCR 相关技术
PCR 技术是检测核酸的常用方法,其相关的衍生技术如实时荧光定量 PCR (quantitative real-time PCR, qPCR)、数字 PCR (digital PCR, dPCR)等已被用于 ctDNA 的检测。qPCR 技术通过检测 PCR 过程中荧光信号的积累来定量目标 DNA 的含量,具有操作简便、快速的特点,但其灵敏度相对较低的缺点,目前仅适用于检测已知的高频突变[12]。dPCR 技术是将样本稀释后分配到大量微小反应单元中进行 PCR 扩增,通过计数阳性反应单元的数量来实现绝对定量,此技术能够具有更高的灵敏度和特异度[13]。研究显示能够检测低至 0.01% 的突变频率,适用于微量 ctDNA 的检测[14]。目前,在 RB 研究中,dPCR 已被用于检测 RB1 基因突变等肿瘤特异性变异 [15]。
2.2 NGS 技术
NGS 技术能够同时对大量 DNA 片段进行测序,可全面检测基因组中的突变、拷贝数变异、结构变异等遗传变异,是目前 ctDNA 检测中应用最广泛的技术。根据测序范围的不同,目前NGS 技术可分为全基因组测序(whole-genome sequencing, WGS)、全外显子组测序(whole-exome sequencing, WES)和靶向测序。WGS 能够检测整个基因组的遗传变异,检测范围覆盖全基因组,具有全面性,但在使用过程中成本较高,数据量大,分析复杂;WES 主要测序基因组中的外显子区域,可检测编码区的突变,成本相对较低;靶向测序是针对特定的基因或基因区域进行测序,测序深度和灵敏度更高,此种技术更适用于检测已知的肿瘤相关基因变异[16-18]。在 RB 研究中,靶向测序常用于检测 RB1 基因的突变和SCNAs等[19-21],WGS和WES的检测则更多地用于发现新的肿瘤相关遗传变异[22- 23]。此外,为提高 ctDNA 检测的灵敏度,还可采用一些预处理方法来富集 ctDNA,比如使用基于磁珠的核酸提取方法、利用肿瘤特异性甲基化模式进行ctDNA 富集等 [8, 18]。
2.3 前分析变量与标准化
ctDNA检测的灵敏度和可重复性高度依赖于前分析变量,包括样本采集、处理、存储和DNA提取方法。例如,血液样本的采集管类型(如乙二胺四乙酸管需快速处理以防白细胞裂解释放基因组DNA,Streck管等cfDNA保护管可延长保存时间)、离心速度和时间(确保去除细胞成分获得纯cfDNA)、存储温度及时间均可影响cfDNA的完整性和浓度。房水样本体积小,需避免溶血和外部DNA污染,采集后需迅速低温保存或直接提取DNA以防止降解[24]。目前,缺乏统一的标准操作流程是导致不同研究间结果难以直接比较和临床推广的主要阻碍之一,不同实验室在样品预处理、DNA提取试剂盒选择、检测平台设置等方面存在差异,影响了检测结果的一致性和可靠性[25]。未来需建立针对RB,特别是不同体液来源样本的多中心共识指南,规范前分析流程,以提高ctDNA检测在RB诊疗中的标准化水平。
3. ctDNA 在视网膜母细胞瘤中的临床应用
3.1 诊断价值
目前关于 RB 的研究认为,早期诊断对于提高治疗效果和保留眼球至关重要[26]。相对于传统的诊断方法主要依赖临床检查和影像学特征,传统方法对于一些不典型病例,诊断难度较大,而ctDNA 作为肿瘤特异性的分子标志物,可以为 RB 的诊断提供补充信息。
多项研究表明,在 RB 患者的房水、血液等体液中可检测到 ctDNA,且其携带的遗传变异与肿瘤组织一致[20, 27]。Berry等[9]对 3 例 RB 患者的眼球房水样本进行检测,发现房水中的 cfDNA 可检测到与肿瘤组织相同的 RB1 基因突变和 SCNA,此研究提示房水内的 ctDNA 可作为 RB 的替代活检样本用于诊断。Kothari 等[5]对 10 例晚期单侧 RB 患者的血浆样本进行分析,成功在血浆 cfDNA 中检测到 RB1 基因突变,其中 9 例患者在治疗前采集的血浆样本中均检测到突变,表明血浆 ctDNA 也可用于 RB 的诊断。此外,研究还发现 ctDNA 的检测灵敏度与肿瘤负荷相关,肿瘤负荷越高,ctDNA 的检出率越高[11]。
除此之外,在一些特殊情况下,比如罕见的双侧 RB 或家族性 RB,可以对此类疾病进行ctDNA 检测,帮助明确诊断和遗传咨询[28]。Wong 等[29] 对 1 例双侧 RB 患者的双眼房水样本进行ctDNA分析,发现患者双眼具有不同的 RB1 基因突变和染色体变异,此研究提示双侧RB可能具有独立的遗传起源,为临床诊断和治疗提供了重要依据。
3.2 预后评估
在恶性肿瘤中,进行准确的预后评估对于制定个体化的治疗方案、改善患者预后具有重要的临床意义[30]。目前,针对RB 的预后情况,主要根据肿瘤的分期、侵犯范围等临床指标进行评估,但这些指标难以反映肿瘤的分子特征和生物学行为,ctDNA 携带肿瘤的分子信息,有望成为新的预后评估标志物[31]。
RB1 基因的突变是 RB 发生的关键事件,多项研究表明 RB1 基因突变的类型和频率与 RB 的预后相关[32-33]。Francis 等[11]对 5 例单侧 RB 患者的血浆样本进行检测,发现了RB1 突变的变异等位基因频率(variant allele frequency, VAF)与肿瘤的活性具有正相关关系,VAF 越高,肿瘤活性越强,预后越差,并且在经过治疗后,VAF 水平下降,提示治疗有效。Xu 等[34]通过对房水 ctDNA 的分析发现,RB1 基因突变和 SCNA 的存在与 RB 的不良预后呈正相关,尤其是染色体 6p 的增益,与肿瘤的侵袭性和眼球摘除率增加相关。除了检测 RB1 基因突变之外,ctDNA 的肿瘤分数 (tumor fraction, TFx)也被认为是重要的预后指标[35]。TFx 是指 cfDNA 中来源于肿瘤细胞的 DNA 所占的比例,它可以反映肿瘤的负荷和活性,研究表明,房水中 ctDNA 的 TFx 水平与 RB 患者的治疗反应相关,TFx 水平越高,治疗反应越差,预后越差[35]。研究者在 RB 治疗过程中发现,TFx 水平的下降提示治疗有效,并且提示 TFx 水平的升高可能预示肿瘤复发或进展[36]。
3.3 治疗反应监测
在 RB 的治疗过程中,及时监测治疗反应并调整治疗方案对于提高治疗效果、减少不良反应至关重要。传统的治疗反应监测方法主要包括临床检查和影像学检查,但这些方法往往在肿瘤出现明显变化后才能反映治疗效果,存在一定的滞后性。ctDNA 能够实时反映肿瘤的分子变化,可作为治疗反应监测的敏感指标。
多项研究表明,ctDNA 的水平和遗传变异模式在治疗过程中会发生动态变化,与治疗反应密切相关,发现随着治疗的进行,房水中 ctDNA 的数量和 TFx 水平逐渐下降,在治疗有效的患者中尤为明显[37]。当肿瘤复发时,ctDNA 的水平再次升高,这种表现可使 ctDNA 可用于监测 RB 的治疗反应和复发情况。
在 RB 的治疗中,ctDNA 还可用于预测治疗耐药性。肿瘤细胞在治疗过程中可能会发生新的基因突变,导致耐药性的产生,这些突变可通过 ctDNA 检测被早期发现[38]。有研究表明,通过对 cfDNA 的分析可检测到肿瘤细胞在治疗过程中出现的新的基因突变,这些突变与治疗耐药相关,为及时调整治疗方案提供了依据[28]。
3.4 产前诊断
通过遗传学相关研究发现,RB 具有一定的遗传性,约 40% 的 RB 患者为遗传性 RB,由生殖细胞 RB1 基因突变引起,这些患者的后代有 50% 的概率患病 [39-40]。因此,对高危胎儿进行产前诊断,可以早期发现 RB 的遗传风险,并且对于优生优育具有重要意义。
相当于传统的产前诊断方法,如羊水穿刺、绒毛膜取样等具有一定的创伤性,可能导致流产、宫内感染等并发症,液体活检技术的发展为 RB 的产前诊断提供了新的非侵入性方法[41]。研究表明,利用孕妇血浆中的 cfDNA 进行产前诊断,通过明确检测对象为 “父源 DNA” 或新发的 RB1 基因突变,cfDNA在RB的产前诊断中具有应用潜力。基于扩增子的大规模并行测序(amplicon-based massively parallel sequencing, MPS)技术,可以对孕妇血浆中的 cfDNA 进行检测,以识别父源或新发的 RB1 基因突变,此种非侵入性方法在临床探索中展现出了较高的准确性与安全性,能够为 RB 的产前风险评估提供了可行的技术路径[35]。
4. 不同体液中 ctDNA 的研究
在 RB 的研究中,房水、血液、脑脊液等体液均被用于 ctDNA 的检测,不同体液中的 ctDNA 具有不同的特点和应用价值。
4.1 房水中的 ctDNA
房水是位于眼球前房内的液体,与视网膜直接接触,RB 肿瘤细胞释放的 ctDNA 可直接进入房水,因此房水中的 ctDNA 含量相对较高,且受全身 cfDNA 的干扰较小,是 RB 液体活检的理想样本来源[42]。
房水中的 ctDNA 能够准确反映 RB 肿瘤的分子特征,Berry 等[9]对 20 例 RB 患者的房水和血液样本进行对比分析,发现房水中的 ctDNA 在检测染色体变异方面明显优于血液,通过比对房水中可检测到 11/20 样本的肿瘤相关染色体变化,而血液样本中未检测到。Kim 等[23] 通过对 68 例 RB 患者房水 ctDNA 的全基因组 SCNA 分析发现,染色体 6p 的增益与肿瘤的侵袭性和不良预后相关,进一步证实了房水 ctDNA 在 RB 研究中的价值。
随着手术技术的发展,房水的采集方法也在不断优化,相关研究描述了一种安全的房水采集方法,通过角膜缘穿刺抽取 0.1~0.15 mL 房水,未发现肿瘤扩散等并发症[43]。Kim等[23]进一步改进了采集方法,使用 32G 针头通过透明角膜穿刺抽取房水,提高了采集的安全性和准确性(图2)。这些方法的建立,可以为房水 ctDNA 的研究和临床应用提供了保障,减少患眼因穿刺引起的损伤。
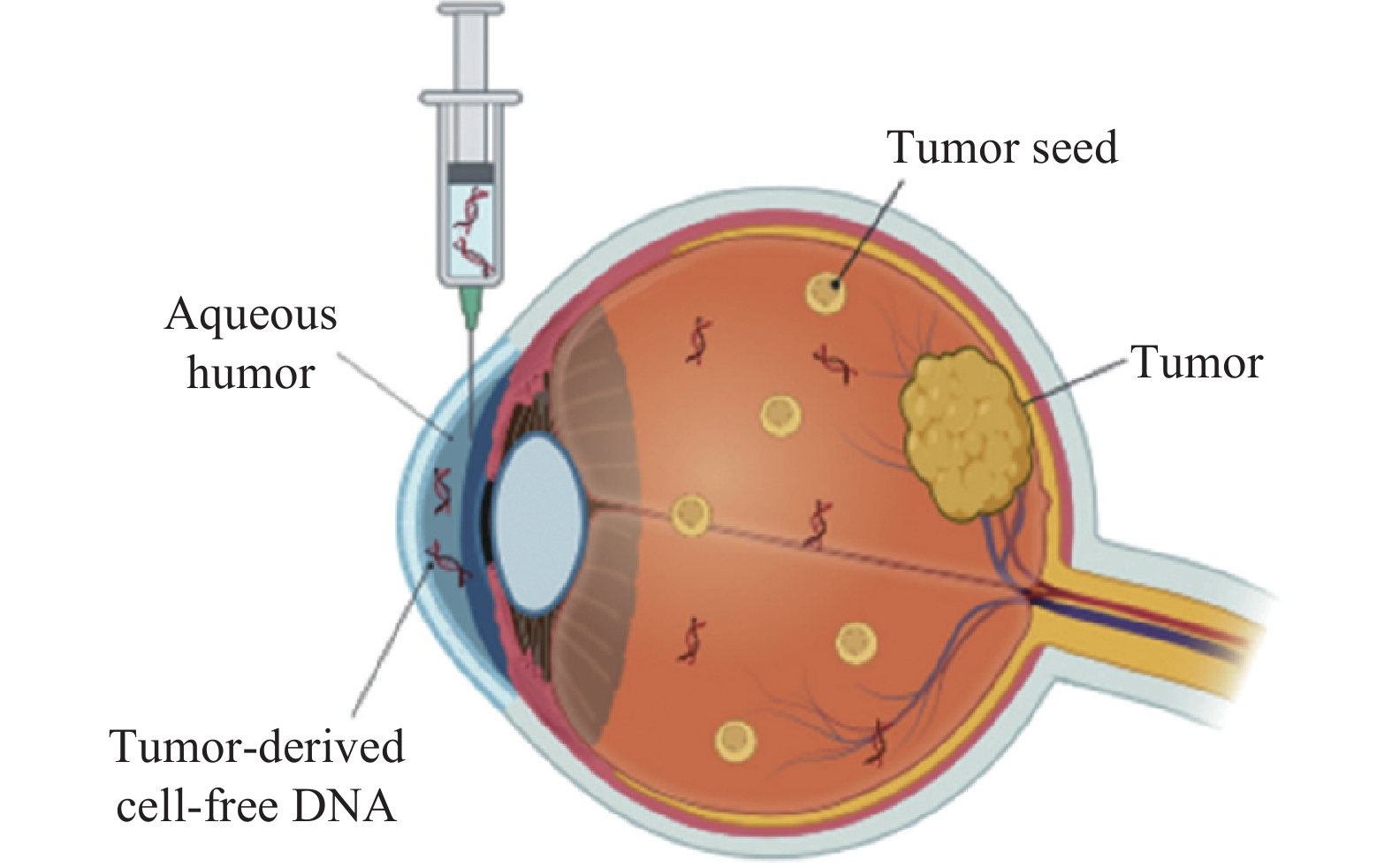
房水中存在肿瘤来源的cfDNA。通过 32G 针头进行简单的角膜穿刺术,可收集约 100 µL 房水[44]。
Tumor-derived cfDNA exists in aqueous humor. Approximately 100 µL of aqueous humor can be collected via a simple corneal paracentesis using a 32-gauge needle[44].
4.2 血液中的 ctDNA
在临床当中,部分患者无法接受房水采样,通常使用血液样本检测。血液样本易于获取,且可反复采集,是液体活检中最常用的样本来源。虽然血液中 ctDNA 的含量相对较低,受正常 cfDNA 的干扰较大,但随着检测技术的进步,血液 ctDNA 在 RB 中的应用也逐渐受到关注。
Kothari等[5]的研究表明,在晚期单侧 RB 患者的血浆中可检测到 RB1 基因突变,且突变的 VAF 与肿瘤的转移风险相关,VAF 越高,转移风险越大。Francis等[11]对 5 例单侧 RB 患者的血浆样本进行检测,发现 RB1 突变的 VAF 在动脉内化疗后明显下降,提示血液 ctDNA 可用于监测 RB 的治疗反应。
然而和房水相比,血液ctDNA在RB中的检测灵敏度较低。Berry等[9]的研究发现,房水中的ctDNA在检测肿瘤相关染色体变化方面明显优于血液,这可能是由于血液中的ctDNA经过全身循环稀释和清除等因素的影响,减少了血液ctDNA的含量。因此,血液 ctDNA 在 RB 中的应用,可能更适用于晚期或转移性 RB 的监测,对于早期 RB 左右有一定局限性。
4.3 脑脊液中的 ctDNA
脑脊液是包围中枢神经系统的液体,RB 肿瘤细胞可侵犯中枢神经系统,释放 ctDNA 到脑脊液中,因此脑脊液中的 ctDNA 可用于监测 RB 的中枢神经系统转移[45]。
Laurent等[46]对 具有高危病理特征的非转移性 RB 患儿的脑脊液和骨髓样本进行检测,发现脑脊液中 GD2 合成酶 mRNA 和视网膜锥杆同源盒(cone-rod homeobox, CRX) mRNA 的表达与微小转移相关,其中 2 例脑脊液中 GD2 合成酶 mRNA 阳性的患儿出现了转移性复发。Demet 等[21]通过对脑脊液中 RB1 基因突变的检测,成功发现了转移性 RB 患者的微小残留病灶,提示脑脊液 ctDNA 可用于监测 RB 的中枢神经系统转移。
4.4 不同体液来源ctDNA检测的临床选择
不同体液的ctDNA检测在RB诊疗中各有其优势和局限性,临床选择需综合考量检测目的、肿瘤分期、操作风险与可行性。
4.4.1 房水
它是眼内RB分子信息获取的首选来源,具有灵敏度高、特异性强的特点,主要适应于眼内RB的精确诊断、分子分型、预后判断和治疗反应监测,因其有创性,需权衡获益与风险,禁忌证包括活动性眼内炎、严重角膜病变等[20]。
4.4.2 血液
这是最便于获取和重复采样的样本,适用于RB的全身性疾病监测,特别是晚期、转移性或无法进行房水采样病例的疗效评估、复发监测和胚系突变筛查,其微创特性使其适用人群广泛,禁忌证极少[47]。
4.4.3 脑脊液
其是监测中枢神经系统转移的特异性窗口,仅适用于疑似或确诊CNS转移的RB患者,由于其操作有创性及较高风险,必须严格掌握适应证[48]。
在实际临床工作中,可根据具体情况联合应用不同来源的体液标本。例如,利用房水进行眼内肿瘤的精准评估,同时利用血液进行全身性监测和长期随访。未来,随着技术发展和对不同体液ctDNA动力学理解的深入,其选择策略将更加精准和个体化。
5. 挑战与展望
5.1 面临的挑战
通过目前相关的研究, ctDNA 在 RB 中的研究取得了一定的进展,但仍然面临诸多困境。ctDNA 在体液中的含量极低,尤其是在早期 RB 患者中,检测难度较大,需要进一步提高检测技术的灵敏度和特异度。由于 RB 发病率较低,所以目前的研究样本量较少,且大多为回顾性研究,缺乏大规模的前瞻性临床试验来验证 ctDNA 的临床应用价值。除此之外,ctDNA 检测的标准化问题也需要进行统一,不同的检测方法、样本处理方式可能导致检测结果的差异,影响其临床应用。
5.2 未来展望
随着目前检测技术的不断进步和研究的深入,在未来针对ctDNA 在 RB 中的应用前景十分广阔。开发更灵敏、更特异的 ctDNA 检测技术,将提高早期 RB 的检出率。开展大规模的前瞻性临床试验,可验证 ctDNA 作为诊断、预后和治疗监测标志物的临床价值。目前多组学数据是研究热点,可通过结合多组学数据(如基因组学、转录组学、蛋白质组学、时空组学等),深入探讨 ctDNA 与 RB 发生、发展和预后的关系,为 RB 的精准治疗提供依据。通过进一步探索 ctDNA 在 RB 个体化治疗中的应用,运用 ctDNA 的分子特征指导治疗方案的选择和调整。随着液体活检技术的普及,检测成本的降低,ctDNA 检测有望成为 RB 临床诊疗的常规手段,实现 RB 的早期诊断、精准预后和个体化治疗,提高患者的生存率和生活质量。
6. 结论
ctDNA 作为一种新型的肿瘤分子标志物,在 RB 的诊断、预后评估、治疗反应监测和产前诊断等方面具有重要的潜在应用价值。通过比较房水、血液、脑脊液等不同体液中的 ctDNA 特征,房水中的 ctDNA 在 RB 的研究中表现出较高的灵敏度和特异度,是理想的样本来源。尽管目前 ctDNA 的检测仍面临诸多挑战,但随着技术的进步和研究的深入,在今后针对 RB 临床诊疗中的应用将日益广泛,将为 RB 的精准医疗提供新的思路和方法。
声明
在本作品的准备过程中,作者使用了豆包(生成式人工智能工具)来协助进行部分文献查询、整理及协助修订参考文献等工作。使用该工具后,作者已对其生成的相关内容进行了严格审查、核对与编辑,确保文献信息的准确性、完整性及与本文研究主题的相关性,并对本论文的全部内容承担责任。
利益冲突
所有作者均声明不存在利益冲突。
开放获取声明
本文适用于知识共享许可协议(Creative Commons),允许第三方用户按照署名(BY)-非商业性使用(NC)-禁止演绎(ND)(CC BY-NC-ND)的方式共享,即允许第三方对本刊发表的文章进行复制、发行、展览、表演、放映、广播或通过信息网络向公众传播,但在这些过程中必须保留作者署名、仅限于非商业性目的、不得进行演绎创作。