激光所致黄斑损伤的机制和临床表现
关键词
摘要
激光所致黄斑损伤是眼科领域日益突出的公共卫生问题,其机制涉及光化学、光热和光机械效应。临床表现以视力下降、中心暗点及视物模糊为主,成人多及时就诊,儿童常因隐瞒而延误治疗。眼底检查可见视网膜色素上皮(retinal pigment epithelium, RPE)层非特异性改变,黄斑区黄色或灰色病灶,严重者出现全层裂孔、视网膜前出血或脉络膜新生血管(choroidal neovascularization, CNV)。辅助检查技术中,光学相干断层扫描(optical coherence tomography, OCT)可精准定位损伤层次,急性期显示外层致密高反射带,慢性期可见光感受器再生或瘢痕;荧光素眼底血管造影(fluorescein fundus angiography, FFA)与吲哚菁绿血管造影(indocyanine green angiography, ICGA)联合评估血管渗漏及脉络膜新生血管;光学相干断层扫描血管成像(optical coherence tomography angiography, OCTA)提供三维血管无创诊断;眼底自发荧光(fundus autofluorescence, FAF)量化损伤范围,视网膜电图(electroretinography, ERG)检测视锥细胞功能异常,自适应光学扫描激光检眼镜(adaptive optics scanning laser ophthalmoscopy, AO-SLO)及近红外反射(near-infrared reflectance, NIR)成像揭示光感受器形态学改变。OCT联合其他辅助检查的多模态影像可提高确诊率。治疗策略尚无共识,药物保守治疗包括糖皮质激素抑制炎症、叶黄素抗氧化及曲安奈德局部注射减轻水肿;手术干预针对全层裂孔(玻璃体切割联合内界膜剥离)、黄斑部玻璃体后皮质下及内界膜下出血(YAG激光)及继发CNV(血管内皮生长因子药物玻璃体腔内注射)。然而,治疗方案在给药时机、剂量及长期疗效方面存在争议,需大样本临床研究验证。防控需多维度推进:加强公众教育,严格市场监管以杜绝高危激光产品流通;推动多中心研究优化治疗窗与治疗方案。本文对黄斑激光损伤的流行病学特征、临床表现、诊断及治疗的基础理论研究进展进行综述,旨在为激光所致黄斑损伤的预防、诊断、治疗提供参考。
全文
文章亮点
1 关键发现
• 本文提出并强调采用“光学相干断层扫描(optical coherence tomography, OCT)联合多模态影像”的综合诊断策略,以提高激光黄斑损伤确诊率。本文系统梳理了OCT、光学相干断层扫描血管成像(optical coherence tomography angiography,OCTA)、荧光素眼底血管造影(fluorescein fundus angiography, FFA)与吲哚菁绿血管造影(indocyanine green angiography,ICGA)、视网膜电图(electroretinography, ERG)及自适应光学扫描激光检眼镜(adaptive optics scanning laser ophthalmoscopy,AO-SLO)等多种技术在损伤分期、层次定位、血管评估及功能形态学检测中的互补价值。 系统综述当前治疗“尚无共识”的现状,综述保守治疗(如糖皮质激素、抗血管内皮生长因子)与手术干预(针对裂孔、出血等)的具体应用场景及争议点(如给药时机、剂量、长期疗效),为未来临床研究指明了方向。 特别指出儿童患者因“隐瞒病史”导致延迟诊断的临床特点,并揭示了从“公众教育”到“市场监管”的综合性防控短板,将临床问题延伸至公共卫生管理层面。
2 已知与发现
• 梳理了激光损伤的光化学、光热、光机械效应机制;黄斑损伤的典型症状(视力下降、中心暗点)及部分眼底表现(如RPE改变、黄斑病灶);OCT、FFA等传统检查的基本应用。 系统整合并强调了OCTA、FFA、AO-SLO等较新技术在诊断中的具体角色与联合应用路径,构建了清晰的现代影像诊断逻辑框架。点明了成人与儿童在就医行为上的关键差异,对早期识别高危儿童患者具有直接警示意义。
3 意义与改变
• 采用“OCT联合多模态影像”的综合诊断策略,为眼科医生,特别是眼外伤、眼底病专科医生,提供了一种即时、全面的临床决策参考。从如何选择并解读多模态检查以明确诊断,到如何根据损伤类型和分期选择治疗策略并理解其局限性,具有直接的指导价值。 将“防控”提升至与“诊疗”同等重要的位置,提出的加强公众(尤其家长)教育、严格市场监管等建议,为相关部门制定干预政策、减少此类可预防性眼外伤提供了明确的策略思路和理论依据。
暴露于强光源(包括阳光、手术显微镜照明和激光)后,由于光辐射被人眼的折射结构聚焦和聚集到视网膜中,辐照度被放大了5~6倍,使视网膜成为最容易受到激光伤害的组织,可能会发生黄斑损伤和视力丧失[1-3] 。由于高功率手持激光设备和激光笔的广泛普及,导致儿童和成人激光相关黄斑损伤的报告越来越多[3-8]。黄斑激光损伤的临床表现多种多样,再加上儿童容易隐瞒激光暴露史,使得及时诊断该病颇具挑战性[9-17] 随着近年来相关报道越来越多,目前已发现某些特征性影像学表现及眼部体征,此疾病应得到重视。
1 激光损伤机制
依据美国食品药品管理局 (Food and Drug Administration, FDA) 和国际电工委员会 (International Electrotechnical Commission, IEC) 制定的激光的分类:当眼睛暴露于Ⅲ类和Ⅳ类激光(功率>1 mW)是有潜在危险[18]。低功率激光器定义为功率输出小于 5 mW,市面上有出售,可用作激光指示器,被标注为“安全”,但有证据表明,即使是这些设备也会引起严重的视网膜损伤,特别是对于那些无意中注视光束的儿童[19-21]。除了功率输出外,波长也是决定持续激光暴露后组织损伤程度的另一个特性。波长越短,传递的能量越大,受伤风险越高[22]。
激光主要通过其化学、热、机械等效应作用于视网膜,从而损伤视网膜色素上皮(retinal pigment epithelium, RPE)细胞、光感受器细胞和双极细胞[23]。光化学效应指低能量的光作用于视网膜上超过10 s,一般不引起眼底改变[22]。光热效应指在几秒内视网膜组织吸收一定能量的激光,使局部组织的蛋白质发生变性、凝固[24]。光机械效应指视网膜组织在极短时间内接收了极强能量的光,瞬间发生变化[25]。长波长红色激光会对眼睛造成热损伤。绿色激光导致能量以532 nm的波长传递到RPE细胞中的黑色素,从而导致RPE层和视网膜外层损伤。如果观察到波长较短的绿色激光或较短的蓝色激光,更多的能量会传递到眼睛,造成光化学损伤[19]。
组织学改变可分为3个时期:急性期、扩展期、重塑期[26]。激光能量首先作用于RPE细胞及外层视网膜,导致光感受器外节断裂、椭圆体带(ellipsoid zone, EZ)和嵌合体带(interdigitation zone, IZ)连续性中断。在动物模型中,观察到激光可诱导视网膜外节溶解和光感受器细胞核固缩[27]。激光损伤后24 h可观察到视网膜中灰白色的病变[26, 28]。Müller细胞迅速反应性增生,表现为胶质纤维酸性蛋白和波形蛋白表达上调,胞体肥大并向损伤区迁移,形成胶质瘢痕雏形[27]。激光照射后第3天,损伤扩散停止,相邻细胞开始填充并重塑病变区域[29] 。幸存RPE细胞迁移覆盖损伤区,但无法完全恢复正常极性排列。光感受器外节再生受限,光学相干断层扫描(optical coherence tomography, OCT)显示椭圆体带永久性缺损区,对应组织学可见外核层厚度减少50%以上[30-31]轻度损伤中,外层视网膜和RPE层可能存在局灶性缺陷;随着损伤的加重,可能会出现外层视网膜萎缩和脉络膜毛细血管缺血[32]。血管阻塞会导致脂质过氧化,进一步加重视网膜损伤[33]。
2 流行病学特征
我国首次激光所致黄斑损伤的病例报道于1976年[34],在2010年前激光所致眼外伤属于罕见病例,主要原因是工作时使用工业激光设备不规范。近15年病例报道显著增加,患者多为儿童,当暴露发生在儿童和青少年(年龄≤18 岁)身上时,它们通常与玩耍行为有关[3]。男性患病率远高于女性,成人患病率较低,但多数为工伤,视力影响大,且预后差[3]。随着医美行业的蓬勃发展,则有因医美激光操作不当引起的误伤[35-36]。我国报道的病例均是意外他伤或自伤情况,国外有故意自伤的案例[37],多发生于有精神疾病患者中[3]。值得注意的是,在故意自伤病例中,患者在初次病史采集时通常会否认有自残行为[3]。
3 临床特征
3.1 临床表现
大部分患者主要为单眼受损,并且单眼和双眼受损患者视力或临床表现相近[3]。患者多表现为视力下降、中心暗点、视野缺损、视力模糊为主诉前来就诊[38]。成人就诊较快,儿童容易隐瞒病情,直到家长发现患儿视力受影响时,就诊偏晚[3]。
3.2 眼部体征
损伤早期多为非特异性RPE层改变、黄斑区独特黄色或灰色病变[3, 19](图1)。少见的体征表现包括视网膜外层条纹病变、全层黄斑裂孔(图2)、黄斑瘢痕、脉络膜新生血管(图3)、卵黄状黄斑病变(图4)、白点综合征和中心凹周围玻璃膜疣样沉积物[39-43];较罕见体征有浆液性色素上皮脱离[16]、各种各样的黄斑区出血、内界膜下出血,视网膜下出血 、脉络膜视网膜出血[44-46] 。Bhavsar等[3]回顾性分析了171例患者,结果发现就诊时的平均视力(visual acuity,VA)为 20/50。其中13眼(7.1%)视力不佳,为指数或手动。严重的视力损伤主要发生在伴有视网膜前出血、全层黄斑裂孔和脉络膜新生血管的眼睛中。相比之下,眼前段异常(平均VA 20/25)或有限的后段损伤,如局灶性RPE变化(平均VA 30/32)、卵黄样黄斑病变(平均VA 50/32)和灰色或黄色视网膜外病变(平均VA20/40)的视力相对较好。
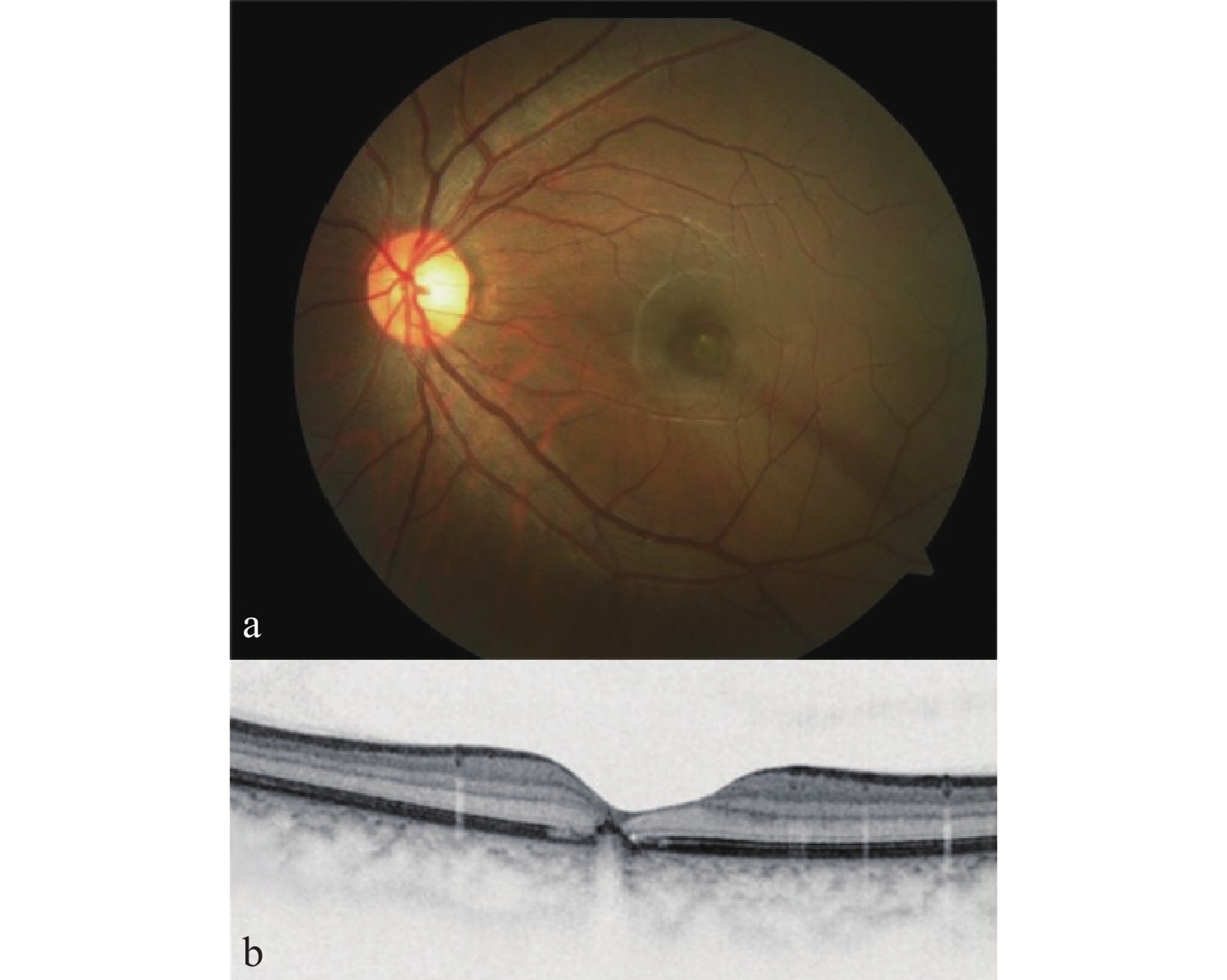
(a)眼底照相显示黄斑区灰色病变; (b) OCT显示黄斑区RPE层连续性中断。
(a) Fundus photography shows a gray lesion in the macular area; (b) OCT reveals a discontinuity of the RPE layer in the macular area.
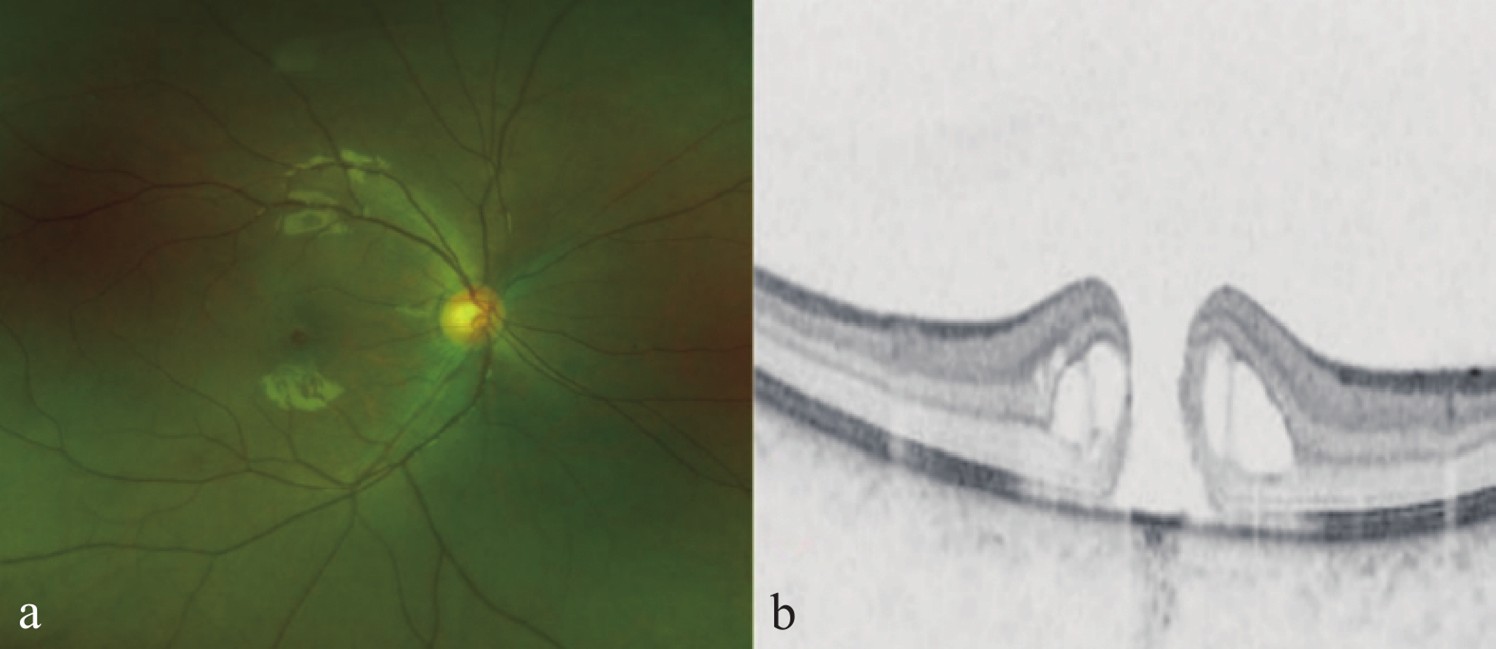
(a)眼底照相显示黄斑中心圆形全层组织缺损底部呈暗红色;(b)OCT提示激光损伤后黄斑区全层裂孔合并层间水肿。
(a) Fundus photography reveals a circular, full-thickness tissue defect at the fovea, with a dark red base; (b) OCT indicates a full-thickness macular hole accompanied by intraretinal edema in the macular area following laser injury.
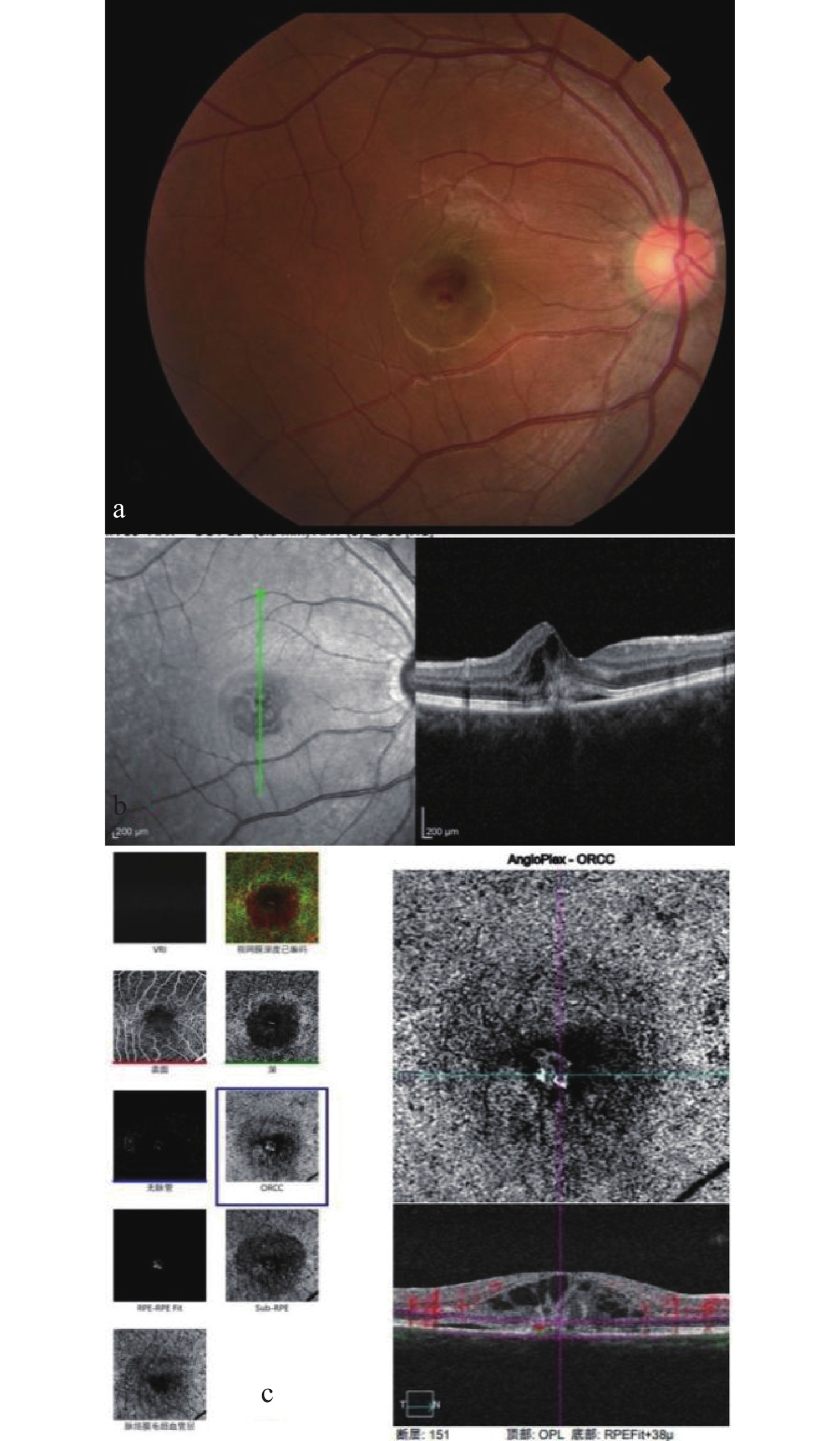
(a)眼底照相显示黄斑区红色出血灶(脉络膜新生血管);(b) OCT显示黄斑区局部RPE层隆起,伴神经上皮层浅脱离及层间水肿;(c) OCT-A显示黄斑区外层视网膜至脉络膜毛细血管层见血流信号。
(a) Fundus photography shows a red hemorrhagic focus (choroidal neovascularization) at the macular area; (b) OCT demonstrates localized elevation of the RPE layer in the macula, accompanied by shallow detachment of the neurosensory retina and intraretinal edema; (c) OCT-A reveals blood flow signals from the outer retina to the choriocapillaris layer in the macular region.
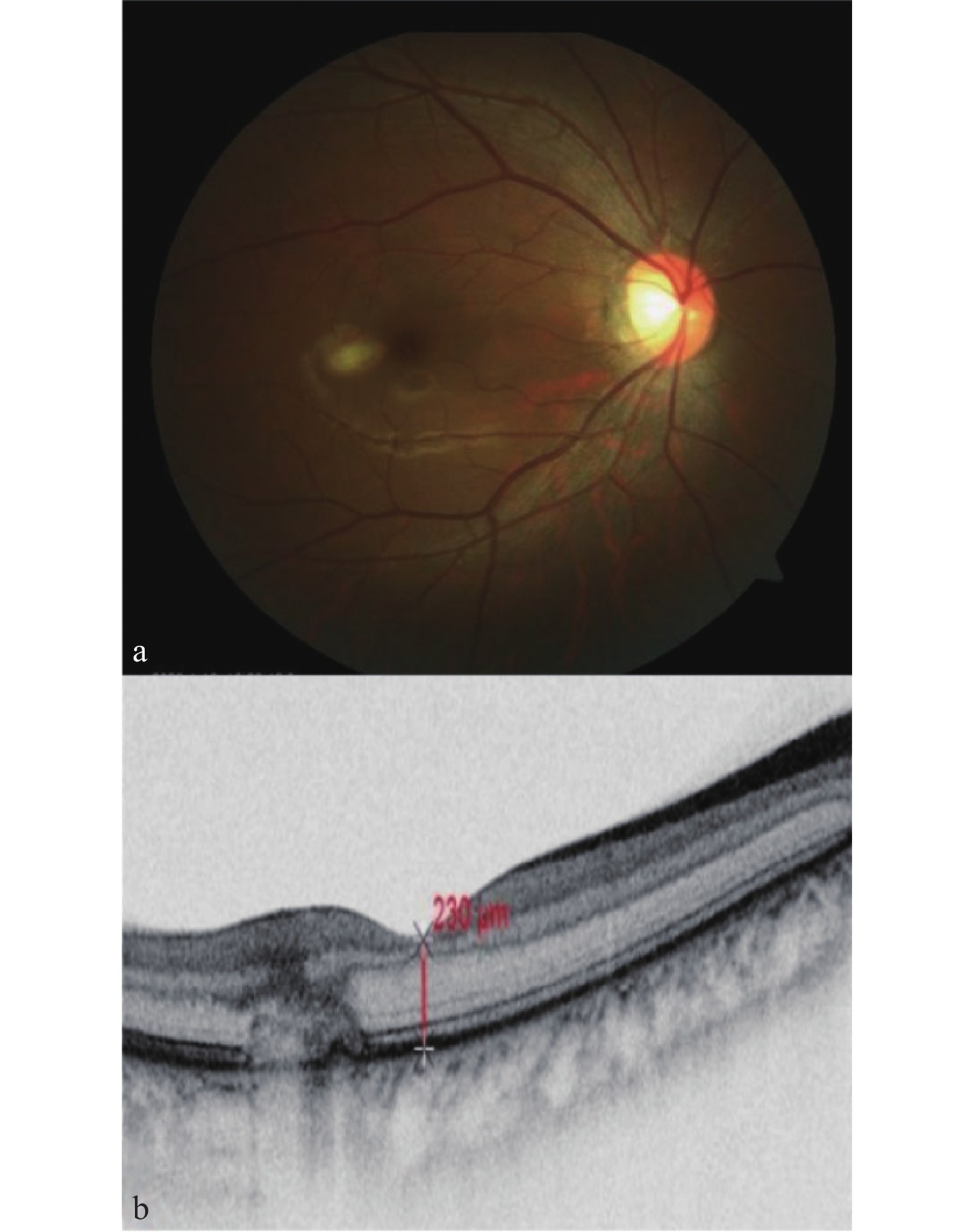
(a)眼底照相显示黄斑区颞侧出现黄白色卵黄状病灶;(b) OCT显示黄斑区颞侧RPE层隆起伴层间结构中断。
(a) Fundus photography shows a yellow-white, yolk-like lesion in the temporal macular area; (b) OCT reveals elevation of the RPE layer with disruption of the inner architecture in the temporal macular region.
3.3 辅助检查
3.3.1 结构成像与分层分析
3.3.1.1 光学相干断层扫描
几乎所有患者在初次就诊时OCT 检查存在异常表现,所以OCT检查在激光所致黄斑损伤的诊断及随访中起着重要的作用,并可联合其他检查形成多模态影像,协助诊治。
OCT检查可通过高分辨率的横断面成像,明确激光损伤累及的视网膜层次,Raoof 等[8]根据OCT影像学表现,将急性激光所致黄斑区损伤分为3个程度:轻度损伤,指损伤局限在黄斑区、间断的外层视网膜及RPE层紊乱,OCT表现为EZ、光感受器外节的局限性缺损,OCT表现为外核层破坏或光感受器内节/外节(IS/OS)断裂[47](图5a)。在部分病例中,即使眼底检查未见明显病变,OCT亦可检测到外丛状层的微结构异常 [48]。中度损伤:指非局限性的视网膜外层受损,OCT表现为RPE层低隆起(图5b)、萎缩或Bruch膜破裂[49]、板层黄斑裂孔(图5c)。重度损伤,指黄斑中心凹下全层视网膜结构破坏,常伴有内层视网膜受累和严重并发症,OCT表现为黄斑中心凹下外层视网膜结构缺损,伴内层视网膜高反射(提示出血)[50]、RPE层高隆起、全层黄斑孔合并周围视网膜水肿(图2b)、局部浆液性脱离(图5d)。在严重病例中,OCT可显示黄斑区直径150~350 μm的深层黄橙色病灶[51]。
OCT可监测病程并判断预后。急性期特征:损伤后即刻表现为视网膜外层致密高反射光带(沿Henle纤维分布的曲线状)(图5e)(随后2周内逐渐消退)[21, 48]。慢性期变化:通过连续随访可观察部分光感受器层再生(如EZ恢复)[52],或形成永久性视网膜外层瘢痕[53]。并发症:如OCT可见视网膜下高反射团块伴积液为继发性脉络膜新生血管(choroidal neovascularization, CNV)[38](图5f),或激光瘢痕周围脉络膜增厚[54]。
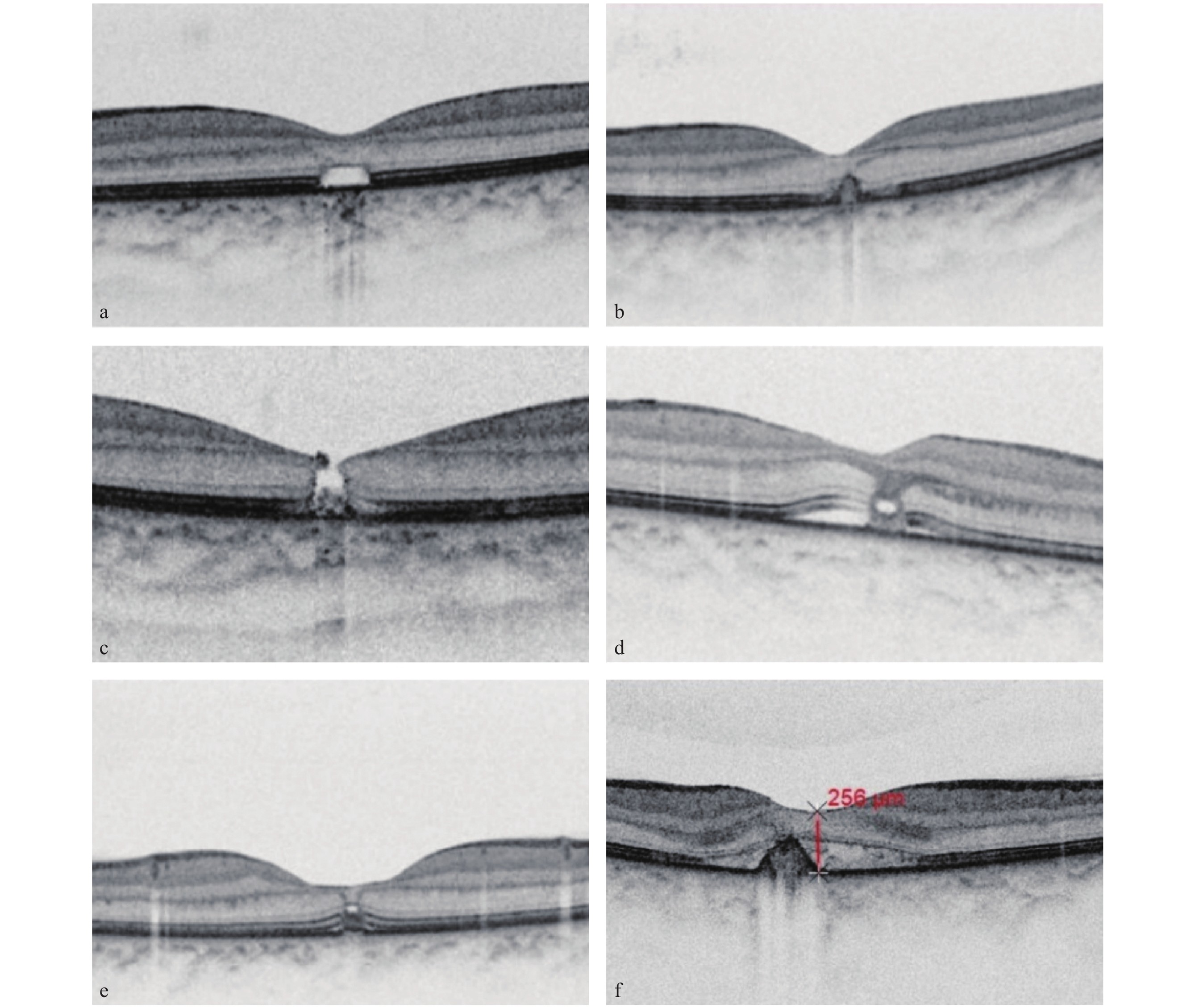
(a) OCT提示激光损伤后光感受器内节/外节(IS/OS)断裂;(b) OCT提示激光损伤后RPE层低隆起;(c) OCT提示激光损伤后黄斑区板层裂孔;(d) OCT提示激光损伤后黄斑区局部浆液性脱离;(e) OCT提示激光损伤后黄斑区高反射结构从中央凹中心沿轨迹径向外延伸;(f) OCT提示激光损伤后黄斑区高反射团块伴局部浆液性脱离。
(a) OCT demonstrates disruption of the inner segment/outer segment (IS/OS) following laser-induced injury; (b) OCT shows slight elevation of the RPE layer after laser injury; (c) OCT reveals a lamellar hole in the macular area secondary to laser injury; (d) OCT indicates a localized serous detachment in the macular region following laser injury; (e) OCT shows a hyperreflective structure extending radially along the trajectory from the foveal center after laser injury; (f) OCT demonstrates a hyperreflective mass accompanied by focal serous detachment in the macular area after laser injury.
3.3.1.2 自适应光学扫描激光检眼镜
自适应光学扫描激光检眼镜(adaptive optics scanning laser ophthalmoscopy, AO-SLO)检查是一种新的非侵入性的高分辨率视网膜成像技术,可用于评估横向分辨率约为2~3 μm的视网膜视锥光感受器[55-56]。近年来,这项技术已被广泛用于各种视网膜病变的观察,如色素性视网膜炎、视网膜脱离和年龄相关的黄斑变性。Fang等[57]通过AO-SLO检查对13例激光所致黄斑损伤的患者进行了视锥细胞的形态变化分析。结果发现,患眼显示视锥密度显著降低,细胞分散性增加,细胞规则性显著降低,且EZ完整性可以反映视锥细胞密度。既往散在的病例报告也显示明显的视网膜中央凹视锥细胞缺失和不规则分布的低反射信号[10, 56,58]。为研究激光黄斑损伤的机制、治疗效果及安全性提供了新的研究方向。
3.3.1.3 近红外反射成像
近红外反射(near-infrared reflectance, NIR)成像是一种新兴的眼底成像技术,近年在视网膜疾病的研究和临床应用中崭露头角。在其图像中血管、视盘和中央凹由于含水量、血液成分及黄斑色素浓度较高呈现高反射,而周边眼底则因细胞、血液、水、黑色素、色素多种物质的混合物而呈现中等反射[59]。适用于观察外层视网膜、RPE层和脉络膜的异常,在激光黄斑损伤中可表现为“树枝状”辐射的高反射性黄斑病变、黄色/灰色黄斑病变、线性高反射性病变、瘢痕[3, 59]。
3.3.2 血管成像与血流评估
3.3.2.1 荧光素眼底血管造影术和吲哚菁绿血管造影
荧光素眼底血管造影术(fluorescein fundus angiography, FFA)常用于观察和评估激光导致的眼底血管相关病变的形态和位置[60]。急性病变最常见的 FFA表现是早期强荧光,晚期荧光着染。其他的表现还有:透见荧光、色素沉积导致的遮蔽荧光、与脉络膜新生血管相关的表现[3]。虽然一些病例可能在 FFA 上显示局部视网膜血管染色,但没有证据证实这是血管炎的改变。个别进行吲哚菁血管造影检查的患者,可发现活动性脉络膜新生血管[3]。
3.3.2.2 光学相干断层扫描血管成像
光学相干断层扫描血管成像(optical coherence tomography angiography, OCTA)通过提供视网膜的三维血管成像,用于研究视网膜新生血管结构和形态,对于怀疑引起视网膜、脉络膜血管病变的患者有着重要的意义。OCTA检查提供了一种非侵入性成像模式,降低了患儿行FFA检查的风险。Veronese 等[61]发现,一例14 岁激光黄斑损伤的患者在 OCTA 上显示出了1个黄色的血管复合体,表现为1条大的中央供血血管从病变的一侧呈放射状散开(“树状”模式)。该病例的 OCT 显示,RPE 层受到严重热损伤或 RPE层破坏,与 2 型 CNV 有关。 Tomasso 等[62]发现,在OCT 上两个局部脉络膜毛细血管血流信号减弱区域,相对应在OCTA 上表现为脉络膜毛细血管减少或上方覆盖高反射物质。 Alsulaiman 等[44]报道了一例激光导致视网膜中心凹周围毛细血管的损伤,在OCTA 上表现为视网膜中心凹无血管区扩大和延伸。
3.3.3 代谢与功能评估
3.3.3.1 眼底自发荧光
眼底自发荧光(fundus autofluorescence, FAF)检查可以用于评估激光所致黄斑损伤的程度和监测损伤的进展。在激光损伤后,FAF可以显示出损伤区域的荧光变化,这些变化反映了RPE细胞和光感受器细胞的损伤情况[16]。通过比较损伤前后的FAF图像,医生可以评估损伤的范围和严重程度,并监测随时间的恢复过程,有助于区分激光损伤与其他黄斑病变。部分受伤患者眼底自发荧光检查可观察到阳性体征,多表现为高自发荧光病变。少见表现有因RPE层破裂或丢失表现为低自发荧光。其他罕见表现有高自发荧光条纹、低自发荧光点、高自发荧光边界的低自发荧光病变[3]。FAF检查常与其他影像学检查联合使用,FAF提供关于RPE细胞和光感受器功能的间接信息,这种联合OCT检查的多模态影像应用有助于更准确地诊断和理解激光损伤的影响。
3.3.3.2 视网膜电图检查
视网膜电图检查(electroretinography, ERG)提供了一种非侵入性、客观的视网膜功能测量方法。ERG通过测量各种视网膜细胞(包括光感受器、双极细胞和神经节细胞)的电反应来客观评估视网膜健康状况。Bhavsar等[3]的研究报道中发现,虽然所有受试眼睛的全视野(full-field ERG,ffERG)都正常,但在接受多焦点视网膜电图(multifocal Electroretinogram,mfERG)检查的部分患眼中检测到视锥细胞振幅降低。Torp-Pedersen 等[20]的研究同样发现 2 只被激光照射的眼睛的 mfERG 中央视网膜视锥细胞反应降低。 Torp-Pedersen 等[20]报道了一名公交车司机,该司机因盯着后视镜反射的光束而导致视网膜光损伤,其视觉诱皮层电位(visual evoked cortical potentials,VEP)检查正常,然而mfERG 显示暴露的眼睛出现旁中心局灶性紊乱,总峰值发生改变。 Liang 等[63]也同样发现一名 29 岁男性在酒吧受到蓝色激光照射后,mfERG 峰值降低。
4 治疗
尽管激光引起的黄斑损伤对视力的威胁很大,但目前国内外对于其治疗尚无统一共识。主要分为口服药物保守治疗和手术治疗。
4.1 药物保守治疗
目前的经验用药会给予患者局部或全身使用皮质类固醇药物[5, 13, 16, 64],此类药物可以减少炎症因子释放、抑制了RPE细胞增殖。既往病例报告了1例25岁患者在激光黄斑损伤后接受口服皮质类固醇治疗的治疗,1周后出现了黄斑区高反射光带消失的改变[5]。因叶黄素具有抗氧化和抗炎作用,已被尝试用于激光黄斑损伤的病例中。Zhao等[17]的病例报道中,给予激光黄斑损伤患者服用20 mg叶黄素治疗12个月后,视力略有改善。有病例报道给予泼尼松龙0.5 mg/(kg·d)联合叶黄素的口服方案,可加速黄斑水肿消退及光感受器重建,部分患者3周内显著恢复视力[53]。局部Tenon囊下注射曲安奈德注射液:早期注射可通过抗炎作用减轻视网膜水肿与炎症反应,可作为受伤后急性期的治疗手段。Cankurtaran等[33]报道了一例激光所致黄斑损伤患者在受伤当天接受了球结膜颞上象限注射曲安奈德注射液(40 mg)治疗后,3个月内OCT显示外层视网膜高反射带减少,视力逐步改善。
4.2 手术治疗
4.2.1 玻璃体切割术、联合内界膜剥离手术
激光所致黄斑全层裂孔虽与特发性黄斑裂孔发病机制不同,但国内外均有散在病例报道,证明玻璃体切割术,联合内界膜剥离手术可改善患者预后视力[65-66]。陈燕云等[67]回顾性分析了12例激光所致黄斑全层裂孔患者,黄斑裂孔术后裂孔均完全闭合,11例患者视力有所提高,仅有1例患者术后视力未提高,考虑与患眼RPE层受损严重及病程长等因素有关。
4.2.2 YAG激光
有病例报道对于玻璃体腔黄斑部玻璃体后皮质下及内界膜下出血的患者使用YAG激光切开玻璃体后界膜及内界膜,将出血引入玻璃体腔内,1个月后最佳矫正视力由0.05提升至0.80, 黄斑部中心凹变平,其下的肌样体带、EZ、IZ以及外界膜结构完整[68]。
4.2.3 玻璃体药物注射治疗抗血管内皮生长因子(vascular endothelial growth factor, VEGF)疗法
针对激光后黄斑区继发性CNV的患者,玻璃体内注射抗VEGF药物可抑制血管渗漏、缩小病灶面积。有病例报道,一例CNV患者经抗VEGF单药治疗2个月后视力有所改善[68]。
5 总结与展望
随着国际上激光黄斑损伤的病例报道数量增加,此类眼部外伤已成为日益严重的公共卫生与安全问题[64]。在受伤的患者中,儿童占多数,这与激光逐渐玩具化和儿童对于激光的危险缺乏认识有关。当患者有意隐瞒病史时,眼部表现易误诊为视网膜遗传性疾病,如卵黄样病变、视锥视杆细胞营养不良和Stargardt病,需要以多模态成像为核心综合多个影像学检查来确诊。临床中最常见的黄斑区损伤为非特异性中央凹RPE层变化和独特的黄色或灰色病变,此类患者视力预后较好。而出现黄斑下出血、全层黄斑裂孔和脉络膜新生血管的患者视力受损较重。OCT检查在疾病的诊断中起着重要作用[69],并可作为长期随访的检查。激光所致黄斑损伤中最关键的干预措施是进行科普和宣教,提高公众对此类损伤的认知。如怀疑患者为自伤,则需建议进行心理干预。对于激光黄斑损伤目前还没有公认的治疗方案,虽然很多医生会首选口服糖皮质激素及抗氧化药物保守治疗,但因为缺乏对照组,目前给药量、时间窗及效果还未明确,这需要进一步研究。而对于全层黄斑裂孔的患者,则建议短期保守治疗无改善,则考虑手术治疗。综上所述,对于激光所致的黄斑损伤未来需做到精准防护及广泛的科普教育,增强市场监管,避免不合规激光类玩具流入市场。最后黄斑激光损伤的治疗还需要大样本的、多中心的临床随机对照试验,从而确定治疗方案,挽救患者视功能。
声明
在本作品的准备过程中,作者使用了Deepseek进行文字润色。使用此工具后,作者根据需要对内容进行了审查和编辑,并对出版物的内容承担全部责任。
利益冲突
所有作者均声明不存在利益冲突。
开放获取声明
本文适用于知识共享许可协议(Creative Commons),允许第三方用户按照署名(BY)-非商业性使用(NC)-禁止演绎(ND)(CC BY-NC-ND)的方式共享,即允许第三方对本刊发表的文章进行复制、发行、展览、表演、放映、广播或通过信息网络向公众传播,但在这些过程中必须保留作者署名、仅限于非商业性目的、不得进行演绎创作。
基金
参考文献
1. Al-Amry MA, Alsulaiman SM, Ghazi NG. Anterior segment injury by a high-power handheld blue laser device[J]. Ocul Immunol Inflamm, 2018, 26(8): 1174-1176. DOI: 10.1080/09273948.2017.1327603.
2. Androudi S, Papageorgiou E. Macular hole from a laser pointer[J]. N Engl J Med, 2018, 378(25): 2420. DOI: 10.1056/NEJMicm1714488.
3. Bhavsar KV, Michel Z, Greenwald M, et al. Retinal injury from handheld lasers: a review[J]. Surv Ophthalmol, 2021, 66(2): 231-260. DOI: 10.1016/j.survophthal.2020.06.006.
4. Hanson JVM, Sromicki J, Mangold M, et al. Maculopathy following exposure to visible and infrared radiation from a laser pointer: a clinical case study[J]. Doc Ophthalmol, 2016, 132(2): 147-155. DOI: 10.1007/s10633-016-9530-5.
5. Hossein M, Bonyadi J, Soheilian R, et al. SD-OCT features of laser pointer maculopathy before and after systemic corticosteroid therapy[J]. Ophthalmic Surg Lasers Imaging, 2011, 42: e135-8. DOI: 10.3928/15428877-20111208-03.
6. Joubert R, Farguette F, Chevreaud O, et al. Unilateral maculopathy in a young male patient: a photic laser injury[J]. J Fr Ophtalmol, 2016, 39(9): 786-790. DOI: 10.1016/j.jfo.2016.03.014.
7. Keunen JEE, Delbecq AMH, Cruysberg JRMH, et al. Laser pointers are not toys; eye injury with permanent loss of visual acuity[J]. Ned Tijdschr Geneeskd, 2014, 158: A7813.
8. Raoof N, Bradley P, Theodorou M, et al. The new pretender: a large UK case series of retinal injuries in children secondary to handheld lasers[J]. Am J Ophthalmol, 2016, 171: 88-94. DOI: 10.1016/j.ajo.2016.08.027.
9. Mainster MA, Stuck BE, Brown J Jr. Assessment of alleged retinal laser injuries[J]. Arch Ophthalmol, 2004, 122(8): 1210-1217. DOI: 10.1001/archopht.122.8.1210.
10. Sheyman AT, Nesper PL, Fawzi AA, et al. Adaptive optics imaging in laser pointer maculopathy[J]. Ophthalmic Surg Lasers Imaging Retina, 2016, 47(8): 782-785. DOI: 10.3928/23258160-20160808-14.
11. Turaka K, Bryan JS, Gordon AJ, et al. Laser pointer induced macular damage: case report and mini review[J]. Int Ophthalmol, 2012, 32(3): 293-297. DOI: 10.1007/s10792-012-9555-z.
12. Weng CY, Baumal CR, Albini TA, et al. Self-induced laser maculopathy in an adolescent boy utilizing a mirror[J]. Ophthalmic Surg Lasers Imaging Retina, 2015, 46(4): 485-488. DOI: 10.3928/23258160-20150422-15.
13. Xu K, Chin EK, Quiram PA, et al. Retinal injury secondary to laser pointers in pediatric patients[J]. Pediatrics, 2016, 138(4): e20161188. DOI: 10.1542/peds.2016-1188.
14. Xu M, Lin T. Bilateral central scotomas following laser pointer misuse[J]. CMAJ, 2014, 186(9): E341. DOI: 10.1503/cmaj.130975.
15. Yan W, Chakrabarti R, Little M, et al. Green-laser induced maculopathy in a 15-year-old boy[J]. J AAPOS, 2016, 20(3): 258-260. DOI: 10.1016/j.jaapos.2015.11.016.
16. Zhang L, Zheng A, Nie H, et al. Laser-induced photic injury phenocopies macular dystrophy[J]. Ophthalmic Genet, 2016, 37(1): 59-67. DOI: 10.3109/13816810.2015.1059458.
17. Zhao N, Liu L. Long-term changes in optic coherence tomography in a child with laser pointer maculopathy: a case report and mini review[J]. Photodiagnosis Photodyn Ther, 2017, 18: 264-266. DOI: 10.1016/j.pdpdt.2017.03.012.
18. Takac S, Stojanović S. Classification of laser irradiation and safety measures[J]. Med Pregl, 1998, 51(9-10): 415-418.
19. Neffendorf JE, Hildebrand GD, Downes SM. Handheld laser devices and laser-induced retinopathy (LIR) in children: an overview of the literature[J]. Eye, 2019, 33(8): 1203-1214. DOI: 10.1038/s41433-019-0395-1.
20. Torp-Pedersen T, Welinder L, Justesen B, et al. Laser pointer maculopathy - on the rise?[J]. Acta Ophthalmol, 2018, 96(7): 749-754. DOI: 10.1111/aos.13856.
21. Farassat N, Boehringer D, Luebke J, et al. Incidence and long-term outcome of laser pointer maculopathy in children[J]. Int Ophthalmol, 2023, 43(7): 2397-2405. DOI: 10.1007/s10792-023-02638-w.
22. Lund DJ, Stuck BE, Edsall P. Retinal injury thresholds for blue wavelength lasers[J]. Health Phys, 2006, 90(5): 477-484. DOI: 10.1097/01.HP.0000190115.83416.cb.
23. Schmitz-Valckenberg S, Guo L, Maass A, et al. Real-time in vivo imaging of retinal cell apoptosis after laser exposure[J]. Invest Ophthalmol Vis Sci, 2008, 49(6): 2773-2780. DOI: 10.1167/iovs.07-1335.
24. Schulmeister K, Stuck BE, Lund DJ, et al. Review of thresholds and recommendations for revised exposure limits for laser and optical radiation for thermally induced retinal injury[J]. Health Phys, 2011, 100(2): 210-220. DOI: 10.1097/HP.0b013e3181ea51e3.
25. Luecking M, Brinkmann R, Ramos S, et al. Capabilities and limitations of a new thermal finite volume model for the evaluation of laser-induced thermo-mechanical retinal damage[J]. Comput Biol Med, 2020, 122: 103835. DOI: 10.1016/j.compbiomed.2020.103835.
26. Pizzirani S, Davidson MG, Gilger BC. Transpupillary diode laser retinopexy in dogs: ophthalmoscopic, fluorescein angiographic and histopathologic study[J]. Vet Ophthalmol, 2003, 6(3): 227-235. DOI: 10.1046/j.1463-5224.2003.00299.x.
27. Jahnke L, Zandi S, Elhelbawi A, et al. Characterization of macroglia response during tissue repair in a laser-induced model of retinal degeneration[J]. Int J Mol Sci, 2023, 24(11): 9172. DOI: 10.3390/ijms24119172.
28. Cain CP, Toth CA, Noojin GD, et al. Thresholds for retinal injury from multiple near-infrared ultrashort laser pulses[J]. Health Phys, 2002, 82(6): 855-862. DOI: 10.1097/00004032-200206000-00014.
29. Belokopytov M, Belkin M, Dubinsky G, et al. Development and recovery of laser-induced retinal lesion in rats[J]. Retina, 2010, 30(4): 662-670. DOI: 10.1097/IAE.0b013e3181bd2fa9.
30. Wiest MRJ, Gunzinger JM, Hamann T, et al. Natural course of solar and laser-associated retinal and macular injuries at a primary care hospital in Switzerland[J]. Klin Monbl Augenheilkd, 2023, 240(4): 516-521. DOI: 10.1055/a-2021-7724.
31. Gebara A, Vofo BN, Jaouni T. Branch retinal artery occlusion from laser pointer misuse[J]. Am J Ophthalmol Case Rep, 2024, 36: 102118. DOI: 10.1016/j.ajoc.2024.102118.
32. Lee GD, Baumal CR, Lally D, et al. Retinal injury after inadvertent handheld laser exposure[J]. Retina, 2014, 34(12): 2388-2396. DOI: 10.1097/IAE.0000000000000397.
33. Cankurtaran M, Şekeryapan Gediz B. Sub-tenon triamcinolone acetonide injection in the acute treatment of handheld laser-induced maculopathy[J]. Turk J Ophthalmol, 2022, 52(4): 281-285. DOI: 10.4274/tjo.galenos.2022.46095.
34. 李传志. 黄斑激光损伤一例报告[J]. 中华眼科杂志, 1978, 2(14): 127.
Li CZ. A case report of macular laser injury[J]. Chin J Ophthalmol, 1978, 2(14): 127.
35. Plăcintă IA, De Freitas RA, Rahhal-Ortuño M, et al. Retinal toxicity after facial laser epilation[J]. Rom J Ophthalmol, 2020, 64(1): 70-74. DOI: 10.22336/rjo.2020.14.
36. Shum JWH, Iu LPL, Cheung DN, et al. A case of accidental ocular injury from cosmetic laser burn[J]. Retin Cases Brief Rep, 2016, 10(2): 115-120. DOI: 10.1097/ICB.0000000000000181.
37. Linton E, Walkden A, Steeples LR, et al. Retinal burns from laser pointers: a risk in children with behavioural problems[J]. Eye, 2019, 33(3): 492-504. DOI: 10.1038/s41433-018-0276-z.
38. Faraj S, Bathen ME, Galeckas A, et al. Retinal injuries in seven teenage boys from the same handheld laser[J]. Am J Ophthalmol Case Rep, 2022, 27: 101596. DOI: 10.1016/j.ajoc.2022.101596.
39. Petrou P, Patwary S, Banerjee PJ, et al. Bilateral macular hole from a handheld laser pointer[J]. Lancet, 2014, 383(9930): 1780. DOI: 10.1016/S0140-6736(14)60757-1.
40. Dhoot DS, Xu D, Srivastava S. High-powered laser pointer injury resulting in macular hole formation[J]. J Pediatr, 2014, 164(3): 668. e1. DOI: 10.1016/j.jpeds.2013.11.019.
41. Fujinami K, Yokoi T, Hiraoka M, et al. Choroidal neovascularization in a child following laser pointer-induced macular injury[J]. Jpn J Ophthalmol, 2010, 54(6): 631-633. DOI: 10.1007/s10384-010-0876-z.
42. Porrúa L, Oblanca N, González-López JJ. Spontaneous closure of a blue laser induced full thickness macular hole[J]. Arch Soc Esp Oftalmol, 2017, 92(1): 29-32. DOI: 10.1016/j.oftal.2016.08.004.
43. Qi Y, Wang Y, You Q, et al. Surgical treatment and optical coherence tomographic evaluation for accidental laser-induced full-thickness macular holes[J]. Eye, 2017, 31(7): 1078-1084. DOI: 10.1038/eye.2017.41.
44. Alsulaiman SM, Alrushood AA, Almasaud J, et al. Full-thickness macular hole secondary to high-power handheld blue laser: natural history and management outcomes[J]. Am J Ophthalmol, 2015, 160(1): 107-113. e1. DOI: 10.1016/j.ajo.2015.04.014.
45. Perez-Montaño CR, Palomares-Ordoñez JL, Ramirez-Estudillo A, et al. Sub-hyaloid and sub-internal limiting membrane macular hemorrhage after laser exposure at music festival: a case report[J]. Doc Ophthalmol, 2019, 138(1): 71-76. DOI: 10.1007/s10633-018-9666-6.
46. Yeo DCM, Osei-Bempong C, Shirodkar A, et al. Foveal haemorrhage from makeshift 'Lightsaber': funduscopy and optical coherence tomography findings[J]. BMJ Case Rep, 2016, 2016: bcr2016214711. DOI: 10.1136/bcr-2016-214711.
47. Liu K, Wang N, Peng X, et al. Long-term effect of laser-induced ocular hypertension on the cone electroretinogram and central macular thickness in monkeys[J]. Photomed Laser Surg, 2014, 32(7): 371-378. DOI: 10.1089/pho.2013.3693.
48. Dhrami-Gavazi E, Lee W, Balaratnasingam C, et al. Multimodal imaging documentation of rapid evolution of retinal changes in handheld laser-induced maculopathy[J]. Int J Retina Vitreous, 2015, 1: 14. DOI: 10.1186/s40942-015-0014-7.
49. Wang Q, Lin X, Xiang W, et al. Assessment of laser induction of Bruch’s membrane disruption in monkey by spectral-domain optical coherence tomography[J]. Br J Ophthalmol, 2015, 99(1): 119-124. DOI: 10.1136/bjophthalmol-2014-305813.
50. Mtanes K, Mimouni M, Zayit-Soudry S. Laser pointer-induced maculopathy: more than meets the eye[J]. J Pediatr Ophthalmol Strabismus, 2018, 55(5): 312-318. DOI: 10.3928/01913913-20180405-01.
51. Xiao H, Liu X, Huang J, et al. Image characters of optical coherence tomography in laser-induced maculopathy[J]. Yan Ke Xue Bao, 2010, 25(2): 82-85. DOI: 10.3969/g.issn.1000-4432.2010.02.005.
52. Jiang F, Shi Y, Wang Z, et al. Case series of photic maculopathy associated with exposure to a plasma flash induced by a femtosecond laser[J]. Lasers Surg Med, 2022, 54(5): 631-638. DOI: 10.1002/lsm.23519.
53. Marinescu AI, Hall CM. Laser-induced maculopathy and outcomes after treatment with corticosteroids and lutein[J]. Cureus, 2021, 13(10): e18470. DOI: 10.7759/cureus.18470.
54. Falavarjani KG, Au A, Anvari P, et al. En face OCT of type 2 neovascularization: a reappraisal of the pitchfork sign[J]. Ophthalmic Surg Lasers Imaging Retina, 2019, 50(11): 719-725. DOI: 10.3928/23258160-20191031-07.
55. Williams DR, Burns SA, Miller DT, et al. Evolution of adaptive optics retinal imaging[J]. Biomed Opt Express, 2023, 14(3): 1307-1338. DOI: 10.1364/BOE.485371.
56. Wang Y, La TT, Mason M, et al. Case report: multimodal, longitudinal assessment of retinal structure and function following laser retinal injury[J]. Optom Vis Sci, 2023, 100(4): 281-288. DOI: 10.1097/OPX.0000000000002004.
57. Fang D, Liang J, Diao Y, et al. Morphologic and functional assessment of photoreceptors in laser-induced retinopathy using adaptive optics scanning laser ophthalmoscopy and microperimetry[J]. Am J Ophthalmol, 2024, 265: 61-72. DOI: 10.1016/j.ajo.2024.03.021.
58. Vitellas C, Doble N, Wells-Gray EM, et al. Cone photoreceptor integrity assessed with adaptive optics imaging after laser pointer-induced retinal injury[J]. Retin Cases Brief Rep, 2022, 16(5): 586-592. DOI: 10.1097/ICB.0000000000001025.
59. Sukkarieh G, Lejoyeux R, LeMer Y, et al. The role of near-infrared reflectance imaging in retinal disease: a systematic review[J]. Surv Ophthalmol, 2023, 68(3): 313-331. DOI: 10.1016/j.survophthal.2022.12.003.
60. Hu W, Cai W, Wu Y, et al. Topical application of cell-penetrating peptide modified anti-VEGF drug alleviated choroidal neovascularization in mice[J]. Int J Nanomedicine, 2024, 19: 35-51. DOI: 10.2147/IJN.S428684.
61. Veronese C, Maiolo C, Huang D, et al. Optical coherence tomography angiography in pediatric choroidal neovascularization[J]. Am J Ophthalmol Case Rep, 2016, 2: 37-40. DOI: 10.1016/j.ajoc.2016.03.009.
62. Tomasso L, Benatti L, La Spina C, et al. Optical coherence tomography angiography findings in laser maculopathy[J]. Eur J Ophthalmol, 2017, 27(1): e13-e15. DOI: 10.5301/ejo.5000844.
63. Liang L, Cui Z, Lu C, et al. Damage to the macula associated with LED-derived blue laser exposure: a case report[J]. BMC Ophthalmol, 2017, 17(1): 49. DOI: 10.1186/s12886-017-0448-9.
64. Birtel J, Harmening WM, Krohne TU, et al. Retinal injury following laser pointer exposure[J]. Dtsch Arztebl Int, 2017, 114(49): 831-837. DOI: 10.3238/arztebl.2017.0831.
65. Chen YJ. Vitrectomy and microperimetry of an accidental macular hole caused by Nd: YAG laser[J]. Case Rep Ophthalmol, 2010, 1(2): 80-84. DOI: 10.1159/000321631.
66. Sou R, Kusaka S, Ohji M, et al. Optical coherence tomographic evaluation of a surgically treated traumatic macular hole secondary to Nd: YAG laser injury[J]. Am J Ophthalmol, 2003, 135(4): 537-539. DOI: 10.1016/s0002-9394(02)02075-5.
67. 陈燕云, 卢宁, 李继鹏, 等. 激光意外损伤所致黄斑裂孔行玻璃体切除联合内界膜剥离术治疗效果观察[J]. 中华医学杂志, 2018, 98(48): 3941-3945. DOI: 10.3760/cma.j.issn.0376-2491.2018.48.007.
Chen YY, Lu N, Li JP, et al. Results of pars Plana vitrectomy with peeling of the inner limiting membrane in patients with laserinduced macular hole[J]. Natl Med J China, 2018, 98(48): 3941-3945. DOI: 10.3760/cma.j.issn.0376-2491.2018.48.007.
68. 冯程程, 高艳, 陈楠, 等. 激光笔所致儿童黄斑损伤的OCT表现及预后观察[J]. 中华眼视光学与视觉科学杂志, 2024, 26(3): 186-192. DOI: 10.3760/cma.j.cn115909-20231103-00168.
Feng CC, Gao Y, Chen N, et al. OCT manifestations and prognosis of macular damage in children caused by laser pen[J]. Chin J Optom Ophthalmol Vis Sci, 2024, 26(3): 186-192. DOI: 10.3760/cma.j.cn115909-20231103-00168.
69. Alsulaiman SM, Alrushood AA, Almasaud J, et al. High-power handheld blue laser-induced maculopathy: the results of the King Khaled Eye Specialist Hospital Collaborative Retina Study Group[J]. Ophthalmology, 2014, 121(2): 566-572. e1. DOI: 10.1016/j.ophtha.2013.09.006.